- Details
- Geschrieben von: CF
- Kategorie: Magen
- Zugriffe: 5098
→ Definition: Das Magenfrühkarzinom (= early-gastric-cancer) ist definiert als Karzinom, das im Vergleich zum Carcinoma in situ (TIS) eine Strumainfiltration aufweist und die Mucosa (Typ M) bzw. Lamina submucosa (Typ SM) nicht überschreitet, unabhängig vom Nachweis von Lymphknotenmetastasen (T1/Nx) und der Flächenausdehnung.
→ Epidemiologie:
→ I: In Deutschland machen die Magenfrühkarzinome einen Anteil von 10-15% aller Magenkarzinome aus.
→ II: In Japan mit hoher Magenkarzinom-Inzidenz liegt sie aufgrund der intensiven Vorsorgeuntersuchungen bei ca. 50%.
→ III: Lokalisation: Das Magenfrühkarzinom ist insbesondere im distalen -, seltener im proximalen Magen nachzuweisen.
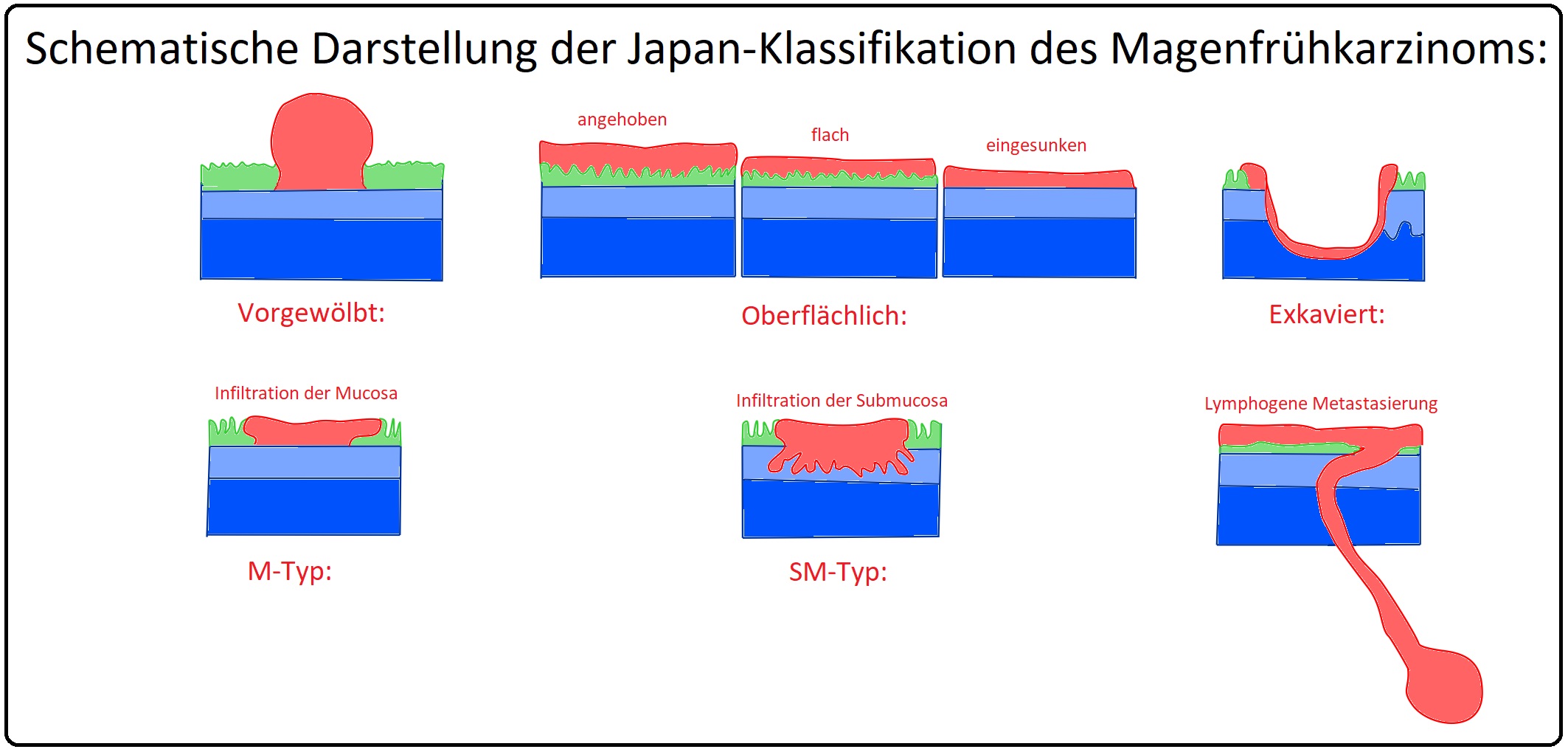
→ Klassifikation: Die Einteilung des Magenfrühkarzinoms erfolgt nach der Japan-Klassifikation nach:
→ I: Infiltrationstiefe:
→ 1) M-Typ: Infiltriert bis in die Mucosa. Die Lymphknotenmetastasen-Rate liegt bei diesem Typ zwischen 4-5%.
→ 2) SM-Typ: Das Karzinom durchbricht die Mucosa und reicht bis in die Submukosa. Hierbei ist die LK-Metastasenrate mit bis zu 22% deutlich höher.
→ II: Morphologie: Makroskopisch werden diese Karzinom nochmals unterteilt in:
→ 1) Typ I: Polypöse Magenfrühkarzinome.
→ 2) Typ II: Flache Magenfrühkarzinome, die eine weitere Klassifikation aufweisen:
→ A) Typ IIa: Leicht erhaben.
→ B) TypIIb: Im Schleimhautniveau liegend und
→ C) Typ IIc: Unterhalb des Schleimhautniveaus liegend.
→ 3) Typ III: Hierbei handelt es sich um eine ulzerierendes Magenfrühkarzinom.
→ Klinisch-relevant:
→ A) Die Mehrzahl der Magenfrühkarzinome ist im Durchmesser größer als 2cm.
→ B) Nach der Lauren-Klassifikation findet man beim Magenfrühkarzinom häufiger den intestinalen als den diffusen Typ und in 5-12% der Fälle tritt es sogar multizentrisch auf.
→ C) Die lymphogene Metastasierungsrate nimmt mit der Infiltrationstiefe zu.
→ Klinik: Die klinische Symptomatik des Magenfrühkarzinom ist sehr uncharakteristisch. In vielen Fällen (> 90%) zeigt sich jedoch eine Infektion mit Helico-bacter pylori.
→ Diagnose:
→ I: Im Vordergrund der Diagnose steht die Gastroskopie mit Biopsie und Histologie. Die häufigsten Befunde sind u.a.:
→ 1) Farbveränderungen der Mucosaoberfläche.
→ 2) Zudem ist die Oberfläche stumpf und aufgeraut und kann unregelmäßige Stufen am Läsionsrand oder breitbasige Erhebungen aufweisen.
→ II: Endosonographie: Zur Erfassung der Infiltrationstiefe des Tumors und möglicher regionärer Lymphknotenmetastasen.
→ Differenzialdiagnosen: Vom Magenfrühkarzinom müssen insbesondere nachfolgende Erkrankungen abgegrenzt werden:
→ I: Chronische Gastrits und gastroduodenale Ulkuskrankheit (Ulcus ventriculi und Ulcus duodeni).
→ II: Weitere Malignome wie Magenkarzinom, MALT-Lymphom, gastrointestinale Stromatumoren, etc.
→ Therapie: Insbesondere beim Magenfrühkarzinom vom M-Typ haben sich minimal-invasive Behandlungsverfahren etabliert; hierzu zählen u.a.:
→ I: Endoskopische Mukosaresektion: (= EMR) Stellt eine Behandlungsmethode des Frühkarzinoms insbesondere im Bereich des Ösophagus und Magens dar.
→ 1) Indikationen: Sind u.a. auf die Mukosa beschränkte Frühkarzinome des Ösophagus und kleinere – des Magens sowie größere Magenadenome.
→ 2) Durchführung:
→ II: Laparoskopische-intragastrale Mukosaresektion:
→ 1) Bei diesem Verfahren wird das suspekte Areal bzw. Tumor endoskopisch markiert. Im Anschluss werden 3 Trokare und das Laparoskop in das Magenlumen eingeführt, der Tumor nochmals inspiziert und die Resektionsgrenzen bestimmt. Nun erfolgt eine En-bloc-Resektion mit einem Thermokauter oder Ultraschalldissektor sowie die Bergung des Resektats mittels Gastroskop.
→ 2) Diese Methode wird angewandt, wenn die endoskopische Mukosaresektion technisch zu schwierig ist. Vorteil ist die durch den simultane Einsatz von Gastroskop und Laparoskop exakte Bestimmbarkeit des Sicherheitsabstands.
→ III: Laparoskopisch-endoskopische lokale Vollwandexzision: Der Tumor wird primär endoskopisch markiert und ein sogenannter T-Lifter durch die Bauchwand in das Magenlumen vorgeschoben. Hierbei ist es wichtig die Neoplasie nicht zu penetrieren. Nun wird der Tumor mit dem T-Lifter angehoben und anschließend unter endoskopischer Kontrolle mit dem Klammerapparat tangential reseziert. Das Resektat wird über einen Bergebeutel geborgen. Vorteile dieses Verfahrens sind insbesondere die Vermeidung der R1-Resektion sowie der postoperativen Ulkusbildung.
→ IV: Ultima ratio ist die Gastrektomie.
→ Prognose: Die Prognose des Magenfrühkarzinoms ist deutlich günstiger als beim Magenkarzinom obwohl z.T. Lymphknotenmetastasen existieren. Die 5-Jahresüberlebenschance liegt:
→ I: Beim M-Typ bei 95% und
→ II: Beim SM-Typ bei 85%.
- Details
- Kategorie: Magen
- Zugriffe: 14941
→ Allgemein: Die chirurgische Intervention der Ulkuskrankheit hat sich nach Einführung der Eradikationstherapie deutlich vermindert. Die operativen Therapien haben zum Ziel:
→ I: Die Säuresekretion zu reduzieren (konservativ nicht beherrschbar) und evtl. Magenulzerationen (Ulcus ventriculi) zu entfernen.
→ II: Akute lebenbedrohliche Komplikationen der Ulkuskrankheit wie Perforation und Blutungen abzuwenden.
→ Klinisch-relevant: Bei der operative Therapie unterscheidet man zwischen:
→ A) Nicht-resezierenden operativen Verfahren und
→ B) Resezidierende Verfahren.
→ I: Nicht resezierende Verfahren: Hierzu gehören u.a.:
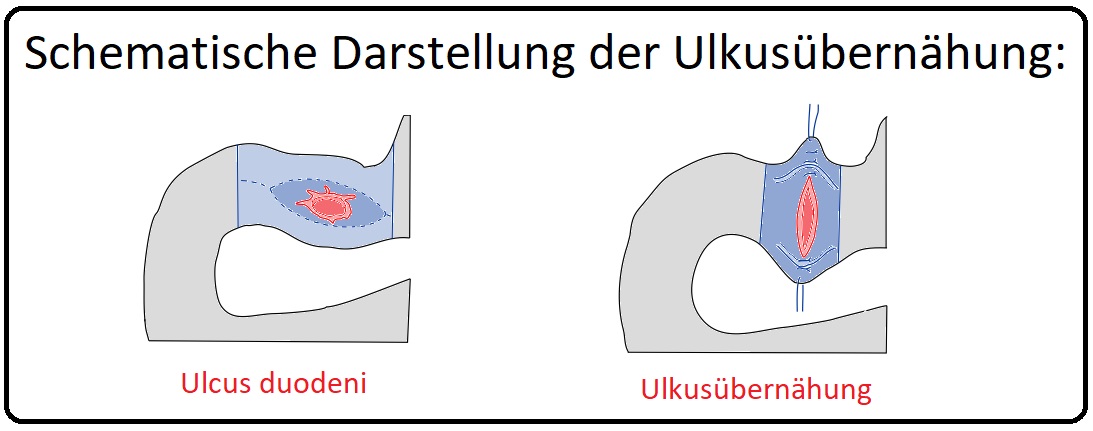
→ A) Ulkusübernähung: Bei akuten Perforationen
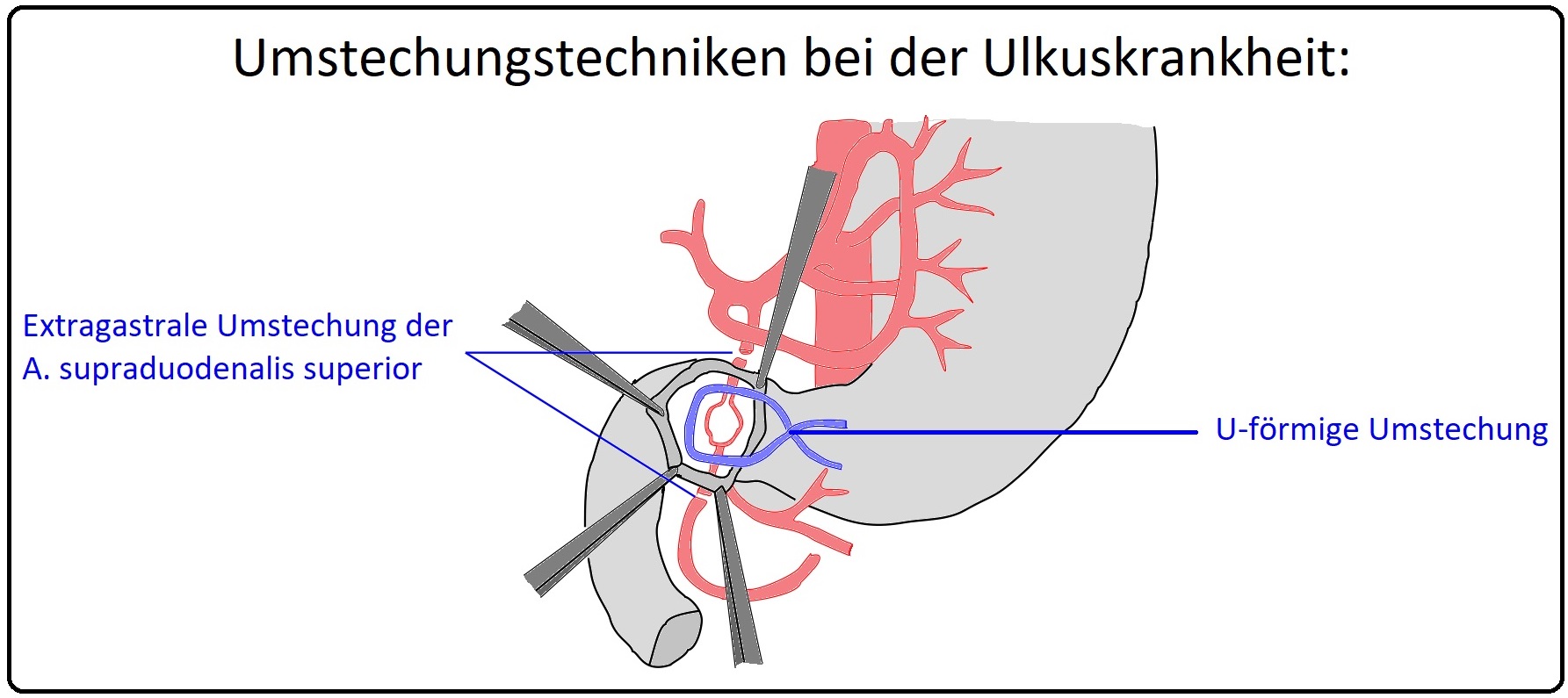
→ B) Ulkusumstechung: Bei endoskopisch nicht beherrschbaren Blutungen aus arrodierten Arterien. Gerade bei den Ulzerationen im Bereich der Bulbushinterwand ist die A. gastroduodenalis oftmals betroffen.
→ C) Vagotomie: Mit oder ohne Pyloroplastik.
→ 1) Ulkusübernähung: Bei einer Perforation ist eine sofortige operative Therapie indiziert. Diese kann laparoskopisch oder durch eine mediane Laparotomie erfolgen. Der Ulkus wird längsovalär exzidiert (Histologie zum Maligintätsausschluss) und mittels Einzelknopfnaht quer verschlossen. In die Perforationsstelle wird eine Drainage eingelegt.
→ 2) Ulkusumstechung: Ist eine Magenblutung endoskopisch nicht beherrschbar erfolgt eine Gastrotomie. Sichtbar blutende Gefäßstümpfe werden direkt umstochen (intraluminale Ligatur). Bei nicht sichtbaren Blutungen ist eine 4 Quadranten-Umstechung, bei der an allen 4 Ulkusseiten eine durchgreifende Ligatur gesetzt wird, indiziert.
→ Klinisch-relevant: Bei Ulzerationen im Bereich der Bulbushinterwand besteht die Gefahr der Arrosion der A. gastroduodenalis (A. pankreaticoduodenalis). Es empfiehlt sich, die Arterien proximal und distal der Unterkreuzung des Duodenumabschnitts extraluminal zu umstechen (legieren).
→ A) Ziel hierbei ist es die Säureproduktion (Säurereduktion von 60-70%) der Belegzellen durch Ausschaltung der vagalen Stimulation (Denervierung) zu minimieren.
→ B) Bei diesem Verfahren ist die Säurereduktion geringer als bei der 2/3 Magenresektion, aber noch ausreichend, um als Therapie der gastroduodenalen Ulkuskrankheit eingesetzt zu werden.
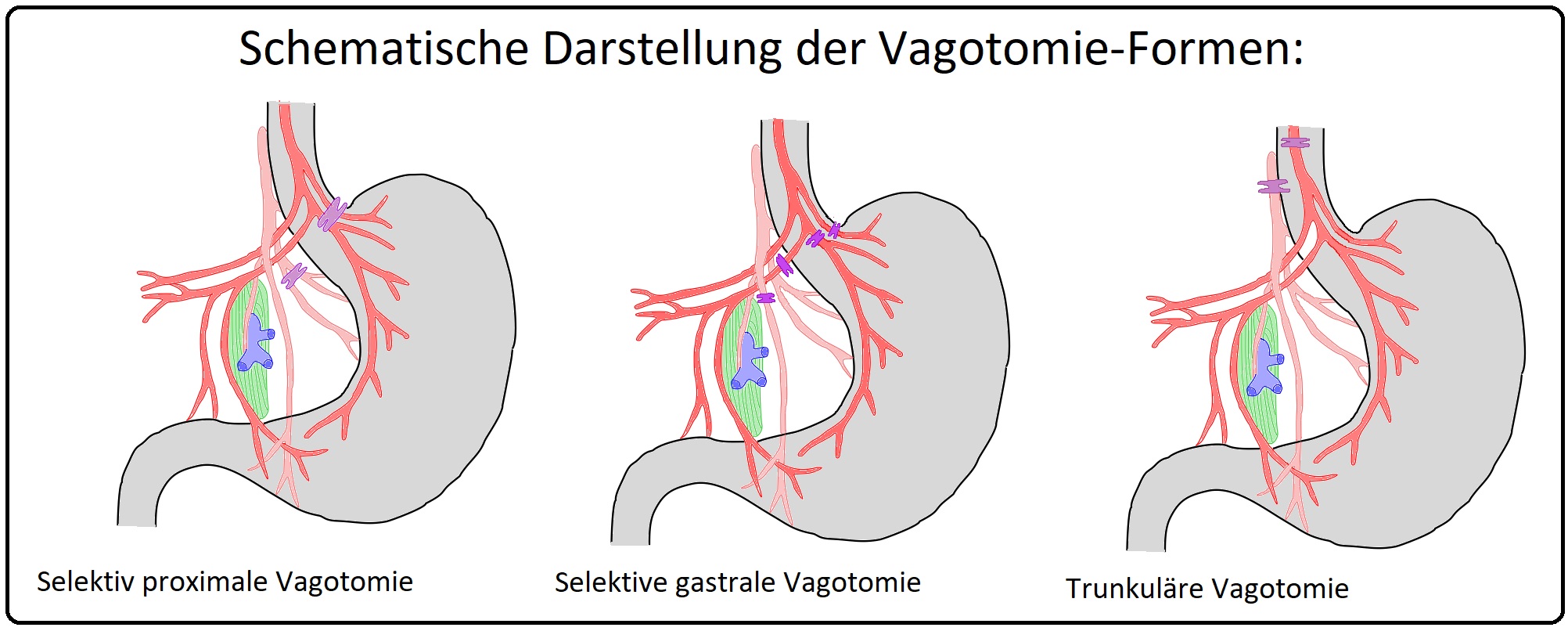
→ Klassifikation: Bei der Vagotomie unterscheidet man v.a.:
→ I: Trunkuläre Vagotomie: (= VT) Hierbei werden sämtliche subdiaphragmale Vagusäste durchtrennt. Es sind neben den gastralen Ästen auch die extragastralen Vagusäste (zur Leber, Dickdarm und Pankreas) mitbetroffen.
→ 1) Prinzip: Durchtrennung der Vagusstämme kurz unterhalb des Diaphragmas vor Abgang der hepatopylorischen Äste bzw. des Rumus coeliacus. Folge ist eine vagale Denervierung des Oberbauches (Leber, Pankreas, Gallenblase, Magen, Dickdarm)
→ 2) Nebenwirkungen: Sind Cholelithiasis, Diarrhoe, exokrine Pankreasinsuffizienz und aufgrund der Durchtrennung der antralen Vagusäste eine Lähmung des Pylorus. Folge ist die Anlage einer Pyloroplastik.
→ Klinisch-relevant: Die trunkuläre Vagotomie ist heutzutage obsolet.
→ II: Selektive-totale-Vagotomie: (= SVT) Wird auch als totale gastrale Vagotomie bezeichnet. Hier erfolgt die Ausschaltung aller gastralen Äste unter Aussparung der extragastralen. Die Indikation besteht bei schwerer Magenausgangsstenose oder wenn eine proximale-gastrale-Vagotomie nicht möglich ist.
→ 1) Prinzip: Durchtrennung der Vagusstämme unterhalb des Diaphragmas nach Abgang der hepatopylorischen Äste bzw. des Ramus coeliacus.
→ 2) Indikation: Sind u.a.:
→ A) Chronisches, therapieresistentes Ulcus duodeni,
→ B) Schwere Magenausgangsstenose etc.
→ 3) Nebenwirkungen: Lähmung des Pylorus. Folge ist die Anlage einer Pyloroplasik.
→ III: Selektive-proximale-Vagotomie: Sie wird auch als proximale gastrale Vagotomie bezeichnet. Es erfolgt einer Denervierung des proximalen Magens im Bereich des belegzellenreichen Fundus und Corpus. Der vordere und hintere Latarjet (= R. antralis des Nervus vagus) wird belassen. Hiermit wird eine nachfolgende Pyloroplastik vermieden. Klassische Indikationsstellung ist ein nicht mehr konservativ-behandelbarer, therapieresistenter Ulcus duodeni.
→ Klinisch-relevant: Um das Rezidivrisiko zu minimieren, ist eine vollständige Denervierung im Bereich des distalen Ösophagus, der kleinen Kurvatur bis zur Incisura angularis und proximalen Magenfundus indiziert.
→ Komplikationen: Wichtige z.T. schwerwiegende Komplikationen sind insbesondere:
→ I: Milzverletzungen (1-2%),
→ II: Distale Ösophagusverletzungen (1-2%),
→ III: Rezidivulkus (6-10%),
→ IV: Motilitätsstörungen und Diarrhoe.
→ II: Resezierende operative Verfahren: (Siehe dort).