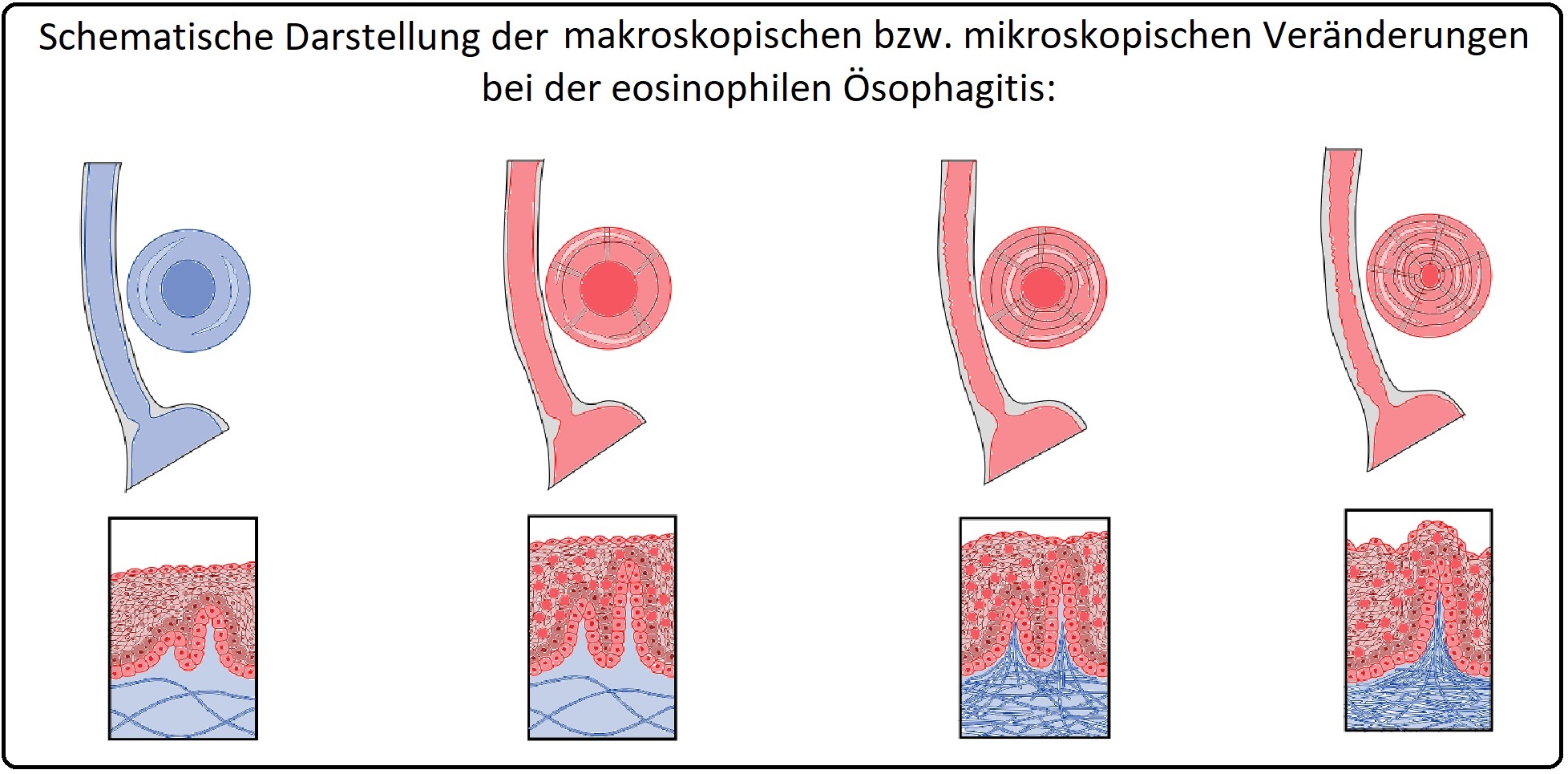
→ Definition: Bei der eosinophilen Ösophagitis handelt es sich um eine chronisch-entzündliche, immunvermittelte Erkrankung des Ösophagus mit Nachweis einer eosinophil dominierenden Inflammation (= Infiltation von eosinophilen Granulozyten) der Mukosa und Submucosa und einer Symptomatik der ösophagealen Dysfunktion.
→ Epidemiologie:
→ I: Es zeigt sich in den westlichen Industrieländern eine Prävalenz von 40/100000 mit steigender Tendenz.
→ II: Die eosinophlie Ösophagitis kann in jedem Lebensalter auftreten; es zeigt sich jedoch ein Manifestationsgipfel zwischen dem 30.-50. Lebensjahr, wobei Männer häufiger als Frauen betroffen sind (M : F = 3 : 1).
→ Ätiopathogenese: Bei der eosinophilen Ösophagitis zeigt sich eine familiäre Häufung.
→ I: Zum einen ist ein Polymorphismus im CCL26-Gen, welche das Eotaxin-3 kodiert, nachweisbar, zum anderen konnten Varianten im Chromosom 5q22 (WDR36-Gen, TSLP-Gen) identifiziert werden.
→ II: Zudem erhöhen perinatale Umweltfaktoren wie Kaiserschnitt, Frühgeburt, mütterliches Fieber, etc. die Inzidenz. Aber auch die Gabe von Antibiotika und Protonenpumpen-Inhibitoren im Kindesalter können die Entwicklung begünstigen.
→ III: Weitere Ursachen: Hierfür sind unter anderem:
→ 1) Häufig weisen Patienten mit eosinophiler Ösophagitis eine allergische Diathese (50-70%) mit allergischer Rhinitis, Asthma, atopischer Dermatitis auf. Bei allen vorher genannten Erkrankungen spielen insbesondere Entzündungsmediatoren wie Eotaxin 3, Interleukin 5 und 13 sowie TNF-Alpha eine wichtige Rolle.
→ 2) Häufig zeigen Patienten mit EoE eine IgE-vermittelte Nahrungsmittelallergie, sodass die eosinophile Ösophagitis als spezielle Form der nicht-IgE-vermittelten Nahrungsmittelallergie angesehen werden kann.
→ IV: Bleibt die EoE unbehandelt, persistiert zumeist die chronische Entzündung und es kommt im weiteren Krankheitsverlauf zur Fibrosierung des Ösophagus mit konsekutiver Stenosierung und Strikur-Bildung (Bolusobstruktion).
→ Klinik: → I: Charakteristisch jedoch nicht obligat sind dysphagische Beschwerden für feste Nahrung, die nicht selten zu einer Bolusobstruktion führen (> 30% der Fälle).
→ II: Oft sind die Patienten an ihre Symptome adaptiert und essen, langsamer, kauen gründlicher, meiden trockene Speisen, um die Nahrungspassage zu erleichtern.
→ III: Auch können refluxähnliche Beschwerden wie retrosternale Schmerzen und Sodbrennen, die von der GERD abgegrenzt werden müssen, auftreten.
→ Klinisch-relevant: Besonders bei der eosinophilen Ösophagitis spricht bei einem Großteil der Patienten die Applikation von Protonenpumpen-Inhibitoren nicht auf Sodbrennen an.
→ IV: Bei Kindern manifestieren sich zumeist unspezifische Symptome wie Nahrungsverweigerung, abdominale Schmerzen, Übelkeit, Erbrechen und nicht zuletzt Gedeihstörungen.
→ Diagnose: Die Diagnose erfolgt ausschließlich durch das Zusammenspiel von klinischer Symptomatik, Endoskopie und Histologie.
→ I: Makroskopie: Mittel der Wahl und Goldstandard in der Diagnostik der EoE ist die Ösophagogastroduodenoskopie mit konsekutiver Probeentnahme (Stufenbiopsie des gesamten Ösophagus mit mindestens 6 Biopsien, möglichst gezielt aus sichtbaren Läsionen).
→ 1) Makroskopisch zeigen sich primär longitudinal verlaufende Furchen und Rillen sowie weißes Exsudat und eine ödematöse Mukosa. Im weiteren Verlauf bilden sich ringförmige Einschnürungen mit Trachealisierung des Ösophagus (Baumring-Aspekt) und Strikturen als Ausdruck fibrotischer Umbauprozesse aus.
→ 2) Im Spätsadium ist die Ösophagusschleimhaut sehr fragil und leicht blutend und wird als „ Krepppapier-Mukosa“ bezeichnet.
→ 3) Die makroskopischen Veränderungen sind charakteristisch, können in beliebiger Kombination auftreten oder gänzlich fehlen, sodass eine endoskopische Diagnose nicht immer sicher gestellt werden kann (Histologie).
→ II: Mikroskopie: Histopathologisch zeigen sich charakteristischerweise vermehrte Infiltrate mit eosinophilen Granulozyten mit einer Dichte von > 15 pro Hauptgesichtsfeld (HPF), Mikroabszesse (= oberflächliche Ansammlungen von eosinophilen Granulozyten) und eine Basalzonenhypertrophie.
→ III: Labor: Hat keine große Bedeutung; nicht selten zeigt sich eine leichte Eosinophilie im Differenzialblutbild (50% der Erwachsenen) und bei bis zu 70% der Betroffenen ein erhöhtes Serum IgE.
→ Differenzialdiagnose: Von der eosinophilen Ösophagitis müssen insbesondere nachfolgende Erkrankungen abgegrenzt werden:
→ I: Gastroösophageale Refluxkrankheit, aber auch Achalasie, diffuser Ösophagusspasmus und das Ösophaguskarzinom.
→ II: Angina pectoris und der Myokardinfarkt.
→ Therapie: In der Behandlung der eosinophilen Ösophagitis sind nachfolgende Therapieziele von besonderer Bedeutung:
→ I: Mittel der ersten Wahl ist die Behandlung mit topischen Kortikosteroiden.
→ 1) Hierfür existiert seit 2018 eine orodispersible Applikationsform von Budenosid als 1 mg Schmelztabletten.
→ 2) Diese wird nach den Mahlzeiten morgens und abends ohne Flüssigkeit für 2 min bis zur Auflösung zwischen Zunge und Gaumen gehalten und geschluckt; für 30 min darf anschließend nicht gegessen und getrunken werden.
→ 3) Die Therapiedauer sollte mindestens 6-12 Wochen betragen, wobei es nach 6 Wochen in > 90% zur histologischen Remissionsrate und nach 12 Wochen kumulativ in > 85% zur histologischen und klinischen Remission kommt.
→ 4) Eine Dauertherapie mit Budenosid ist möglich, jedoch kann sich eine Candidiasis des Ösophagus manifestieren.
→ II: In der Behandlung mit PPI weist nur bei einem geringen Anteil der Patienten mit eosinophiler Ösophagitis eine klinischen und histologischen Remission auf (in manchen Fällen ist eine initiale PPI-Therapie zur differenzialdiagnostischen Unterscheidung zur GERD möglich).
→ III: 6-Food-Eliminationsdiät: (SFED) Hierbei wird innerhalb von 6 Wochen durch Verzicht auf Weizen, Kuhmilch, Eier, Meeresfrüchte, Nüsse und Soja in 70% der Fälle eine Remission erreicht. Anschließend erfolgt eine gezielte Exposition, um den Trigger zu identifizieren, der von dem Zeitpunkt gemieden werden sollte. Häufigste Trigger sind Weizen und Kuhmilch.
→ IV: Des Weiteren existiert eine Phase-3-Studie, bei der der monoklonale Antikörper Dupilumab (anti IL4/IL13) eine hohe Wirksamkeit in Bezug auf Symptome, Endoskopie und Histologie von Patienten mit EoE aufweist.
→ V: Die endoskopische Dilatationstherapie ist ausschließlich bei symptmatischer narbiger Stenosierung indiziert. Trotz z.T. sehr langstreckiger Stenosen ist die Perforationsgefahr bei Bougierung der EoE im Vergleich zu anderen Indikationen relativ gering.
→ Prognose: Die eosinophile Ösophagitis ist mit derzeitigen Therapieoptionen nicht heilbar.
→ I: So ist die Rezidivrate insgesamt sehr hoch, beträgt bei der topischen Steroid-Behandlung ca. 50% und bei der 6-Food-Eliminationsdiät sogar 100% im ersten Jahr.
→ II: In der Mehrzahl der Fälle kann jedoch langfristig eine symptomatische Linderung erreicht werden.