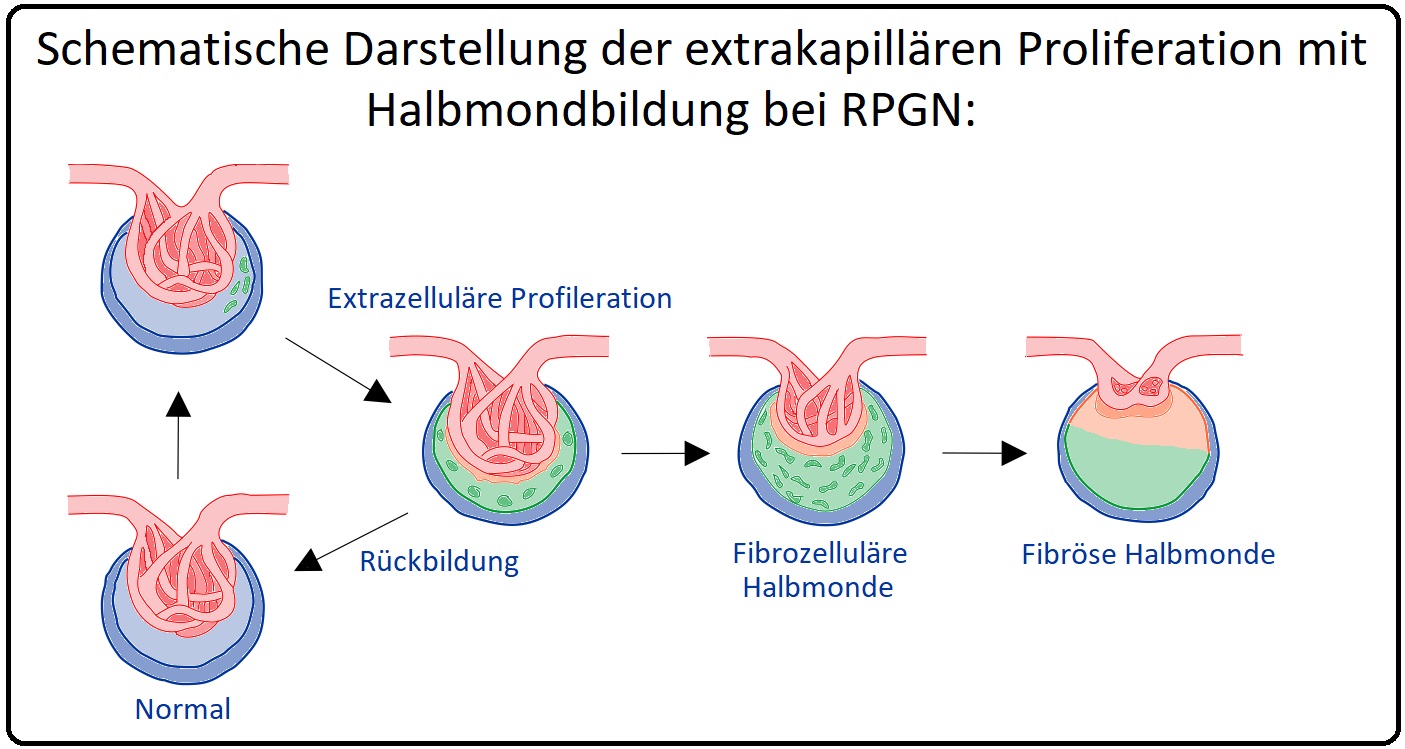
→ Definition: Bei der rapid progressiven GN handelt es sich um eine seltene Glomerulonephritis mit raschem Abfall der Nierenfunktion im Sinne eines intrarenalen akuten Nierenversagens (Übergang in eine terminale Niereninsuffizienz innerhalb von Wochen bis Monaten. Charakteristikum ist der Nachweis einer extrakapillären Proliferation (Halbmonde) im Lichtmikroskop (Abb.: Schematische Darstellung der Rapid-progressiven GN).
→ Epidemiologie:
→ I: Die Inzidenz liegt bei 1/100000 und kann in jedem Lebensalter auftreten.
→ II: Generell kann sie sich aus jeder proliferativen GN oder Vaskulitis (Wegener Granulomatose) entwickeln.
→ III: Die häufigste Form der rapid-progressiven GN ist diejenige mit Nachweis von antineutrophilen Ak (mit ca. 80% der Fälle) gefolgt von derjenigen mit Ak gegen die glomeruläre Basalmembran (ca. 15%). Schlusslicht bildet die Gruppe mit Ablagerung von Immunkomplexen.
→ Pathogenese: Bei der Entstehung der RPGN hat die Entwicklung der glomerulären, extrakapillären Halbmonde eine wichtige Bedeutung. Hierbei kommt es zur Proliferation und Migration von Podozyten, Makrophagen und T-Lymphozyten, die zur Zerstörung der Schrankenfunktion der Glomeruli führen.
→ Klassifikation:
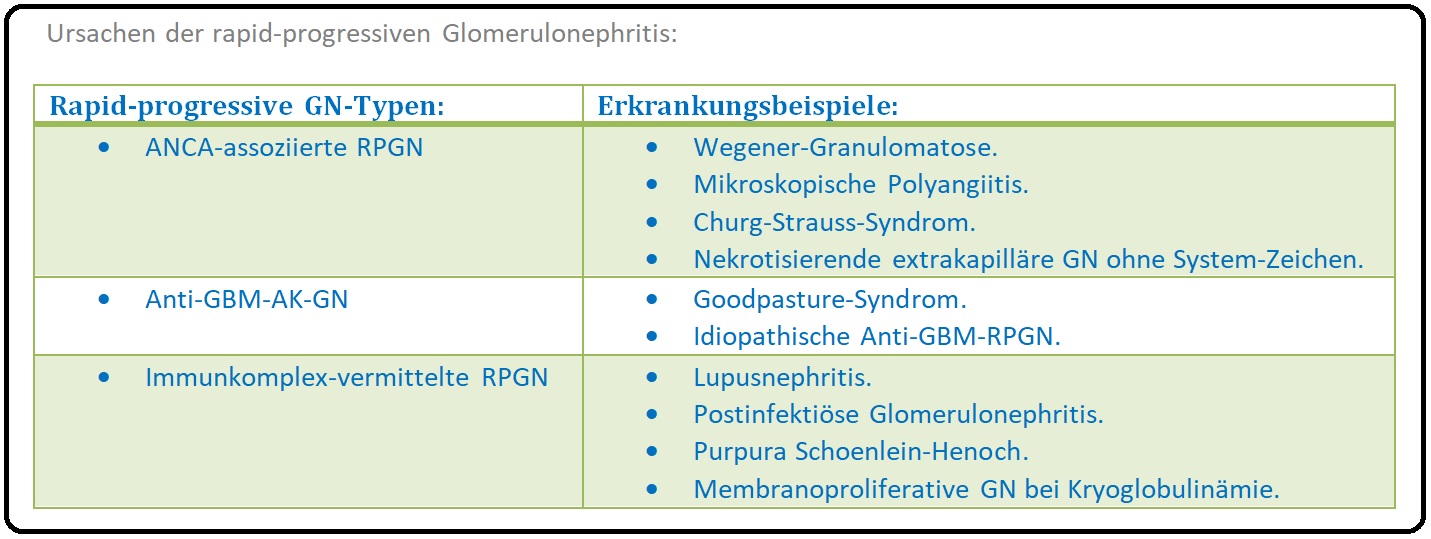
→ I: Typ 1: (= Antibasalmembran-RPGN) Stellt eine seltene Form dar; Charakteristsisch ist der Nachweis von Antikörpern (IgG und C-3), sogenannten GBM-Antikörper, gegen die glomeruläre Basalmembran, die sich linear an sie anlagern. Nicht selten manfestiert sich eine gleichzeitige Lungenbeteiligung mit konsekutiven Lungenblutungen (z.B. klinisch Hämoptysen), da eine Antigenverwandtschaft zwischen glomerulärer und bronchialer Basalmembran (Kollagen IV) besteht. Bei Lungenbeteiligung spricht man von dem Goodpasture-Syndrom, das insbesondere bei jungen Männern um das 40. Lebensjahr auftritt. (Weisen die Patienten einen positiven ANCA-Test auf, ist dies prognostisch günstig).
→ II: Typ 2: (= Immunkomplex-RPGN) Bei der häufiger auftretenden Typ 2 Form der RPGN kommt es zur glandulären Ablagerung von Immunkomplexen (sogenannten humps) entlang der glomerulären Basalmembran. Folge ist eine proliferative glomeruläre Halbmondbildung. Sie tritt häufig para- und postinfektiös (insbesondere postinfektiöse Glomerulonephritis), bei systemischen Lupus erythematodes (Anti-DNS-Ak) und der Schönlein-Henoch-Nephritis, aber auch im Rahmen von weiteren primären Glumerulonephritiden wie IgA-GN oder mebranoproliferative GN auf.
→ III: Typ 3: (= ANCA-assoziierte Vaskulitiden) (70-80%) Hier fehlen Ablagerungen von Immunglobulinen und Komplement (= pauci-immun). Man findet sie gerade bei den renalen Verlaufsformen der ANCA-assoziierten-Vaskulitiden, wie:
→ 1) Mikroskopische Polyangiitis mit pANCA. Das Zielantigen ist die hierbei die Myeloperoxidase.
→ 2) Wegener-Granulomatose: Mit cANCA. Das Zielantigen ist die Proteinase 3 (= Anti-Proteinase-3-AK).
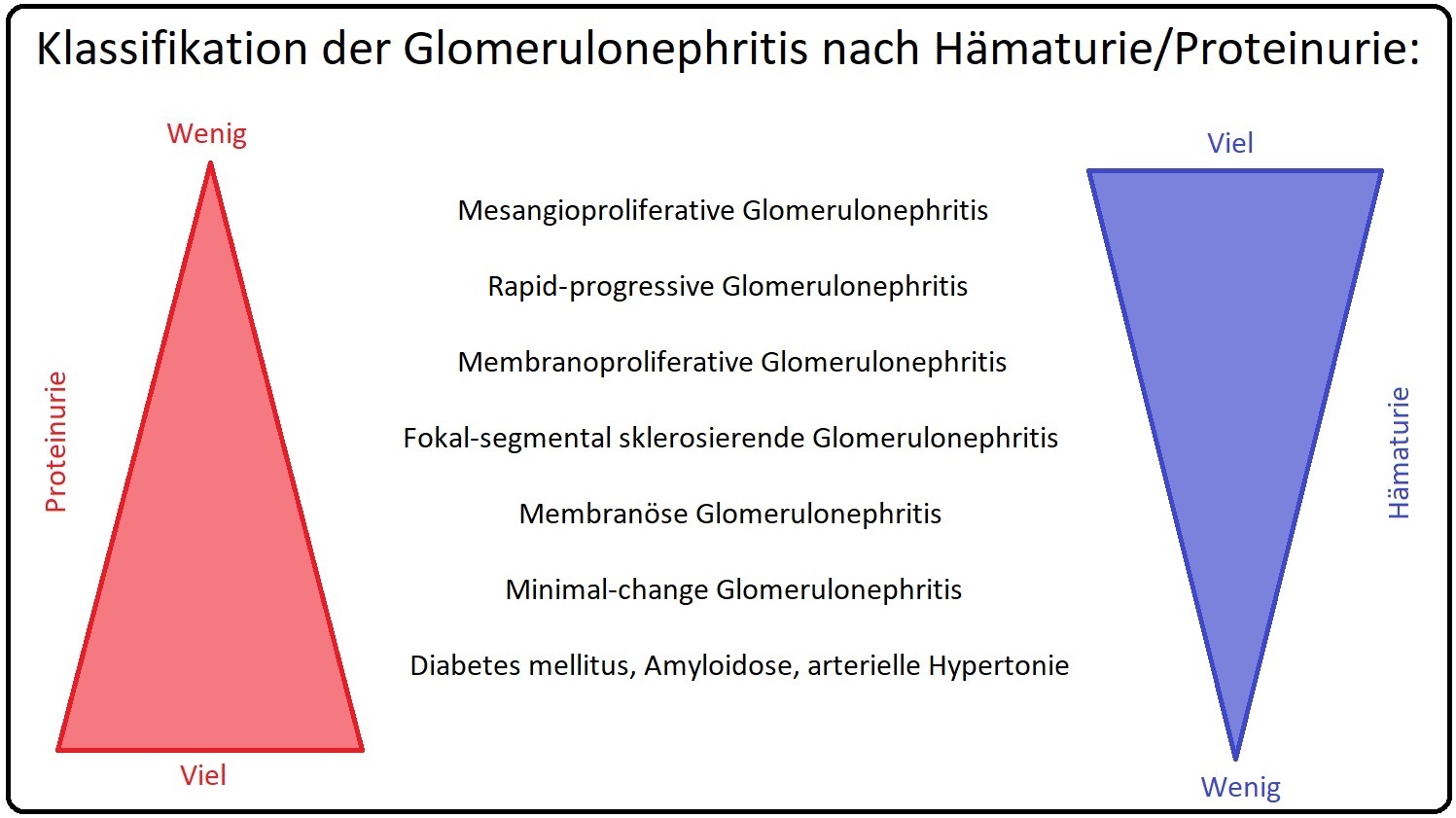
→ Klinik: Leitsymptome der rapid-progressiven-Glomerulonephritis sind insbesondere rascher Abfall der GFR, glomeruläre Hämaturie, nephritisches Sediment und variabel Proteinurie (zumeist < 3,5g/24h)
→ I: Leistungsminderung, Schwäche, evtl. Übelkeit, (klassische Zeichen einer Urämie).
→ II: Nephritisches Syndrom mit gering ausgeprägter Proteinurie und leichten Ödemen und Mikrohämaturie.
→ III: Arterielle Hypertonie und ein sich rasch entwickelnder Nierenfunktionsverlust mit konsekutiver Niereninsuffizienz binnen Tagen bis Wochen.
→ IV: Lungenblutungen manifestieren sich beim Goodpasture Syndrom.
→ Diagnose:
→ I: Labor:
→ 1) BSG und CRP Erhöhung.
→ 2) Rascher Anstieg der Rentensionswerte Kreatinin und Harnstoff.
→ 3) 24h-Sammelurin: Nachweis einer unselektiven, hochmolekularen Proteinurie.
→ Klinisch-relevant:
→ A) Typ 1: Serologischer Nachweis von Anti-GBM-Ak.
→ B) Typ 2: Serologischer Nachweis von Immunkomplexen.
→ C) Typ 3: Nachweis von pANCA und cANCA.
→ II: Sonographie: Zunehmende Niereninsuffizienz bei normal großen Nieren.
→ III: Nierenbiopsie: Histologisch zeigt sich eine extrakapilläre Proliferation mit Halbmondbildung (unterschiedlich alte Läsionen als Zeichen eines schubartigen Verlaufes) um die glomerulären Kapillaren, aber auch eine fokal-segmental nekrotisierende Entzündung der Kapillarschlingen. Die Halbmonde stellen das histologische Korrelat einer massiven Proliferation der Bowman-Kapsel dar.
→ Differenzialdiagnose: Insbesondere muss das akute Nierenversagen von der rapid-progressiven GN abgegrenzt werden.
→ Therapie: Die rapid-progressive Glomerulonephritis stellt immer eine nephrologische Notfallsituation dar. Um eine terminale Niereninsuffizienz zu vermeiden, ist eine frühzeitige und adäquate Behandlung obligat (eine rechtzeitige Behandlung kann zur Heilung führen).
→ I: Typ 1:
→ 1) Kortikoid-Cyclophosphamid Stoßtherapie über 3 Tage, initial 1g/d Methyl-Prednisolon intravenös (danach langsame Dosisreduktion über 3-4 Monate) und Cyclophosphamid 1-4mg/kgKG/d oral.
→ 2) Plasmapherese über 2-3 Wochen 1/d. Die Therapiedauer beträgt zumeist 6-9 bis maximal 12 Monate.
→ II: Typ 2: Initiale 3 tägige Stoßtherapie mit einem Kortikosteroid (1g/d i.v.) + Cyclophosphamid. Wiederholungen jeweils nach 4 Wochen über ein Therapie-Intervall von 6 Monaten. Eine Plasmapherese erfolgt hier nicht.
→ III: Typ 3: Eine Kombinationstherapie, bestehend aus einem Kortikosteroid und Methotrexat bei leichteren Formen, bei schwereren eine Kombination aus einem Kortikosteroid und Cyclophosphamid. Bei einem Serumkreatinin von > 6mg/dl ist eine zusätzliche Plasmapherese indiziert.
→ IV: Bei akutem Nierenversagen symptomatische Therapie, evtl. Dialyse, ultima ratio ist die Nierentransplantation.
→ Prognose:
→ I: Unbehandelt ist die Prognose ungünsitig insbesondere bei Patienten des Goodpasture-Syndroms und es bildet sich innerhalb von Monaten eine terminale Niereninsuffizienz aus.
→ II: Ein frühzeitiger Therapiebeginn (Kreatinin < 6mg/dl) führt häufig zur Besserung der Nierenfunktion.
→ III: Die Antibasalmembran-RPGN ist selbstlimitierend und rezidiviert nicht.
→ IV: Bei Typ II/III manifestieren sich häufiger Rezidive.