→ Definition:
→ I: Das abdominelle Kompartmentsyndom ist durch eine langanhaltende intraabdominelle Druckerhöhung (= IAP) von > 20mmHg, einen abdominellen Perfusionsdruck (= AAP) < 60mmHg und eine neu auftretende Organdysfunktion (hohe Atemwegsdrücke, Anurie, niedriges Herzzeitvolumen) definiert.
→ II: Der physiologische abdominelle Druck liegt bei etwa 5mmHg.
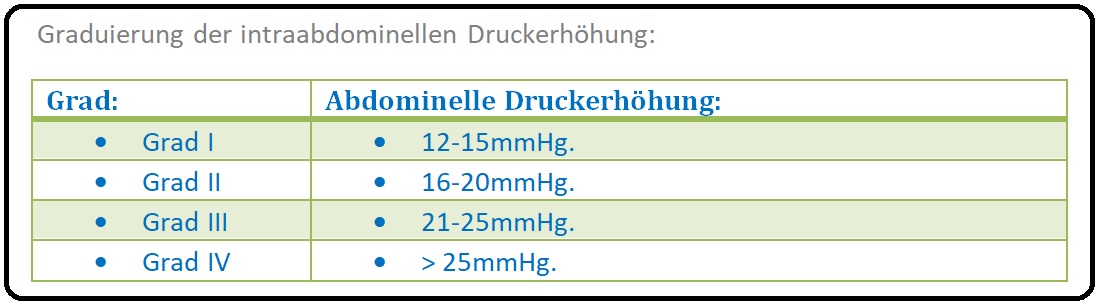
→ III: Intraabdominelle Hypertension: Sie stellt eine kurzfristige abdominelle Druckerhöhung dar und wird in 4 Grade abgestuft:
→ Ätiologie: Die Ursachen des intraabdominellen Kompartmentsyndroms sind vielfältig und es werden hinsichtlich des Entstehungsmechanismus zwischen einem:
→ I: Primären intraabdominellen Kompartment-,
→ II: Sekundären extraabdominellen – und
→ III: Einem tertiären chronischen Kompartmentsyndrom unterschieden.
→ I: Primäres intraabdominelles Kompartmentsyndrom: Ursachen hierfür sind u.a.: Stumpfes, penetrierendes Traumata, Beckentrauma, ruptiertes Bauchaortenaneurysma, Tumoren, Pankreatitis, Aszites oder Peritonitis.
→ II: Sekundäres Kompartmentsyndrom: Extraabdominelle Ursachen die ein Kompartment durch Volumenverschiebung triggern sind z.B.: Massentransfusionen, Verbrennungen oder Sepsis.
→ III: Tertiäres Kompartmentsyndrom: Chronisch nach Bauchdeckenverschluss oder mögliche Entwicklung aus einer primären oder sekundären Form.
→ IV: Weitere Risikofaktoren sind:
→ Pathogenese: Im Mittelpunkt der Entstehung steht die Abnahme des venösen Abflusses. Im weiteren Krankheitsverlauf tritt dann auch eine Abnahme der arteriellen Perfusion mit konsekutiver Dysfunktion intraabdomineller/ später extraabdomineller Organe auf.
→ Klinik:
→ I: Charakteristische klinische Symptome des intraabdominellen Kompartmentsyndroms sind:
→ 1) Zunahme des Bauchumfangs aufgrund eines distendierten Abdomens.
→ 2) Kardiales Low-output-Syndrom mit Hypotonie und Tachykardie.
→ 3) Anstieg des Blasendrucks; in der Spätphase entwickeln sich typischerweise Oligurie und Anurie.
→ 5) Weitere häufig auftretende Symptome sind Darmatonie und respiratorische Insuffizienz
→ II: Zudem entwickeln klinische Folgen aufgrund einer Minderperfusion aller Organsysteme:
→ 1) Kardiovaskuläre Folgen: Der erhöhte intraabdominelle – führt zu einem intrathorakalen Druckanstieg mit deutlicher Verschlechterung des Herzminutenvolumens und der hämodynamischen Stabilität. Bei der intraabdominellen Hypertension wird dieser Mechanismus durch die Erhöhung des peripheren Widerstandes kompensiert.
→ 2) Pulmonale Folgen: Folgen des erhöhten intrathorakalen Druckes sind:
→ A) Zwerchfellhochstand mit Minderbelüftung der basalen Lungenabschnitte mit konsekutive Abnahme des funktionalen Residualvolumens.
→ B) Hyperkapnie und Hypoxie sowie
→ C) Steigerung der Atelektase-Bildung.
→ 3) Hepatische Folgen: Die intraabdominelle Druckerhöhung führt sowohl zu einer arteriellen Minderperfusion der Leber, als auch zu einer Verminderung des portalen Blutflusses. Eine Folge ist z.B. das vermehrte Auftreten von Komplikationen wie Varizenblutungen bei Patienten mit Leberzirrhose.
→ 4) Intestinale: Der Darm reagiert am empfindlichsten auf die intraabdominelle Druckerhöhung infolge einer verminderten mesenterialen Perfusion. Begünstigt hierdurch werden u.a.:
→ A) Bakterielle Translokaltion,
→ B) Entwicklung einer Azidose,
→ C) Freisetzung toxischer Metaboliten und proinflammatorischer Zytokinen wie IL-1, IL-6, IL-8 und TNF-Alpha.
→ D) Darmdilatation sowie die Steigerung der Darmpermeabilität.
→ 5) Renale: Im Rahmen des Kompartmentsyndroms kann sich auch eine renale Minderperfusion mit Abnahme der glomerulären Filtrationsrate entwickeln. Hierbei spielen weitere Faktoren eine bedeutende Rolle:
→ A) Erhöhung des Venendrucks mit konsekutiver Aktivierung des Renin-Angiotensin-Aldosteron-Systems.
→ B) Erhöhung des Sympathikotonus,
→ C) Nichtosmotische ADH-Sekretion.
→ D) Kompression der Niere mit Steigerung des Gefäßwiderstandes und der Ureteren.
→ 6) Neurologische: Auch hier kann es zur Steigerung des intrazerebralen Drucks mit konsekutiver Minderperfusion aufgrund eines erhöhten Gefäßwiderstandes kommen.
→ Komplikationen: Bei ausbleibender Intervention manifestiert sich häufig ein Multiorganversagen mit letalem Ausgang.
→ Diagnose:
→ I: Anamnese: Erhebung der Risikofaktoren und der klinischen Symptomatik.
→ II: Klinische Untersuchung: Der Goldstandard zur Quantifizierung des intraabdominellen Druckes ist die Bestimmung des Blasendrucks. Hierbei wird die Blase nach vollständiger Entleerung mit 50ml isotoner Na+Cl--Lösung gefüllt und mittels transurethraler Messung (= Blasenkatheter) bestimmt. Der Blasendruck korreliert direkt mit dem intraabdominellen Druck (bei intensivmedizinischen Patienten mit Risiko für ein abominelles Kompartmentsyndrom ist eine regelmäßige Messung alle 4-6 Stunden indiziert).
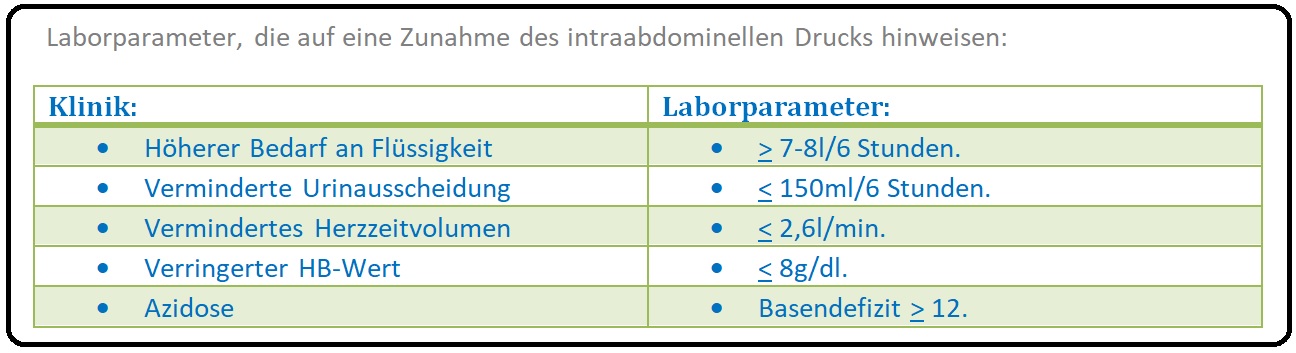
→ III: Weitere Faktoren, die auf eine Zunahme des intraabdominellen Druck hinweisen können:
→ Therapie: Von großer Bedeutung in der Behandlung des abdominellen Kompartmentsyndroms ist die laparotomische Dekompression bevor irreversible strukturelle Organschäden auftreten. Klassische Indikationen sind intraabdominelle Drucksteigerung und die Progredienz des Organversagens.
→ I: Allgemeinmaßnahmen:
→ 1) Stabilisierung des Kreislaufs durch Volumen- und Katecholaminsubstitution.
→ 2) Bei Ateminsuffizienz sollte eine Beatmung (BIPAP) erfolgen.
→ 3) Bei bestehendem Ileus können entlastende Maßnahmen wie die Anlage einer nasogastralen Sonde zur Verhinderung einer Aspiration, aber auch Prokinetika eingeleitet werden.
→ 4) Bei Patienten mit ausgeprägten Aszites ist eine Parazentese, bei intrabdominellen Abzessen die Anlage einer Drainage hilfreich.
→ II: Chirurgische Therapie:
→ 1) Häufig jedoch reichen konservative/interventionelle Therapiemaßnahmen nicht aus, sodass eine dekompressive Entlastungslaparatomie (IAP > 26mmHg) indiziert ist.
→ 2) Hierbei wird das Abdomen mittels medianer Laparatomie eröffnet und entweder als Laparostoma belassen (bis der Blasendruck < 10mmHg sinkt) oder mittels Vicrylnetz verschlossen.
→ 3) Zumeist wird ein sekundärer Bauchdeckenverschluss Faszienverschluss nach 6-8 Tagen angestrebt.
→ Klinisch-relevant: Eine sekundärer Bauchdeckenverschluss sollte erst bei einem Blasendruck < 10mmHg durchgeführt werden.
→ 4) Kann der Bauchdeckenverschluss jedoch nicht erfolgen, werden die Granulationsflächen mittels Spalthauttransplantaten gedeckt. Anschließend ist eine Rekonstruktion der Bauchwand in einem Zeitintervall von 6-8 Monaten nach Ausheilung indiziert.
→ 5) Alternativ kann nach der Entlastungslaparotomie eine abdominelle Vakuumtherapie (z.B. Vakuumverband) mit einem negativen Druck von 75-100mmHg versucht werden.