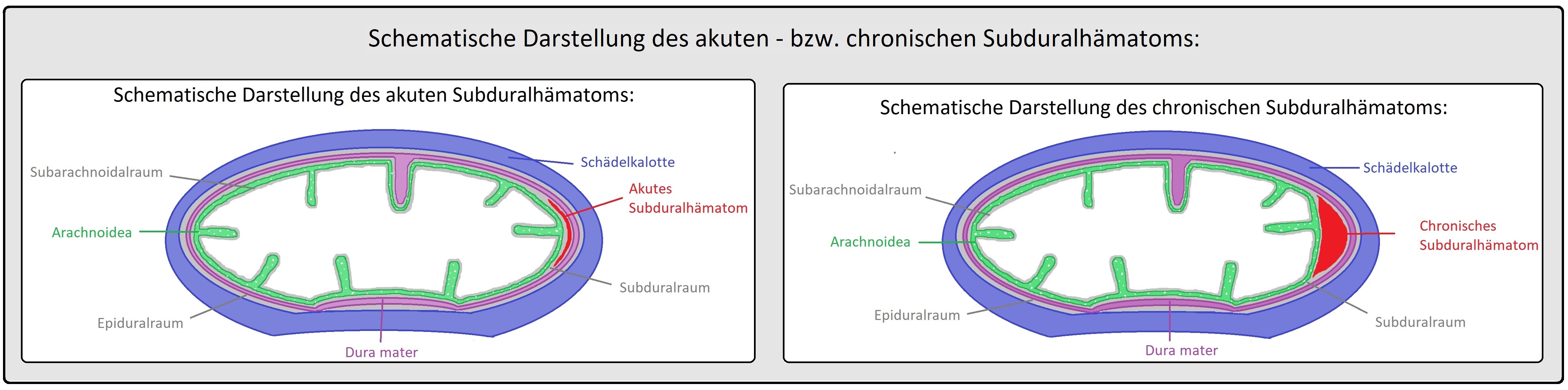
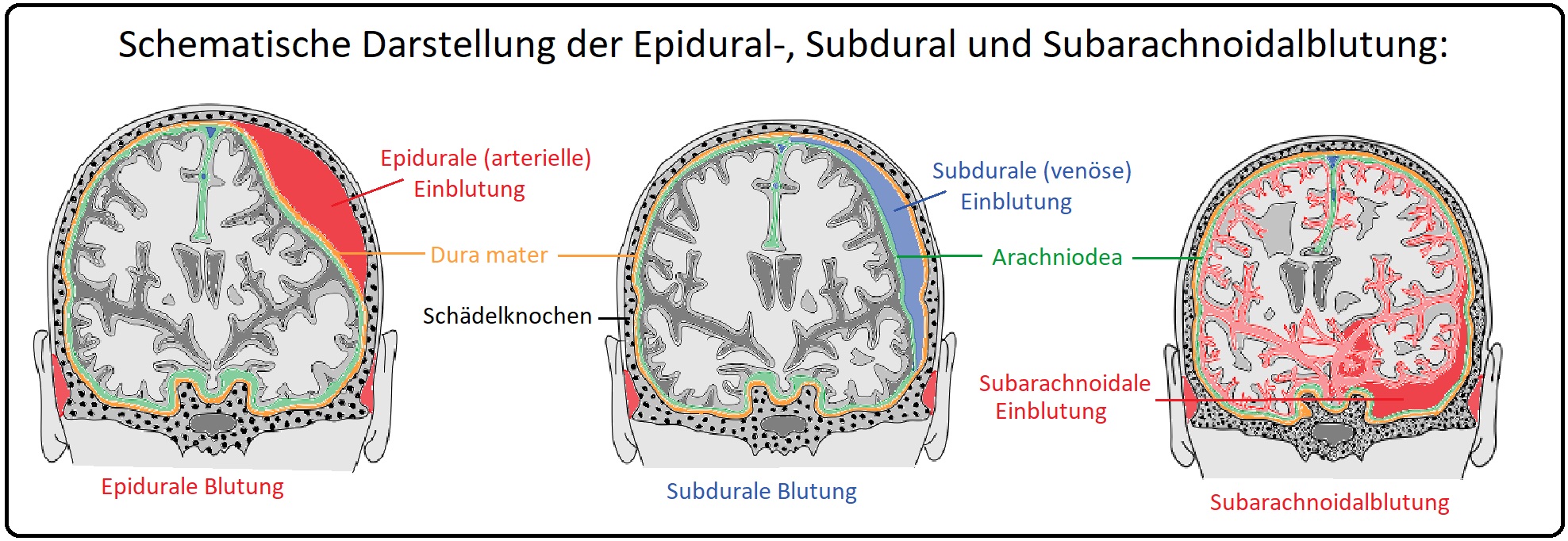
→ Definition: Beim Subduralhämatom (= SDH) handelt es sich um eine Blutung im Subduralraum zwischen Dura mater und Arachnoidea.
→ Epidemiologie:
→ I: Die Subduralhämatome haben eine Häufigkeit von 10-20% aller Patienten mit Schädel-Hirn-Trauma; nicht selten sind sie mit weiteren Hämatomformen (z.B. subarachnoidal und/oder intrazerebral) kombiniert.
→ II: In 95% der Fälle sind die SDH supratentoriell (insbesondere frontoparietal), in 15% beidseitig lokalisiert.
→ Klassifikation: Beim Subduralhämatom werden 2 Formen unterschieden:
→ I: Akutes SDH: Durch ein schweres SHT mit zumeist begleitender Parenchymverletzung hervorgerufen und ist überwiegend frontotemporal sowie parietal lokalisiert. Es tritt in direktem zeitlichem Zusammenhang mit dem Trauma auf (entwickelt sich innerhalb von 48 (-72 Stunden), meist in den ersten 8 Stunden).
→ II: Chronisches SDH: Oftmals im Rahmen eines Bagatelltraumas bei älteren Patienten, aber auch unter Antikoagulations- (z.B. Macumar) oder Streptokinasetherapie. Es ist insbesondere parietal (90% der Fälle), aber auch doppelseitig (10%) lokalisiert.
→ Ätiologie:
→ I: Akutes SDH:
→ 1) Traumatisch: Fast ausschließlich im Zusammenhang mit einem Schädel-Hirn-Trauma durch schwere Gewalteinwirkung mit Verletzung insbesondere der Brückenvenen (seltener Brückenarterien).
→ 2) Nicht-traumatisch: Seltene nicht-traumatische Ursachen sind z.B. Durafistel, Sinusvenenthrombose, Aneurysmablutung, myeloproliferative Erkrankungen, etc.
→ II: Chronisches SDH:
→ 1) Bagatelltrauma und Trauma, Gerinnungsstörungen, Einnahme von ASS und weiteren Antikoagulanzien, Alkoholabhängigkeit.
→ 2) Iatrogene Faktoren: Shunt-Überfunktion bei Normaldruckhydrozephalus, Liquordrainage etc.
→ 3) Disponierte Faktoren: Höheres Lebensalter, männliches Geschlecht, Hirnatrophie (durch Zug auf die Brückenvenen), Epilepsie, Stoffwechsel- und Gefäßerkrankungen etc.
→ Klinik:
→ I: Akutes SDH: Eine klinische Differenzierung zum Epiduralhämatom ist nicht möglich. Typische klinische Symptome sind u.a.:
→ 1) Innerhalb von Stunden kommt es zur protrahierte Bewusstseinseintrübung (zumeist keine Aufhellung nach dem Trauma).
→ 2) Ipsilaterale Pupillenerweiterung (50%) und Blickdeviation, sowie
→ 3) Kontralaterale Hemiparesen und epileptische Anfälle.
→ II: Chronisches SDH: Das klinische Bild des chronischen SDH ist vielgestaltig und entwickelt sich langsam progredient, sodass die Symptomatik ihre maximale klinische Ausprägung zumeist erst nach Monaten (2-3 Monaten) erreicht. Charakteristische Symptome hierbei sind:
→ 1) Zunehmende Kopfschmerzen, Schwindel und Bewusstseinsstörungen (zunächst wechselnde Bewusstseinsstörungen), selten Koma.
→ 2) Störungen des Antriebs mit psychomotorischer Verlangsamung, Lethagie, Apathie, aber auch Konzentrations- und Gedächtnisstörungen, Desorientierung und Verwirrtheitszustände (bis zur Demenz).
→ 3) Weitere Symptome sind u.a. homolaterale Mydriasis (kontralaterale) motorische Halbseitensymptomatik, fokale -, seltener generalisierte Anfälle (Epilepsie allgemein).
→ Diagnose:
→ I: Anamnese: Insbesondere beim chronischen SDH sollten Traumata, mögliche Vorerkrankungen, Medikamentenanamnese etc. erfolgen.
→ II: CCT:
→ 1) Akutes SDH: Konkave, sichelförmige, zumeist hyperdense, der Schädelkalotte anliegende Raumforderung (je nach Alter des Hämatoms hyper-, iso- oder hypodens von frisch nach alt). Mittellinienverlagerung, die bei beidseitigen Hämatomen fehlen kann sowie Liquorzirkulationsstörungen mit z.T. reduzierter Grau-Weiß-Differenzierbarkeit.
→ 2) Chronisches SDH: Bikonvexe oder plankonvexe hypo- oder isodense dem Hirn anliegende Raumforderung. Weitere radiologische Zeichen sind das Überschreiten der Suturgrenze sowie die Mittellinienverlagerung.
→ Klinisch-relevant: Subduralhämatome stellen sich im CT innerhalb der ersten Wochen nach dem Ereignis hyperdens, im subakuten Stadium isodens und im chronischen – (ca. nach 3-4 Wochen) hypodens dar.
→ III: MRT: Die MRT-Untersuchung ermöglicht neben der genaueren Darstellung des Hämatoms auch den Nachweis einer möglichen Hirnstammkontusion (prognostisch ungünstig).
→ IV: Labor: Mit Bestimmung von pTT, Quick und Gerinnngungsfaktoren zum Ausschluss einer Koagulopathie bzw. Kontrolle einer Antikoagulanzien-Therapie.
→ V: EEG: Typischerweise kommt es zur Amplitudenabnahme bzw. -abflachung über dem Hämatom.
→ Differenzialdiagnose: Von dem Subduralhämatom müssen vor allem nachfolgende Erkrankungen abgegrenzt werden:
→ I: Subdurales Hygrom: Stellt eine subdurale Flüssigkeitsansammlung nach traumatischer Verletzung der Arachnoidea dar.
→ II: Pachymeningeosis haemorrhagica interna ist das subdurale Hämatom bei Alkoholikern.
→ III: Epidurales Hämatom.
→ IV: Weitere Differenzialdiadiagnosen: Bezüglich des chronischen Subduralhämatoms (da die Symptomatik des chronischen SDH sehr vielgestaltig ist, gestaltet sich die Diagnosestellung in Einzelfällen als sehr schwer):
→ 1) Demenz insbesondere auch die Alzheimer-Krankheit (aber auch weitere Demenzformen); hierbei ist die Anamnese deutlich länger und es bestehen zumeist keine fokal neurologischen Symptome.
→ 2) TIA: Im Vordergrund steht der Zeitfaktor.
→ 3) Endogene Psychosen: Weist in der Vorgeschichte meist keine neurologischen Ausfälle auf.
→ 4) NPH: (=) Charakteristische Symptome sind u.a. kleinschrittiger Gang sowie Blasenstörungen.
→ Therapie:
→ I: Kleinere chronische SDH können primär unter radiologischer Kontrolle beobachtet werden (die Gabe von Dexamethason ist umstritten; angenommen wird, dass das Pharmakon die Ausbildung von Membranen an den Hämatomrändern hemmt). Sind die Betroffenen jedoch symptomatisch ist eine operative Intervention obligat.
→ II: Indikationen für eine Operation sind insbesondere:
→ 1) Jedes symptomatische Subduralhämatom.
→ 2) Ein Subduralhämatom mit einer Dicke > 10mm oder einer Mittellinienverlagerung von > 5mm unabhängig von der Vigilanz.
→ 3) Subduralhämatome mit einer Dicke < 10mm, Mittellinienverlagerung < 5mm, einem Glasgow-Coma Score < 9 und bei denen ein weiteres der nachfolgenden Kriterien erfüllt wird:
→ III: Operative Therapie:
→ 1) Kraniostomie: Hierbei erfolgt eine Stichinzision im Bereich der maximalen Hämatomausdehnung, anschließend wird die Schädelkalotte mittels Handbohrer eröffnet. Dura und parietale Hämatomkapsel werden mit einer Nadel penetriert und schließlich eine Kanüle zum Ablassen des Hämatoms eingeführt. Dieses Verfahren kann unter Lokalanästhesie durchgeführt werden.
→ 2) Bohrlochtrepanation: Erfolgt über der größten Hämatomausdehnung mit Ablassen der Flüssigkeit, Spülung und anschließender Anlage eines Drainageschlauchs nach außen. Häufigster Trepanationsort ist der Cushing-Kocher Punkt, der dicht vor oder auf der Kranznaht, ca. 3-4cm paramedian liegt.
→ 3) Insbesondere bei den akuten SDH ist zumeist eine notfallmäßige Kraniotomie mit Duraeröffnung und anschließender Entlastung indiziert.
→ III: Postoperativ:
→ 1) Eine postoperative Drainage sowie die „ Flach-Lagerung“ des Pattienten vermindert das Rezidivrisiko deutlich.
→ 2) CCT-Kontrolle direkt postoperativ und nach 2-4 Wochen im Rahmen einer Nachuntersuchung.
→ 3) Frühzeitige, postoperativ (noch am OP-Tag) Mobilisation zur Vermeidung von Komplikationen.
→ Prognose:
→ I: Die Prognose ist insbesondere vom Typus des SDH, der Ausdehnung und Lokalisation des Hämatoms sowie dem Grad der zerebralen Beeinträchtigung vor OP, etc. abhängig.
→ II: Insbesondere beim akuten SDH ist die Prognose meist schlecht; die Mortalität liegt bei bis zu 70% (-90%) der Fälle.
→ III: Bei der chronischen Form ist sie deutlich besser, in bis zu 90% kommt es trotz des hohen Alters zu einer (un-)vollständigen Erholung.