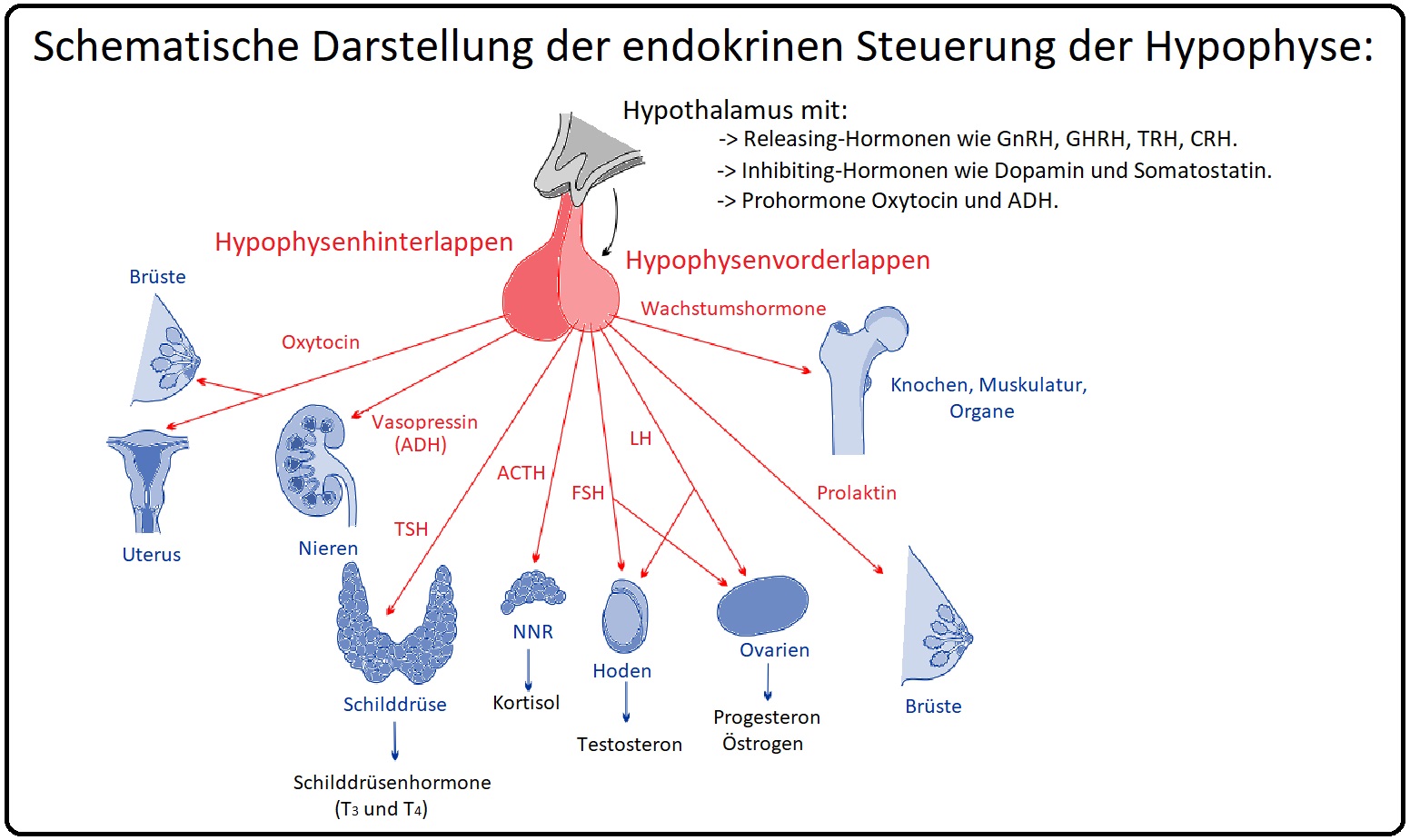
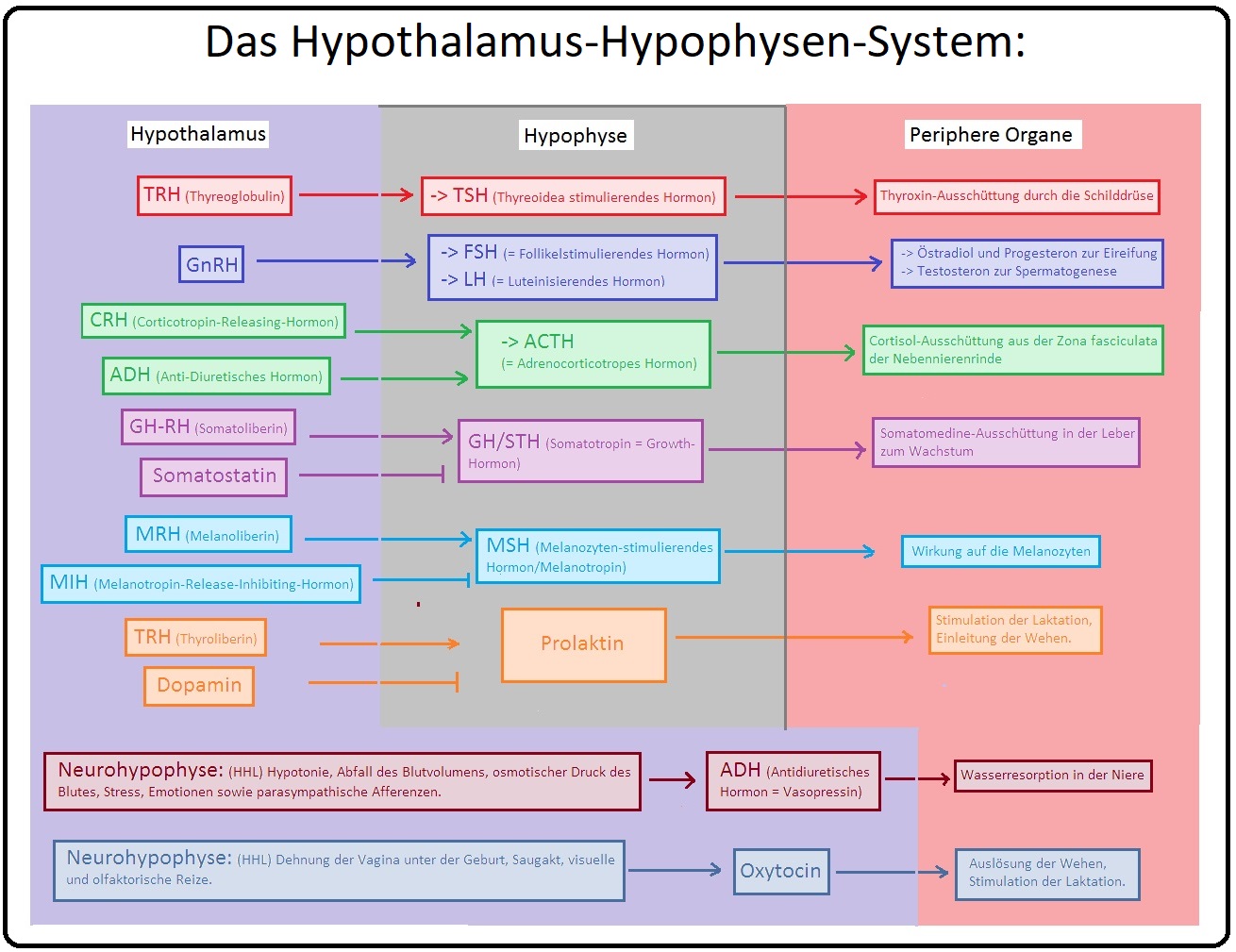
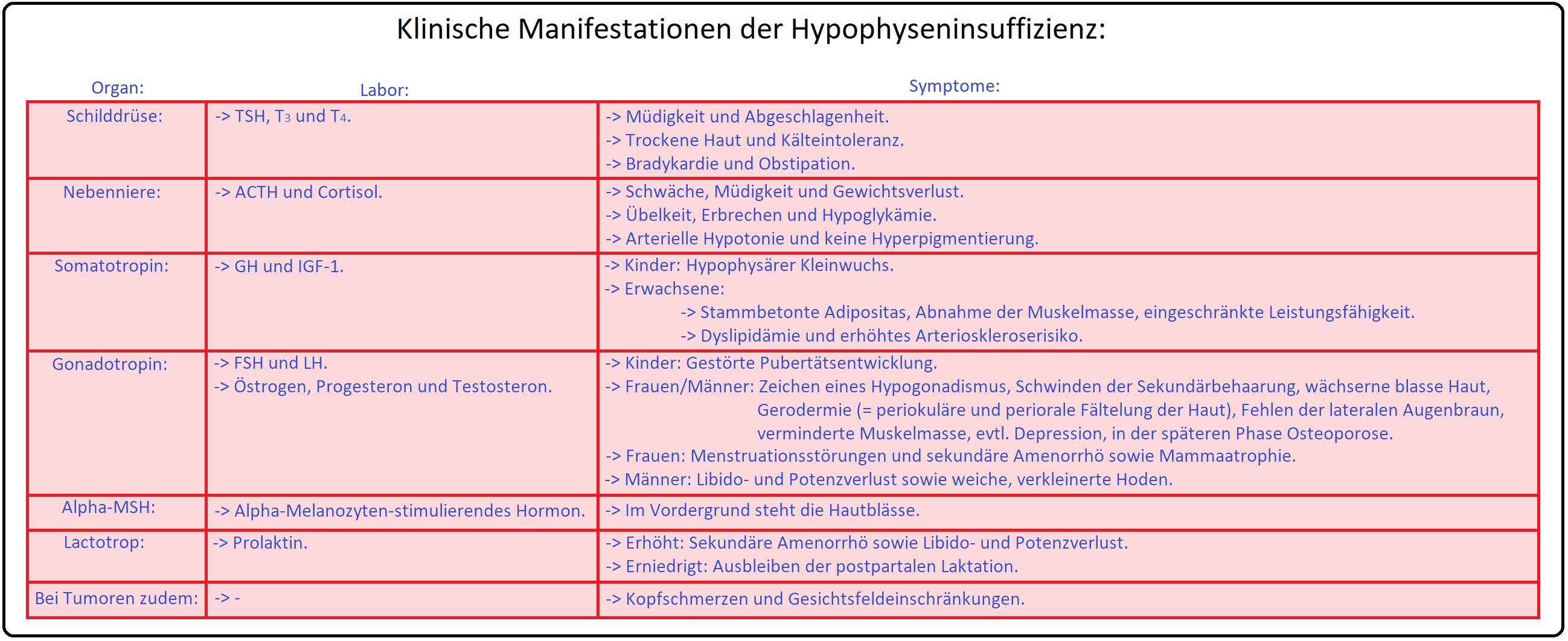
→ Definition: Bei der HVL-Insuffizienz handelt es sich um einen partiellen oder totalen Funktionsausfall der Hypophyse infolge einer verminderten bzw. fehlenden Sekretion adenotroper Hormone. Das Sheehan-Syndrom wiederum stellt eine postpartale Hypophysennekrose dar. Während der Schwangerschaft wächst die Hypophyse und reagiert empfindlich auf Hypoxie (Ursache hierfür sind insbesondere größerer Blutverlust und Thrombosebildungen).
→ Ätiologie: Ursachen für die Entstehung eines Hypopituitarismus sind u.a.:
→ I: Tumorös: Raumforderungen wie Hypophysenadenome, Kraniopharyngeome (benigner Tumor, der sich aus Restzellen der Rathke-Tasche entwickelt), Meningeome oder Metastasen.
→ II: Traumatisch: Traumen (z.B. Schädel-Hirn-Trauma) im Bereich der Hypophyse mit Einblutungen, Operationen, Bestrahlung.
→ III: Vaskulär: Wichtig zu erwähnen, ist das Sheehan-Syndrom, welches nur noch selten auftritt. Hierbei entwickelt sich eine Hypophysenvorderlappeninsuffizienz infolge eines ausgeprägten postpartalen Blutverlustes mit anschließender Nekrosebildung. Aber auch beim A. carotis Aneurysma und der Arteriitis temporalis (Horton)
→ IV: Entzündlich: Autoimmunhypophysitis (tritt charakteristischweise in der 2. Schwangerschaftshälfte auf mit lymphozytären Infiltrationen), granulomatöse Systemerkrankungen wie Sarkoidose, Wegener-Granulomatose und TBC.
→ V) Weitere Ursachen: Sind u.a. Amyloidose, Hämochromatose oder post chirurgisch.
→ Klassifikation:
→ I: Nach der Entstehung:
→ 1) Primäre HVL-Insuffizienz: Hierbei sind die Zellen der Hypophyse selbst betroffen.
→ 2) Sekundäre HVL-Insuffizienz: Durch Störungen bzw. Kompression des Hypothalamus oder des Hypophysenstiels.
→ II: Nach ihrem Funktionsausfall:
→ 1) Partielle HVL-Insuffizienz: Mit Störung der Sekretion einer oder mehrerer HVL-Hormone.
→ 2) Komplette HVL-Insuffizienz: Mit Beeinträchtigung aller Hypophysenvorderlappen-Hormone (GH, LH, FSH, TSH, ACTH, PRL); wird als Panhypopituitarismus bezeichnet.
→ Klinisch-relevant: Klinische Symptome manfestieren sich erst, wenn 80% des Hypophysenvorderlappens zerstört sind. Besteht der Übergang von einer partiellen in eine komplette HVL-Insuffizienz fallen die Hormone in folgender Reihenfolge aus; beginnend mit GH und Gonadotropin (FSH, LH) bis schließlich zum ACTH. Prolaktin fällt nur selten aus.
→ Klinik: Die klinische Symptomatik ist vor allem abhängig vom Ausfall des Hormons sowie vom Zeitpunkt (Alter: Präpubertät oder Postpubertät); Klinische Symptome treten erst und zumeist schleichend auf, wenn 80% des Hypophysenvorderlappens zerstört ist. Bei den Hypophysenadenomen manifestiert sich eine charakteristische Reihenfolge des Funktionsausfalls, beginnend mit GH über FSH bzw. LH und TSH zu ACTH.
→ I: Partieller Ausfall:
→ 1) STH-Ausfall: Manifestiert sich vor der Pubertät eine STH-Sekretionsstörung, entwickelt sich ein hypophysären Minderwuchs bei normalen Körperproportionen und Intelligenz. Im Erwachsenenalter bilden sich wie abdominelle Fetteinlagerung, erhöhtes Arteriosklerose-Risiko (LDL erhöht, HDL-erniedrigt) aus.
→ 2) TSH-Ausfall: Ausbildung einer sekundäre Hypothyreose mit u.a. trockener teigiger Haut, Kältemepfindlichkeit, psychomotorischer Verlangsamung und periorbitalem Ödme.
→ 3) ACTH-Ausfall: Manifestation einer sekundären Nebenniereninsuffizienz und konsekutiven klinischen Zeichen wie frühzeitige Ermüdbarkeit, Adynamie, Gewichtsverlust, Pigmentstörungen (wächserne Blässe) Hypotonie und Hypoglykämie.
→ 4) Gonadotropin-Ausfall: Präpubertär manifestiert sich eine ausbleibende Geschlechtsreife (= Eunuchoidismus = Kallman-Syndrom). Postpubertär sind klassisch klinische Symptome Zyklusstörungen, sekundäre Amenorrhö, Libido- und Potenzstörungen (= Hypogonadismus) sowie der Verlust der Achsel- und lateralen Augenbraunbehaarung.
→ Klinisch-relevant: Frühsymptome des Sheehan-Syndroms sind Agalaktie, Amenorrhö und Verlust der sekundäre Behaarung. Die Symptome können sich z.T. erst nach Jahren manifestieren.
→ II: Kompletter Ausfall: Hierbei sind charakteristische klinische Symptome des Hypopituitarismus Müdigkeit, Abgeschlagenheit, trockene kühle dünne Haut. Aufgrund des ACTH-Mangels zeigt sich eine alablasterfarbene Haut, Verlust der sekundären Schambehaarung, evtl. Ausbleiben der Bartbehaarung sowie das Auftreten einer Hypotonie und Hypoglykämie.
→ Klinisch-relevant: Beim Hypopituitarusmus treten die 7 As auf:
→ A) Gonadotropin-bedingt: Verlust der Achsel- und lateralen Augenbraunbehaarung (= Herthoge-Zeiche), Amenorrhö, Agalaktie.
→ B) TSH-bedingt: Apathie,
→ C) MSH-bedingt: Alablastärfarbene, blasse Haut.
→ D) ACTH-bedingt: Adynamie.
→ III: Weitere Symptome: Im Rahmen von Raumforderungen manifestieren sich im weiteren Krankheitsverlauf zudem ausgeprägte Kopfschmerzen und Gesichtsfeldausfälle, etc.
→ IV: Komplikation: Wichtigste und schwerwiegenste Komplikation ist das unter Stresssituationen (z.B. Infektionen, großer Operationen, etc.) sich entwickelnde hypophysäre Koma (durch Dekompensation einer chronischen HVL-Insuffizienz).
→ Diagnose: Bei Verdacht auf eine Hypophyseninsuffizienz bzw. einen Hormonmangel sollten diagnostisch (immer) sowohl die hypophysären als auch die peripheren Hormone (gleichzeitg) bestimmt werden.
→ I: Anamnese und klinische Untersuchung.
→ II: Labor: Mit insbesondere:
→ 1) Verminderung der peripheren Hormonkonzentrationen wie fT3, fT4, Cortisol, Östradiol und Testosteron.
→ 2) Erniedrigung der basalen Hypophysenhormonspiegel für FSH, LH, TSH und ACTH.
→ III: Endokrine-Stimulationstests: Bei Makroadenomen ist zu berücksichtigen, dass es durch einen Stimulationstest potenziell zu einem Hypophysenapoplex kommen kann.
→ 1) Somatotrope Funktion: Nach Applikation von GHRH oder im Insulin-Hypoglykämie-Test sind ein unzureichender Anstieg von IGF-1 und GH eruierbar.
→ 2) Gonadotrope Funktion: LH und FSH basal sowie Östradiol und Testosteron sind nach Gabe von LHRH erniedrigt.
→ 3) Thyreotrope Funktion: Nach Applikation von THR kommt es zum unzureichenden Anstieg von TSH sowie T3 und T4.
→ 4) Kortikotrope Funktion: ACTH und Cortisol basal sind erniedrigt und nach Gabe von CRH bzw. im Insulin-Hypoglykämie-Test zeigt sich ein zu geringer Anstieg der Hormone.
→ 5) Laktotrope Funktionsüberprüfung erfolgt durch Gabe von TRH, die beim Panhypopituitarismus durch einen zu niedrigen Prolaktinspiegel auffällt.
→ IV: Bildgebung mit CT und MRT zur Tumorsuche bzw Ausschluss.
→ Klinisch-relevant:
→ A) Bei hypothalamischen Prozessen ist Prolaktin aufgrund der Beeinträchtigung des Prolaktin-inhibitin-factor (= Dopamin) eher erhöht.
→ B) Ein normaler TSH-Wert schließt eine sekundäre Hypothyreose bzw. Störung der thyreotropen Funktion nicht aus, sodass bei Verdacht auf HVL-Insuffizienz auch immer die fT4-Konzentration mitbestimmt werden sollte.
→ Differenzialdiagnose: Von der Hypophysenvorderlappen-Insuffizienz müssen insbesondere nachfolgende Erkrankungen abgegrenzt werden:
→ I: Polyglanduläres Autoimmunsyndrom: Auch hier zeigen sich endokrine Funktionsverluste, jedoch sind zumeist die NNR (im Sinne einer Nebennierenrinden-Insuffizienz) oder die Schilddrüse (Hashimoto-Thyreoiditis) betroffen.
→ II: Essstörungen: Bei der Essstörung, Anorexia nervosa, bildet sich überwiegend auch ein Hypogonadismus aus, jedoch ohne Verlust der sekundären Behaarung.
→ Therapie:
→ I: Medikamentöse Therapie: Hier steht die Gabe der fehlenden adenotropen Hormone im Vordergrund:
→ 1) ACTH-Mangel: Applikation von Hydrocortisol 20-30mg/d, wobei 2/3 der Dosis morgens, der Rest über den Tag verteilt verabreicht wird (20-5-5mg). Insbesondere bei Infektionen und Operationen kann eine Erhöhung der Tagesdosis auf das 2-3-fache nötig sein. Müdigkeit, Appetitlosigkeit oder Übelkeit weisen auf eine Unterdosierung hin. Kontrollparameter sind u.a. das Befinden des Patienten, der Blutdruck und die Serum-Natriumkonzentration.
→ 2) GH-Mangel: Bei Auftreten eines Wachstumshormonmangels im Erwachsenenalter ist eine Hormonsubstitution nicht nötig. Bei Kindern sollte vor Epiphysenfugenschluss die Therapie beginnen. Es erfolgt die Applikation eines synthetisch-hergestellten humanen GH mit einer Initialdosis von 0,15-0,3mg/d bis zu einer Maximaldosis von 1mg/d. Kontrollparameter sind der IGF-1 Wert sowie das Befinden des Patienten. Zudem hat die Wachstumshormonsubstitution positive Auswirkungen auf Knochendichte, Muskelmasse und Muskelkraft.
→ 3) Gonadotroper-Mangel: Männern wird 250mg Testosteron intramuskulär alle 3-4 Wochen bzw. 1000mg alle 3 Monate verabreicht. Frauen wiederum wird ein Östrogen-Gestagen-Kombinationspräparat unter gynäkologischer Kontrolle verabreicht. Kontrollparameter sind für beide Geschlechter u.a. Serumtestosteron, sekundäre Geschlechtsmerkmale, Libido, Potenz, etc.
→ 4) TSH-Mangel: Applikationstherapie mit L-Thyroxin einschleichend mit einer Anfangsdosis von 50µg/d und schrittweisen Aufdosierung um 25-50µg/d (30min vor dem Frühstück). Die Zieldosis liegt zwischen 100-150µg/d. Kontrollparameter sind nicht das TSH, sondern vielmehr das fT4 sowie nach dem Befinden des Patienten.
→ Klinisch-relevant: Die mittlere Tagesdosis von Hydrocortison muss in Belastungssituationen deutlich erhöht (5-10-fache) werden, um die Entwicklung einer Addison-Krise zu vermeiden.
→ II: Operative Therapie: Bei Tumoren erfolgt eine operative Therapie oder evtl. Bestrahlung mit anschließender Hormonsubstitution.