→ Definition: Bei der exogen toxischen Myopathie handelt es sich um eine akute oder chronische Muskeldestruktion bzw. Schädigung der neuromuskulären Endplatte, die insbesondere durch eine Vielzahl von Medikamenten und Drogen induziert wird.
→ Epidemiologie: Absolute Zahlen existieren nicht, jedoch aufgrund der steigenden polypharmakologischen Behandlungen in den letzten Jahren nimmt die Häufigkeit toxischer Schädigung der Skelettmuskulatur zu.
→ Ätiopathogenese: Die zugrunde liegenden Pathomechanismen der exogen-toxische Myopathie sind bei vielen Substanzen bekannt, bei manch anderen werden sie noch diskutiert.
→ I: Eine Myopathie kann prinzipiell verursacht werden durch:
→ 1) Direkt toxische Wirkung auf den Muskel.
→ 2) Indirekte Wirkung auf den Muskel über metabolische, endokrine oder immunologische Mechanismen.
→ 3) Lokale Schädigungen durch z.B. intramuskuläre Injektionen und nicht zuletzt durch eine gestörte Muskelfunktion im Sinne eines myasthenen Syndroms durch Wirkung der Substanz an der mtorischen Endplatte.
→ II: Prädisponierende Faktoren: Für die Entwicklung einer exogen toxischen Muskelschädigung sind insbesondere:
→ 1) Höheres Lebensalter,
→ 2) Eingeschränkte Nierenfunktion (z.B. Niereninsuffizienz),
→ 3) Multimorbidität und die damit verbundene
→ 4) Vielfachmedikation.
→ III: Nicht-medikamentös induzierte exogen toxische Myopathien werden insbesondere durch Suchtmittel (z.B. Alkohol), Chemikalien und durch biologische Toxine hervorgerufen.
→ Klinisch-relevant: Wichtige Beispiele für die Auslösung dieser Myopathie sind u.a.:
→ A) Medikamente: Wie z.B. Glukokortikoide bzw. Kortikosteroide, Fibrate (Lipidsenker wie Bezafibrat), Statine insbesondere Cervistatin und Simvastatin, Lovastatin (sowie deren Kombination aus Fibraten und Statinen), Amphotericin, antivirale Substanzen (wie Zidovudin, Lamivudin), Amiodaron, Chloroquin, Ciclosporin, D-Penicillamin, Missbrauch von Schilddrüsenhormonen, Neuroleptika, Überdosierung von Vitamin A, etc.
→ B) Suchtmittel: Hierzu zählen insbesondere Alkohol (Alkoholabhängigkeit) Barbituratintoxikation, Kokain, Ecstasy, Phencyclidin, Heroin, etc.
→ C) Mechanisch: Im Koma oder bei langanhaltender tiefer Bewusstlosigkeit kann sich aufgrund von großen Traumen, Muskelanspannung, Druck von der Unterlage auf die Muskulatur, etc. eine Rhabdomyolyse entwickeln.
→ D) Sepsis (Critical-illness-Myopathie).
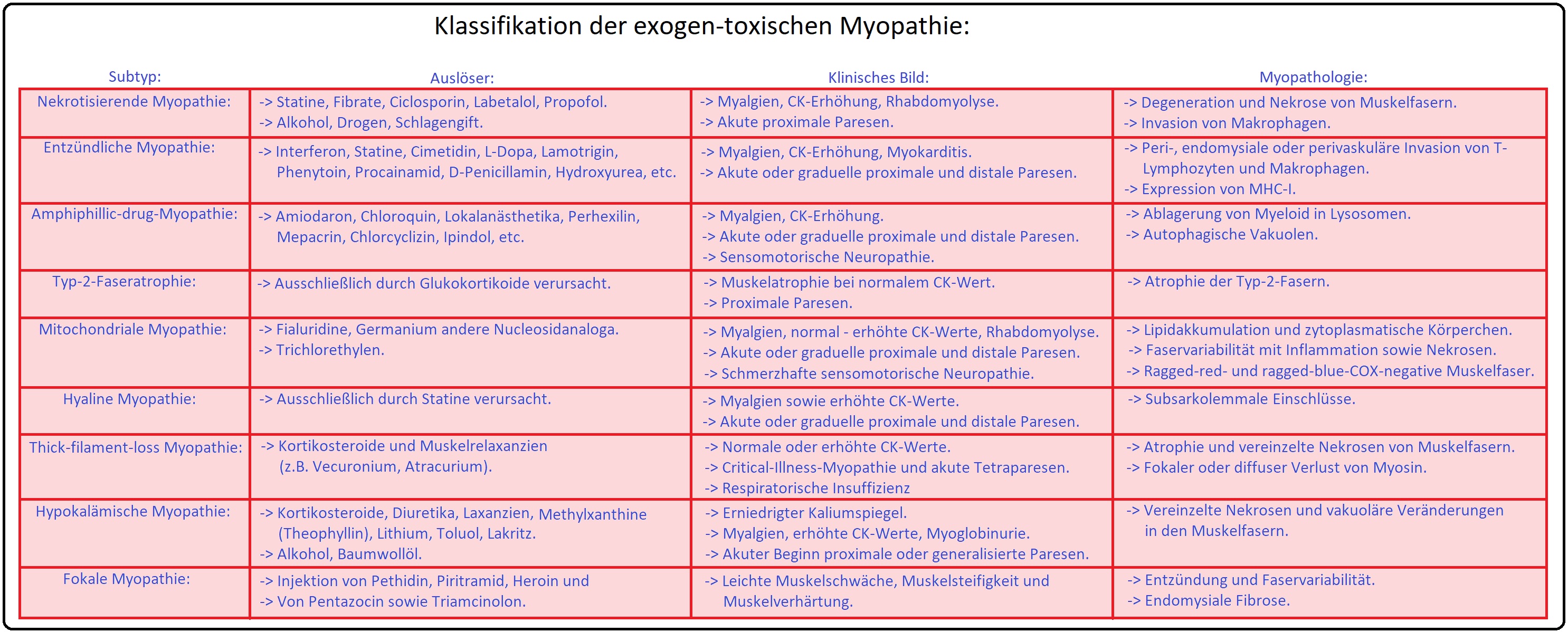
→ Klassifikation: Die exogen-toxischen Myopathien können nach klinischen und histologischen Kriterien sowie Substanzklassen und Pathomechanismus unterteilt werden:
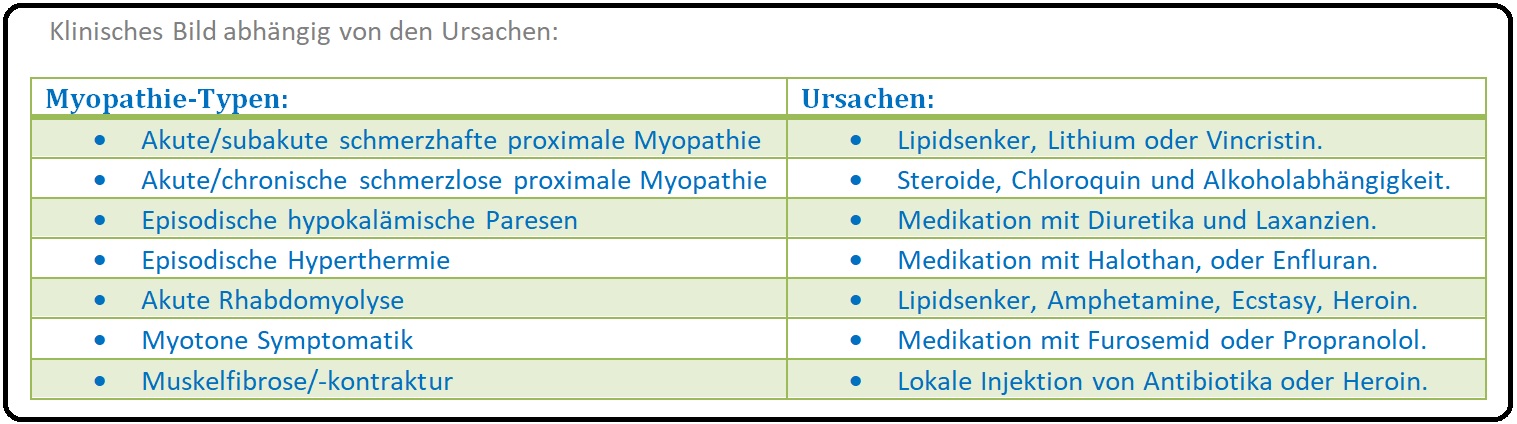
→ Klinik: Das klinische Bild der exogen-toxischen Myopathie ist vielfältig und z.T. unspezifisch.
→ I: Das klinische Bild reicht von Muskelschmerzen, Krampi (= Muskelkrämpfen) und myotonen Symptomen, über Muskelatrophie und -fibrose bis hin zu manifesten Paresen und Kontrakturen.
→ II: Komplikationen: Schwerwiegende und oft auch lebensbedrohliche Situationen sind insbesondere:
→ 1) Rhabdomyolyse und die
→ 2) Maligne Hyperthermie.
→ Diagnose:
→ I: Anamnese: Eigenanamnese inklusive der Medikamenteneinnahme und des Alkoholkonsums.
→ II: Klinische Untersuchung:
→ 1) Neurologischer Untersuchung mit druckdolente Muskulatur (insbesondere Wadenmuskulatur), proximal betonten Paresen, evtl. sichtbarer Muskelatrophie, abgeschwächten Reflexen, etc.
→ 2) Labor: Nachweis einer CK-Erhöhung und evtl. Myoglobinurie mit Dunkelfärbung des Urins.
→ III: Muskelbiopsie: Fasernekrosen mit Vakuolenbildung, bei Alkohol auch tubuläre Formation.
→ Therapie: Im Vordergrund steht das Absetzen des Medikaments bzw. die Abstinenz von der toxischen Substanz. Durch diese gezielte Intervention ist die exogen-toxische Myopathie zumeist langsam reversibel.
→ Wichtige Beispiele:
→ I: Alkoholmyopathie: Hierbei handelt es sich um eine durch Alkoholabusus verursachte Myopathie. Bei der Pathogenese der alkoholbedingten Myopathie werden direkte toxische Effekte sowie Malnutration diskutiert.
→ 1) Klassifikation: Bei der Alkoholmyopathie werden nach dem klinischen Verlauf 2 Subtypen unterschieden:
→ 2) Klinik: Ein Frühsymptom der Alkoholmyopathie ist der Wadendruckschmerz. Insbesondere bei der chronischen Verlaufsform manifestieren sich Muskelatrophie, proximale Paresen charakteristischerweise im Bereich des Becken- (und Schultergürtels). Zudem kann sich ein paroxysmales Vorhofflimmern („holiday-heart-syndrome“) bis hin zur dilatativen Kardiomyopathie mit konsekutiver Herzinsuffizienz entwickeln, da Alkohol dosisabhängig die glatte Herzmuskulatur schädigt. Bei der akuten Verlaufsform stehen wiederum Symptome wie die Rhabdomyolyse mit massiven Muskelschmerzen, Muskelschwellung und Myoglobinurie, die sich innerhalb von Stunden bis Tagen ausbilden, im Vordergrund. Des Weiteren kann sich aufgrund einer niedrigen alkoholbedingten K+-Plasmakonzentration eine Hypokaliämie-induzierte Myopathie entwickeln.
→ 3) Diagnose: Laborchemisch manifestieren sich eine CK-Erhöhung (massiv insbesondere bei der akuten Verlaufsform) und evtl. eine Hypokaliämie bei K+-verminderter Myopathie. Bei der alkoholinduzierten Myopathie zeigt sich in der Muskelbiopsie charakteristische tubuläre Formationen.
→ 4) Therapie: Im Vordergrund der therapeutischen Interventionen steht die absolute Alkoholkarenz.
→ II: Steroidmyopathie: Bei dieser Form handelt es sich um eine durch Kortikosteroide verursachte Myopathie. Sie entwickelt sich zumeist innerhalb eines Zeitintervalls von 1-4 Wochen nach Therapiebeginn. Auslöser sind zumeist die fluorierten Steroide (z.B. Glukokortikoide), wobei eine signitikante Beziehung zwischen kumulativer Dosis und Auftreten der Myopathie besteht.
→ 1) Klinik: Eine subakute bzw. chronische Verlaufsform der Steroidmyopathie ist durch schmerzlose Paresen und Muskelatrophien v.a. der proximalen Beinmuskulatur gekennzeichnet. Die akute Form wiederum zeigt überwiegend eine rasch einsetzende, proximal betonte Muskelschwäche des Beckengürtels, der Nacken- und Atemmuskulatur. Ursache hierbei ist ein Verlust der sakromerischen Myosin-Filamente.
→ 2) Diagnose: Laborchemisch lässt sich zumeist eine normale bis erhöhte (akute Form) CK-Konzentration nachweisen. Elektromyographisch zeigen sich keine wegweisenden Befunde. In der Muskelbiopsie sind bei der akuten Form der Verlust von Myosin-Filamenten, bei der chronischen Form eine Typ-2-Faseratrophie eruieren.
→ 3) Therapie: Mögliche Interventionen sind u.a. der Austausch fluorierter gegen nicht-fluorierte Steroide, Physiotherapie und als ultima ratio das sofortige Absetzen der Steroide. Nach Absetzen der Medikation remittiert die Symptomatik in der Regel nach 3-6 Monaten vollständig.
→ III: Lipidsenker-Myopathie: (Statin-assoziierte Myopathie).