→ Definition: Beim Lungenödem handelt es sich um eine massive, extravaskuläre Flüssigkeitsansammlung (aus den Lungenkapillaren) initial im Lungenintersitium, später auch im Alveolarraum mit konsekutiver Behinderung des Gasaustausches. Hierbei unterscheidet man zwischen 2 Formen:
→ I: Dem interstitielle Lungenödem: Initial durch Flüssigkeitsansammlung im Bereich der Zellzwischenräume (bzw. des Lungengewebes) und
→ II: Dem alveolären Lungenödem: Im weiteren Krankheitsverlauf tritt die Flüssigkeit in den Alveolarraum (Alveolen, Bronchiolen) über.
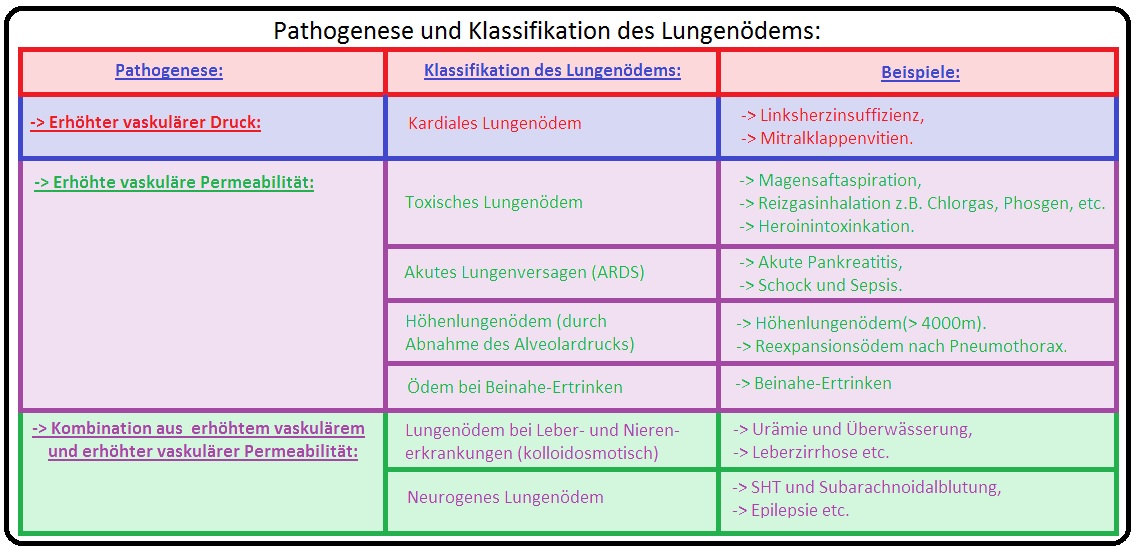
→ Ätiologie: Hinsichtlich der Genese wird es in einen kardialen- und einen nicht-kardialen Typ unterteilt:
→ I: Kardiales Lungenödem: Meist aufgrund einer akuten/chronischen Linksherzinsuffizienz mit immensem Druckanstieg im Lungenkreislauf, verursacht durch:
→ 1) Einen Myokardinfarkt,
→ 2) Hypertensive Krisen,
→ 3) Myokarditiden,
→ 4) Tachykarde und bradykarde Herzrhythmusstörungen oder
→ 5) Eine Dekompensation einer chronischen Herzinsuffizienz bzw. aufgrund von Herzklappenvitien, insbesondere die Mitralinsuffizienz und die Mitralstenose.
→ II: Nicht-kardiales Lungenödem:
→ 1) Durch Abfall des onkotischen Drucks bei akuter oder chronisch dekompensierter Niereninsuffizienz kommt es zum massiven Flüssigkeitsübertritt
→ 2) Erniedrigung des Alveolardrucks bei Punktion großer Mengen Flüssigkeit (Pleurapunktion von > 1,5l kann zu einem Postexpansions-Lungenödem führen).
→ 3) Permeabilitätssteigerung der Alveolargefäße aufgrund allergischer Reaktionen (anaphylaktischer Schock), Noxen wie Reizgase (z.B. Chlorgas), Heroinintoxikation, Magensaftaspiration (Mendelson-Syndrom) oder Aspiration von Süß- und Salzwasser.
→ 4) Weitere Ursachen: Sind Lungenembolie und Schädel-Hirn-Traumata, Komplikationen einer Rickettsiose, infolge einer Sympathikusaktivierung mit konsekutiver Vasokonstriktion.
→ Pathogenese: des kardialen Lungenödems:
→ I: Im Zuge der Linksherzinsuffizienz staut sich das Blut vor dem linken Ventrikel in den Lungenkreislauf zurück mit konsekutivem Druckanstieg. Übersteigt der hydrostatische Druck den entgegengesetzten Drücken, (nämlich Alveolardruck, Gewebedruck und onkotischer Druck) tritt Flüssigkeit aus den Gefäßen in das Lungengewebe (= Interstitium) und im weiteren Krankheitsverlauf in den Alveolarraum über.
→ II: Folgen: des Lungenödems sind u.a.:
→ 1) Abnahme der Lungencompliance und der Vitalkapazität,
→ 2) Erhöhung der Diffusionsstrecke für Sauerstoff,
→ 3) Anstieg des Atemwiderstandes und
→ 4) Entwicklung einer ausgeprägten respiratorischen Insuffizienz mit Hypoxämie (= Abfall der Sauerstoffsättigung im Blut).
→ Klassifikation: Das Lungenödem wird in 4 Stadien unterteilt:
→ I: Stadium I: Interstitielles Lungenödem mit Flüssigkeitsansammlung im Lungengewebe.
→ II: Stadium II: Alveoläre Lungenödem mit Exsudat bzw. Transsudat in den Alveolen und Bronchiolen.
→ III: Stadium III: Schaumbildung mit weiterer Flüssigkeitsausbreitung.
→ IV: Stadium IV: Asphyxie.
→ Klinik:
→ I: Interstitielle Lungenödem: Verschärftes Atemgeräusch mit Giemen, Dyspnoe, Tachypnoe, Orthopnoe evtl. Husten (Asthma cardiale).
→ II: Alveoläres Lungenödem: Körperliche Unruhe, Todesangst, schwerste Dyspnoe, Blässe, Zyanose, feuchte Rasselgeräusche, schaumiges Sputum, Schocksymptomatik. Insbesondere beim ausgeprägten alveolären Lungenödem kardialen Ursprungs kann aus der Distanz ein Trachealrasseln hörbar sein und nicht selten wird ein rötliches, seröses, z.T. schaumiges Sekret abgehustet.
→ Diagnose:
→ I: Anamnese: Kardiale Vorerkrankungen,
→ II: Klinische Untersuchung:
→ 1) Inspektion: kaltschweißige, blasse, evtl. zyanotische Haut, Halsvenenstauung
→ 2) Auskultation: Feuchte Rasselgeräusche initial feinblasig, später grobblasig, zumeist basal lokalisiert, rechts > als links.
→ III: EKG-Monitoring: Eventuell Herzrhythmusstörungen, Ischämiezeichen usw.
→ IV: Röntgen:
→ 1) Parahiläre, schmetterlingsförmige Verschattungen,
→ 2) Beim interstitiellen Lungenödem Nachweis von Karley-B-Linien = laterobasal lokalisierte, horizontal verlaufende Linien in beiden Lungenhälften.
→ 3) Beim alveolären Lungenödem diffuse Verschattungen = Milchglaszeichnung der Lunge.
→ 4) Evtl. radiologisch nachweisbare Zunahme der Herzgröße bei Linksherzinsuffizienz.
→ 5) Das interstitielle Lungenödem ist nur radiologisch (perihiläre schmetterlingsförmige Verschattungen) nachweisbar, das alveoläre Lungenödem imponiert auskultatorisch durch feuchte Rasselgeräusche.
→ V: Labor: Zu bestimmen sind BB, Elektrolytstatus, Retentionswerte (Harnstoff, Kreatinin), Marker der Myokardschädigung (CK, CK-MB,Troponin I/T, LDH etc.) und die BGA z.B. durch Punktion der A. radialis oder ulnaris (Abb.: Normwerte der BGA).
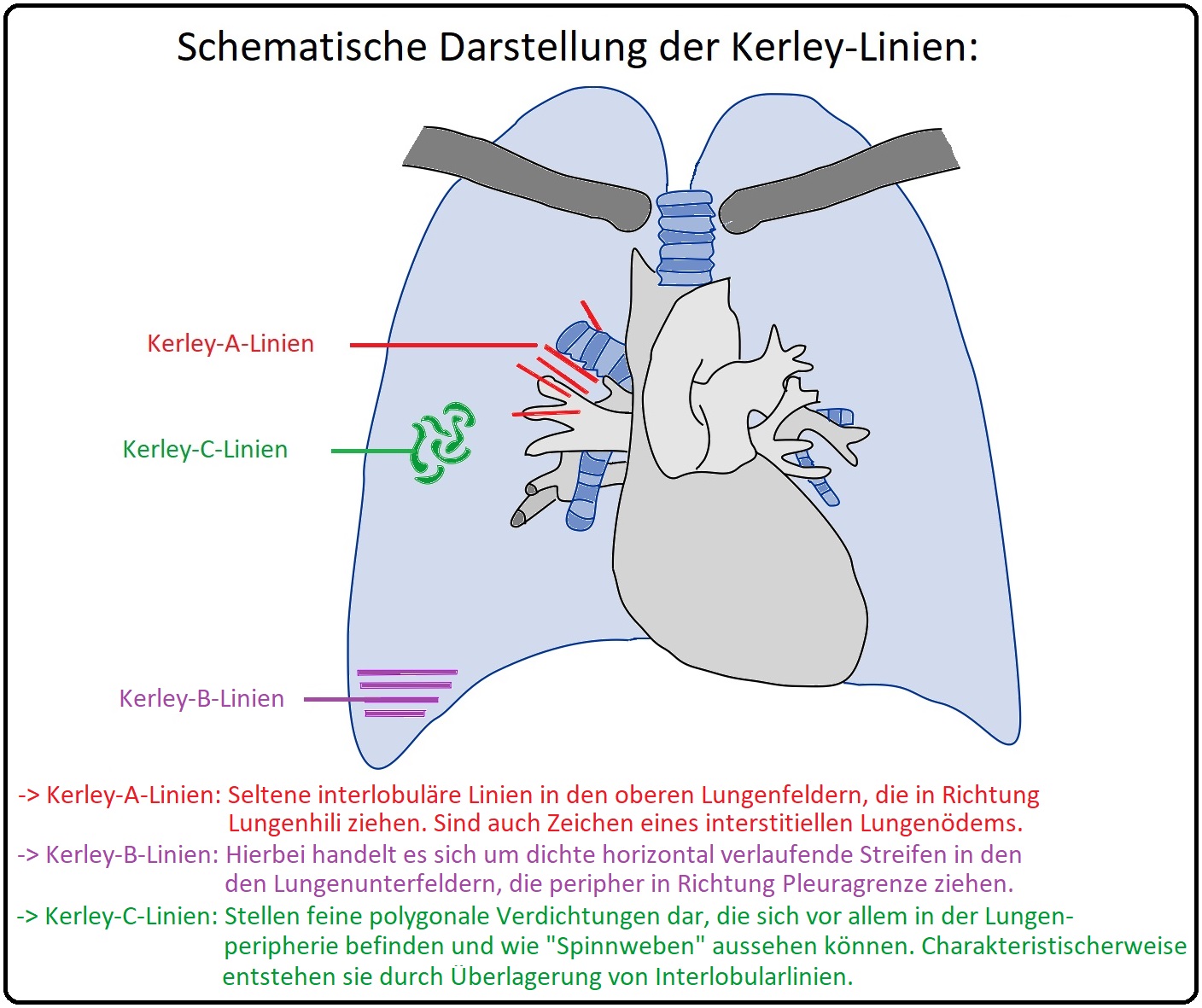
→ Klinisch-relevant: Die Kerley-Linien (= Kerley-A/-B/-C-Linien) sind im Röntgenbild transiente, maximal 1mm breite Linien, die durch eine ödematöse Erweiterung der Bindegewebssepten und der Lymphgefäße entstehen. Es werden hierbei 3 Typen von Kerley-Linien unterschieden:
→ A) Kerley-A-Linien: (= APIKAL) Radiologisch handelt es sich 4-6cm lange, irreguläre Linien, die in der Regel von den Oberlappen Richtung Lungenhili ziehen. Diese selten auftretenden Linien entstehen aufgrund einer Verdickung der Interlobulärsepten und treten u.a. beim interstitiellen Lungenödem auf.
→ B) Kerley-B-Linien: (= BASAL) Hierbei handelt es sich um 1-2cm lange, horizontal verlaufende, nicht-verzweigende Linien, die in den Lungenunterfeldern (= laterobasal) lokalisierte sind und in der Regel die pleurale Grenze erreichen. Sie können durch eine chronische pulmonalvenöse Drucksteigerung z.B. bei Mitralstenose oder Lymphangiosis carcinomatosa fibrosieren und folglich persistieren. Sie sind insbesondere im Bereich des Recessus phrenicocostalis gut erkennbar.
→ C) Kerley-C-Linien: (= CENTRAL) Sie stellen feinmaschige Netzzeichnungen dar, die diffus auf allen Lungenfeldern auftreten können, aber häufig zentral nachweisbar sind.
→ Differenzialdiagnose: Vom Lungenödem sind u.a. nachfolgende Erkrankungen abzugrenzen:
→ I: Die Pneumonie imponiert häufig durch Fieber und den einseitigen Befall der Lunge (Infiltration).
→ II: Das Asthma bronchiale ist insbesondere gekennzeichnet durch das Auftreten von:
→ 1) Trockenen Rasselgeräuschen,
→ 2) Trockener Haut und
→ 3) Durch den Nachweis einer pulmonalen Vorgeschichte.
→ III: Lungenembolie und
→ IV: Atemstörungen bei zerebralen Erkrankungen oder exogenen/endogenen Intoxikationen.
→ Therapie:
→ I: Allgemeinmaßnahmen: Sitzende Lagerung mit herabhängenden Beinen (herabhängende Beine vermindern den venösen Rückfluss und senken somit den hydrostatischen Druck in der Lunge). Die Oxygenierung erfolgt initial 4-8l über eine Maske (CAVE: Bei Patienten mit COPD), nachfolgend nach BGA; evtl. Intubation. Sedierende Maßnahmen (Todesängste) mit Morphin 3-5mg (1:10 verdünnt) s.c. und/oder i.v.
→ Klinisch-relevant: Morphin hat eine vasodilatatorische Wirkung und senkt somit den pulmonalen Gefäßwiderstand.
→ II: Kardiales Lungenödem: Hierbei steht die Vorlastsenkung im Vordergrund:
→ 1) Nitrate: Wie Nitroglycerin 2-3Hub (in höheren Dosen senkt es auch die Nachlast. Anschließend Nitroperfusor 1-6ml/h (1ml = 1mg) nach RR.
→ 2) Schleifendiuretikum: Furosemid 40-80mg i.v. evtl. Wiederholung nach 30min. Bei Patienten mit Niereninsuffizienz ist die Initialdosis deutlich erhöht (125-250mg).
→ 3) Nicht-medikamentöser unblutiger Aderlass durch Abbinden einzener Extremitäten mit einer Blutdruckmanschette.
→ III: Bei Hypotonie: Gabe von Dopamin oder Noradrenalin + Dobutatmin.
→ 1) Dopamin: 1 Amp/5ml entspricht 200mg. Die Dosierung ist 2-12ml/h.
→ 2) Noradrenalin: 1 Amp enthält 1mg. Perfusortherapie (5 Amp auf 45ml einer 0,9%iger NaCl-Lösung) mit einer Dosierung von 3-12 ml/h. Es verursacht eine Vasokonstriktion und eine Steigerung des HZV.
→ 3) Dobutamin: 1 Amp (250mg trocken) auf 50ml einer G-5%iger Lösung. Die Dosierung ist 2-12ml/h. Dobutamin steigert das HZV und hat fast keinen Einfluss auf den Gefäßtonus
→ IV: Bei Herzrhythmusstörungen: Wie den ventrikuläre Tachykardien mit Salvenbildung kann folgendes appliziert werden:
→ 1) Amiodaron: (Cordarex) in einer Dosierung von 150-300mg/i.v. als Bolus über 10 min (bzw. Perfusortherapie 2ml/h).
→ 2) Verapamil (Isoptin) intravenös mit einer Dosierung von maximal 100mg/d (2-10ml/h).
→ V: Allgergisch-toxisches Lungenödem:
→ 1) Bei diesen Formen des Lungenödems ist eine inhalative Glukokortikoid-Applikation mit 5Hub/10min bis zum Abklingen der Symptome indiziert.
→ 2) Bei schweren Formen ist ggf. eine intravenöse Glukokortikoid-Therapie nötig.
→ VI: Kausale Therapie der Grunderkrankung.
→ Klinisch-relevant: Gerade bei der Inhalation von Reizgasen kann das Lungenödem noch nach einer Latenz von 12 Stunden auftreten, sodass eine prophylaktische stationäre Überwachung immer indiziert ist.