→ Definition:
→ I: Die konventionellen Antipsychotika (= klassische Neuroleptika) blockieren primär postsynaptische Dopamin2-Rezeptoren der mesolimbischen und mesokortikalen, dopaminergen Neuronen. Sie weisen aber auch eine antagonistische Wirkung an den 5HT2a-(serotonergen), Alpha1-(adrengerg), H1-(histaminerge)- und den Muskarin-Rezeptoren auf (Ausnahme bildet Sulpirid als reiner D2-Antagonist). Dies verursacht u.a. die psychomotorisch-dämpfende bzw. sedierende, aber auch die antiemetische und hypotherme Wirkung.
→II: Ihre antipsychotische Wirkung bezieht sich ausschließlich auf die Plus-Symptomatik und stellt die sogenannte neuroleptische Potenz dar (die Minus-Symptomatik wird kaum beeinflusst).
→ Klinisch-relevant: Im Zusammenhang mit der Manifestation von extrapyramidal-motorischer-Nebenwirkungen unterscheidet man zwischen den:
→ A) Klassischen Neuroleptika und
→ B) Atypischen Neuroleptika.
→ Klassifikation: Einteilung der Antipsychotika der 1. Generation nach ihrer chemischen Struktur:
→ I: Trizyklische Neuroleptika: Hierzu gehören:
→ 1) Phenothiazine: Sind unselektive D2-Antagonisten und haben ein Wirkspektrum vom Sedativum bis zum hochpotenten Neuroleptikum. Hierzu gehören:
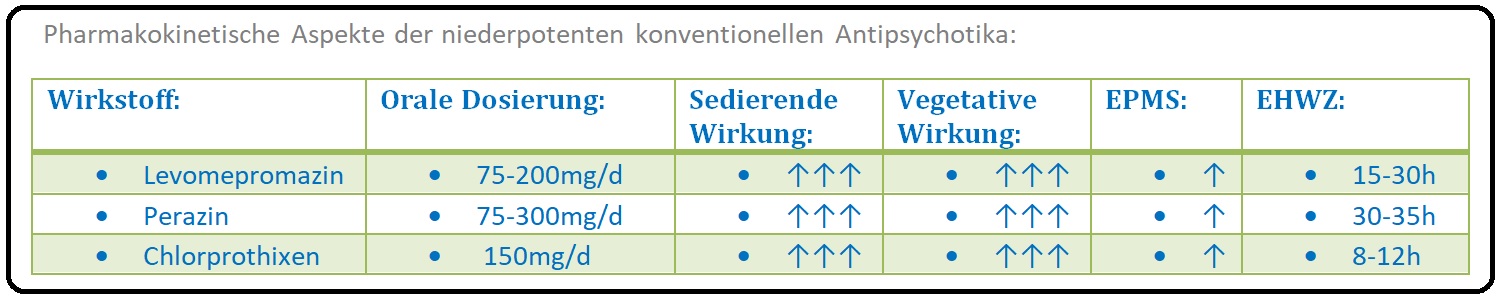
→ A) Niederpotente NL: Promethazin (Atosil), Levomepromazin (Neurocil). Sie sind somit schwach antipsychotisch wirksam und werden vorwiegend als Sedativum eingesetzt.
→ B) Mittelpotente NL: Perazin (Taxilan).
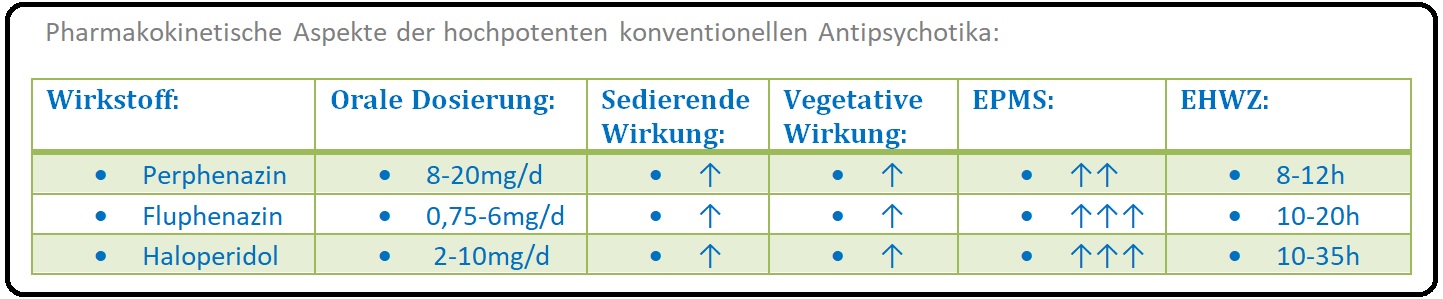
→ C) Hochpotente NL: Perphenazin (Decentan), Fluphenazin (Lyogen).
→ 2) Thioxanthene: Sie gehören wie die Phenothiazine zu den trizyklischen Antipsychotika. Auch hier existieren Substanzen mit einer aliphatischen Seitenkette, die eine niedrige D2-Rezeptoraffinität aufweisen, und Substanzen mit einer Piperazinylseitenkette. Zu ihnen gehören u.a..
→ A) Niederpotente NL: Chlorprothixen (Truxal),
→ B) Mittelpotente NL: Zyclopenthixol (Ciatyl-Z),
→ C) Hochpotente NL: Flupenthixol (Fluanxol).
→ II: Butyrophenone: Hierzu gehören:
→ 1) Hochpotente NL: Haloperidol (Haldol), Benperidol, Bromperidol.
→ 2) Niederpotente NL: Melperon (Eunerpan) und Pipamperon (Dipiperon).
→ III: Diphenylbutylpiperidine: Diese weisen eine sehr hohe Affinität zu den D2-Rezeptoren auf, zu anderen Rezeptoren weniger.
→ 1) Hochpotente NL: Pimozid (Orap), Fluspirilen (Imap).
→ Klassifikation: Nach ihrer neuroleptischen Potenz:
→ I: Niederpotent Neuroleptika: Sie zeichnen sich durch ihre sedierende Wirkung aus ein antipsychotischer Effekt fehlt. Wichtige Indikationen der niederpotenten Neuroleptika sind u.a. Schlafstörungen und die Reduktion von aggressiven Erregungszuständen.
→ 1) Pipameron: = Dipiperon: mittlere Tagesdosis 60-360mg/d.
→ 2) Melperon: = Eunerpan: mittlere Tagesdosis 25-375 mg/d.
→ 3) Levomepromazin: = Neurocil: mittlere Tagesdosis 25-400mg/d.
→ 4) Chlorprothixen: =Truxal: mittlere Tagesdosis 30-400 mg/d.
→ II: Mittelpotente Neuroleptika: Weisen sowohl antipsychotische - als auch sedierende Eigenschaften auf. Werden insbesondere bei angespannten psychotischen und manischen Patienten eingesetzt.
→ 1) Zuclopenthixol: = Ciatyl-Z: mittlere Tagesdosis 2-75 mg/d.
→ 2) Perazin: = Taxilan: mittlere Tagesdosis 50-600 mg/d.
→ III: Hochpotente Neuroleptika: Zeigen bei niedriger bis mittlerer Dosierung eine gute antipsychotische Wirkung ohne sedierenden Effekt. Sie werden insbesondere bei der Behandlung der Produktiv-Symptomatik eingesetzt.
→ 1) Haloperidol: = Haldol: mittlere Tagesdosis 5-30 mg/d.
→ 2) Fluphenazin: = Dapotum: mittlere Tagesdosis 5-40 mg/d.
→ 3) Flupentixol: = Fluanxo: mittlere Tagesdosisl 5-30 mg/d).
→ IV: Depot-Anticholinergika der 1.Generation: Hierzu gehören:
→ 1) Zuclopethixol-Decanoat: Ciatyl-Z-Depot: Die applizierte Dosis liegt zwischen 100-400 mg. Das Applikationsintervall beträgt 2-4 Wochen. Die Applikationsform ist intramuskulär.
→ 2) Fluphenazin: Lyogen-Depot: Die applizierte Dosis liegt zwischen 12,5-100 mg. Das Applikationsintervall beträgt 2-4 Wochen. Die Applikationsform ist intramuskulär.
→ 3) Fluphentixol: Fluanxol-Depot: Die applizierte Dosis liegt zwischen 10-60 mg. Das Applikationsintervall beträgt 2-4 Wochen. Die Applikationsform ist intramuskulär.
→ 4) Haloperidol-Decanoat: Haldol-Decanoat: Die applizierte Dosis liegt zwischen 50-300 mg. Das Applikationsintervall liegt bei 4 Wochen. Die Applikationsform ist intramuskulär.
→ 5) Fluspirilen: Imap: Die applizierte Dosis liegt zwischen 2-12 mg. Das Applikationsintervall liegt bei 1 Woche Die Applikationsform ist intramuskulär.
→ Wirkung: Die Wirkung der konventionellen Antipsychotika wird vor allem durch die Blockade von Dopamin-D2-Rezeptoren erreicht.
→ I: Antipsychotisch: Beinhaltet die Minderung der psychotischen Symptomatik, die u.a. durch den Realitätsverlust und mangelnde Krankheitseinsicht charakterisiert ist.
→ II: Sedierend: Es erfolgt eine Reduzierung des Aggressivitäts- und Erregungszustandes. Je höher die psychomotorisch dämpfende/sedierende Wirkung, desto geringer die antipsychotische Komponente.
→ III: Antiemetisch: Wird durch Blockade der Area postrema (= Triggerzone) des Brechzentrums erreicht.
→ IV: Hypothermisch: Durch funktionelle Ausschaltung des Wärmeregulationszentrums im Thalamus.
→ V: Analgetisch-verstärkend: Konventionelle Neuroleptika führen zum einen zu einer Distanzierung vom Schmerz, zum anderen vermindern sie die Toleranzentwicklung der Analgetika.
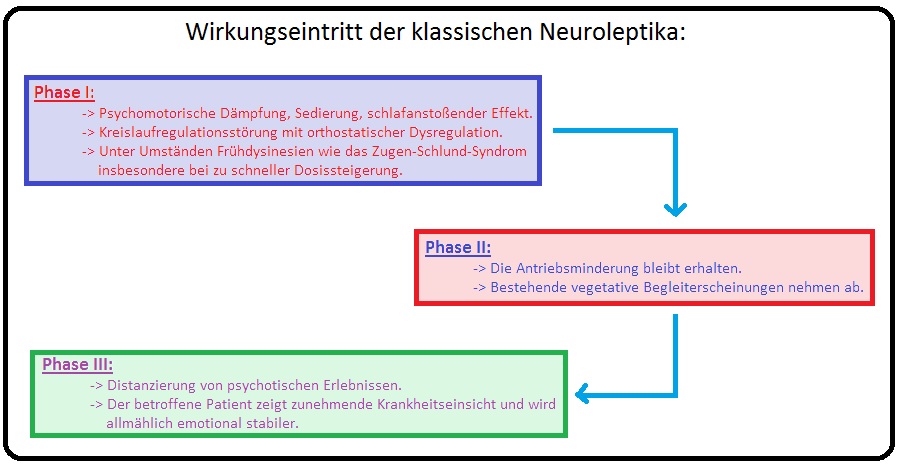
→ Wirkungseintritt: Der Wirkungseintritt verläuft bei den Antipsychotika der 1. Generation typischerweise in 3 Phasen:
→ Indikationspektrum: der Antipsychotika der 1. Generation (Pharmakotherapie der Schizophrenie). Ihre antipsychotische Wirkung bezieht sich ausschließlich auf die Plus-Symptomatik. Hierbei unterscheidet man:
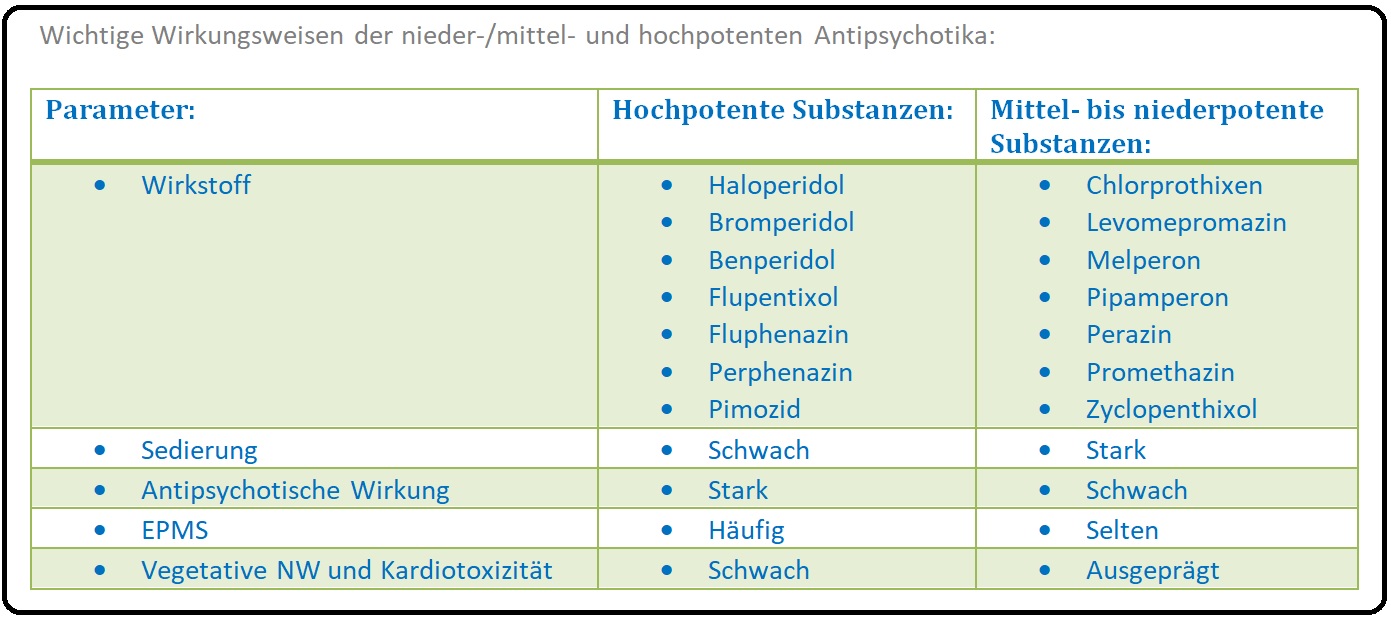
→ I: Klassische Neuroleptika mit schwacher neuroleptischer Potenz: Sie weisen eher eine niedrige Affinität an den D2-Rezeptor auf und werden vorwiegend zur Sedierung und Dämpfung des Patienten bei Schlafstörungen (z.B. Insomnie, etc.), psychomotorischer Unruhe infolge z.B. eines Delirs eingesetzt; hierzu zählen u.a. Levomepromazin, Promethazin, Melperon, Pipamperon.
→ II: Klassische Neuroleptika mit starker neuroleptischer Potenz: Haben eine hohe Affinität zu den D2-Rezeptoren und kommen insbesondere bei der Therapie der akuten psychotischen (produktiven) Symptome aufgrund einer Schizophrenie, aber auch bei einer Depression mit psychotischer Symptomatik zum Einsatz (haben jedoch keinen Einfluss auf die Negativsymptome). Hierzu gehören Haloperidol, Benperidol, Fluphenazin, Flupentixol.
→ Indikation:
→ I: Akute Schizophrenie,
→ II: Rezidivprophylaxe der Schizophrenie,
→ III: Schizoaffektive Störungen: Hierbei handel es sich um Mischpsychosen mit Symptomen aus dem schizophrenen und dem manisch-depressiven Formenkreis. Während die schizomanischen Perioden allein mit einem Antipsychotikum behandelt werden können, werden die schizo-depressiven Episoden meist zusätzlich noch mit einem Antidepressivum therapiert.
→ IV: Demenz-bedingte Psychosen: Bei psychomotorischer Unruhe, psychotischen Erregungszuständen kann die vorübergehende Substitution eines niedrig-dosierten Neuroleptikums (z.B. Haloperidol 1-4mg) Linderung schaffen. Hierbei sollten jedoch Antipsychotika mit einer hohen Affinität zum Muskarinrezeptor (z.B. Chlorprothixen, Olanzapin, Clozapin) gemieden werden, da sie die kognitiven Störungen verstärken.
→ V: Manie: Die psychotische Symptomatik bei der Manie spricht gut auf Antipsychotika an, soadass in der Akutphase eine Kombination mit Lithium üblich ist.
→ VI: Nicht-psychiatrische Indikationen: Sind:
→ 1) Chronische Schmerzzustände,
→ 2) Prämedikation in der Anästhesie und
→ 3) Zytostatika induzierte Übelkeit (z.B. Droperidol 0,625-1,25mg i.v.) im Sinne einer antiemetischen Therapie.
→ Kontraindikation: Wichtige Kontraindikationen für die Behandlung mit Antipsychotika der 1. Generation sind u.a.:
→ I: Intoxikation mit Antidepressiva, Tranquilizer, Hypnotika, Analgetika, aber auch Alkohol.
→ II: Schwere Bewusstseinsstörungen und hirnorganische Vorschädigungen.
→ III: Bekanntes neuroleptisches Syndrom.
→ IV: Des Weiteren besteht erhöhte Vorsicht bei erhöhter Epilepsie-Bereitschaft, Störungen der Hämatopoese und nicht zuletzt bei kardiovaskulären Vorerkrankungen.
→ Klinisch-relevant: Sehr gut lassen sich die nieder- Neuroleptika auch mit den hochpotenten kombinieren.