→ Definition:
→ I: Bei den Benzodiazepinen handelt es sich um die größte Gruppe der Tranquilizer und sie weisen in therapeutischer Dosierung eine angst- und spannungslösende Wirkung auf.
→ II: Die chemische Grundstruktur der Benzodiazepine besteht aus einem Phenylring und einem 7-gliedrigen Diazepinring, der immer ein Phenylrest besitzt (hauptverantwortlich für die Substanzwirkung ist der intakte Diazepinring).
→ III: Sie gehören neben den:
→ 1) Niedrig-dosierten, schwach-potenten Neuroleptika (z.B. Promethazin, Fluspirilen),
→ 2) Non-Benzodiazepin-Tranquilizern (z.B. Opipramol, Buspiron, Hydroxyzin),
→ 3) Barbituraten (heutzutage obsolet) und den
→ 4) Pflanzlichen Sedativa (z.B. Baldrian, Hopfen) zu den Anxiolytika bzw. Sedativa.
→ IV: Hauptvertreter der Benzodiazepine ist das Diazepam.
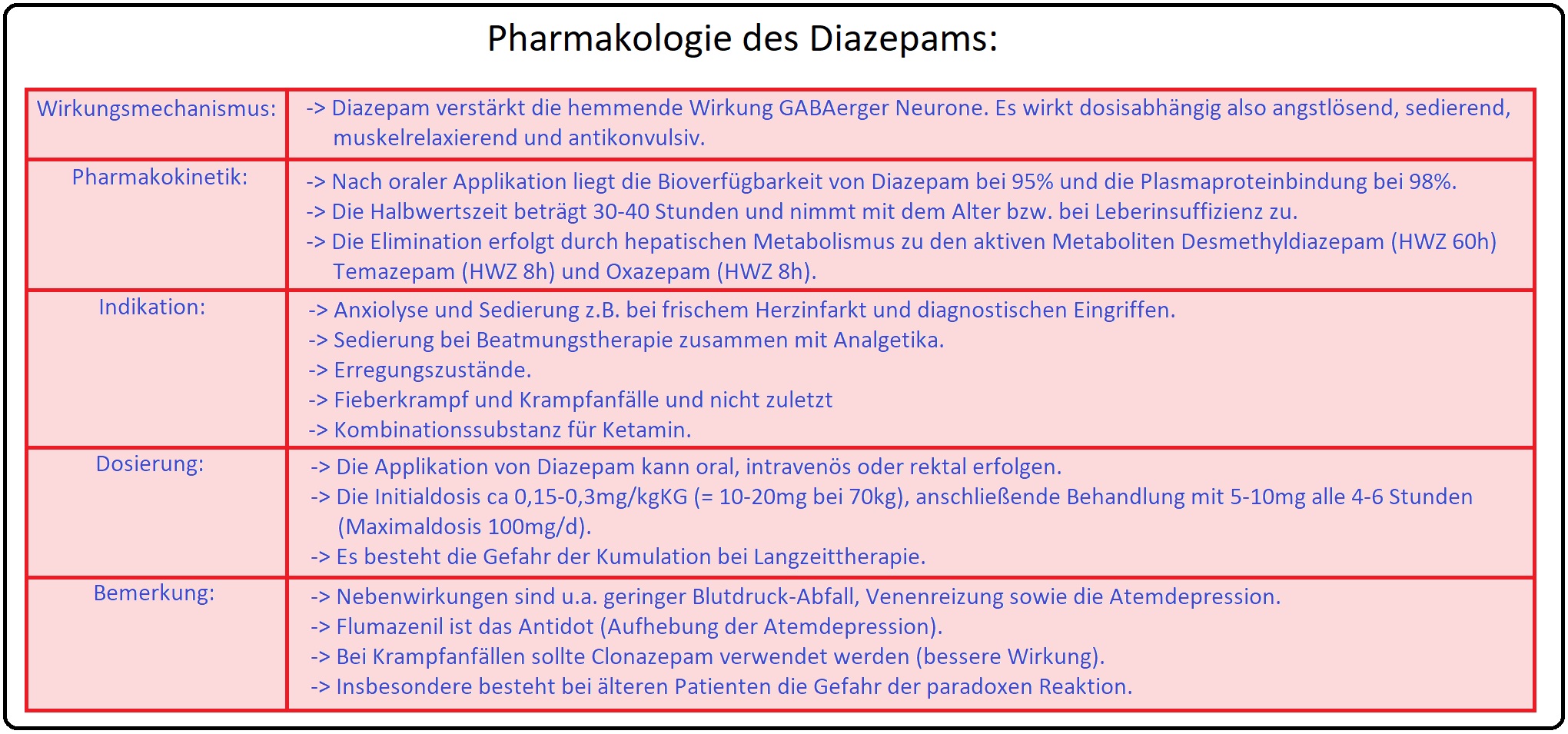
→ Wirkungsmechanismus:
→ I: Benzodiazepine wirken selektiv durch Bindung an eine separate regulatorische Domäne (Alpha-Untereinheit) des GABAA-Rezeptors.
→ II: Folge ist eine Verstärkung der GABA-Wirkung am Rezeptor bzw. ein Anstieg der Affinität des Rezeptors für GABA mit konsekutiver Steigerung der Öffnungswahrscheinlichkeit von Chloridkanälen.
→ III: Es resultiert ein vermehrter Chlorid-Einstrom in die GABAerg innervierten Nervenzellen mit Hyperpolarisation und konsekutiver Hemmung der neuronalen Erregbarkeit.
→ IV: Somit ist die neuronale Wirkung der Benzodiazepine an die Anwesenheit von GABA gebunden (können nicht als direkte GABAA-Agonisten wirken).
→ Klinisch-relevant:
→ A) GABA-A-Rezeptor: GABA stellt den wichtigsten inhibitorischen Rezeptor des ZNS dar und besteht aus 5 Untereinheiten:
→ 1) Alpha-Untereinheit mit insgesamt 6 Isoformen u.a. auch die 1,2,3,5Alpha-Untereinheit.
→ 2) 2 Beta-Untereinheiten und
→ 3) Einer Gamma-Untereinheit. Im Zentrum des Pentamers ist der Cl--Kanal lokalisiert, der durch Aktivierung den Chlorideinstrom steigert und somit die zelluläre Erregbarkeit vermindert.
→ B) Bindungsverhalten: Am GABAA-Rezeptor:
→ 1) Benzodiazepine binden an die 1,2,3,5-Alpha-Untereinheit und erleichtern hierdurch die Bindung von GABA an die ß-Untereinheit,
→ 2) Nicht-Benzodiazepin-Agonisten wie Zopiclon und Zolpidem binden auch an eine Alpha-Untereinheit,
→ 3) An die Beta-Untereinheit binden Barbiturate sowie GABA.
→ 4) Da sich Alkohol auch an die Alpha-Untereinheit des Rezeptors anlagert, wird die Wirkung der Benzodiazepine und GABAA-Agonisten verstärkt.
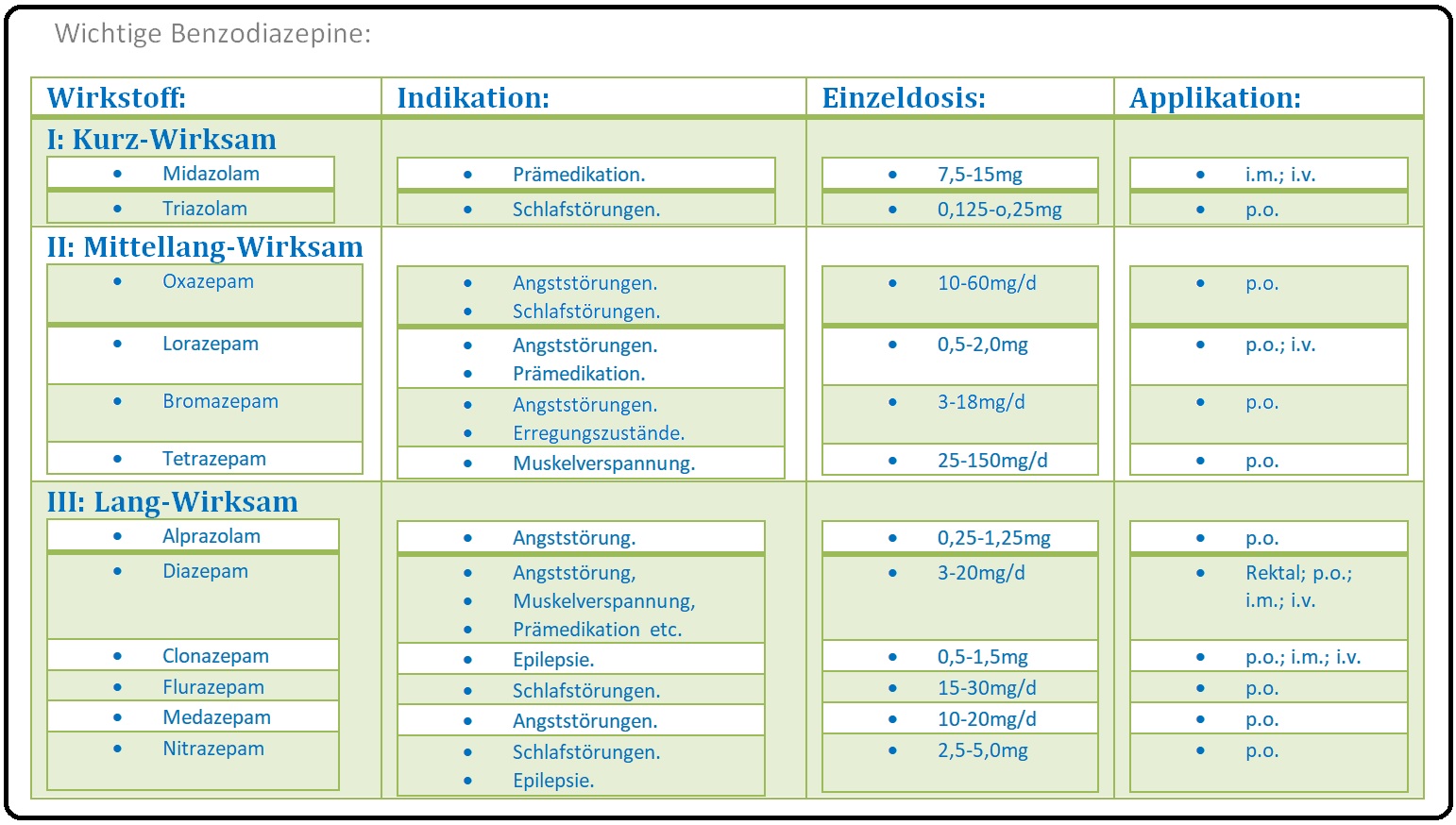
→ Wirkung: Je nach Substanz weisen die Benzodiazepine unterschiedliche Schwerpunkte auf:
→ I: Anxiolytisch: Schon in geringen Dosen wirken Benzodiazepine im Bereich des limbischen System angstlösend.
→ II: Sedativ/hypnotisch: Die sedierende bzw. schlaffördernde Wirkung wird erst bei höheren Dosen erreicht. Flunitrazepam weist aufgrund seiner großen Potenz einen stark sedierenden Effekt auf.
→ III: Amnesie: Benzodiazepine können eine anterograde Amnesie, d.h. Gedächtnislücken nach Verabreichung des Medikaments, hervorrufen.
→ IV: Antikonvulsiv: Benzodiazepine hemmen in hohen Dosen die Erregungsausbreitung im ZNS und entwickeln hierüber einen antiepileptischen Effekt (Epilepsie allgemein).
→ V: Weitere unmittelbare Effekte dieser Substanzgruppe sind schlafinduzierend und muskelrelaxierend.
→ Indikation:
→ I: Angststörungen: Auch im Zuge von Depressionen oder Schizophrenien. Es erfolgt zumeist eine Kombinationstherapie aus Verhaltenstherapie und einer initial passageren medikamentösen Therapie mit z.B. Lorazepam oder Alprazolam.
→ II: Symptomatische Behandlung von akuten Erregungs-, Spannungszuständen sowie Panikerkrankungen und die generalisierte Angststörung.
→ III: Schlafstörungen (= Insomnie) Kurz- bis mittellang wirkende Benzodiazepine, um ein „Hang-over“ Phänomen zu vermeiden.
→ IV: Krampfanfälle: Benzodiazepine erhöhen die Krampfschwelle im Nucleus amygdalae. In der Dauermedikation spielen sie jedoch eine untergeordnete Rolle, da sich frühzeitig eine Toleranzentwicklung mit konsekutiver Wirkungslosigkeit manifestiert. Vielmehr werden sie in der Akuttherapie des Grand mal Anfalls bzw. Status epilepticus (Diazepam 10-20mg i.v., Clonazepam 1-2mg intravenös) oder bei Fieberkrämpfen (Kinder wird Diazepam rektal appliziert) eingesetzt.
→ V: Weitere psychische Störungen: Des Weiteren kann die Gruppe der Benzodiazepine bei nachfolgenden psychischen Störungen eingesetzt werden:
→ 1) Somatoforme Störungen,
→ 2) Delir,
→ 3) Akathisie (= Bewegungsunruhe, Bewegungszwang; z.B. frühes klinisches Zeichen eines Morbus Parkinson) und tardive Dystonien sowie das
→ 4) Alkoholentzugssyndrom.
→ VI: Prämedikation: Zur Prämedikation in der Anästhesie und Narkoseeinleitung. Hierfür eignet sich vor allem das Midazolam (Dormicum).
→ Pharmakokinetik:
→ I: Benzodiazepine werden nach oraler Gabe schnell resorbiert, haben aufgrund ihrer hohen Lipophilie eine rasche zentrale Anflutung und weisen eine hohe Bioverfügbarkeit auf. Sie werden abhängig von ihrer HWZ (sehr variabel) in der Leber über das Cytochrom P-450-System (CYP 3A4, CYP 2C19) metabolisiert (demethyliert und hydroxyliert) und renal eliminiert.
→ II: Metabolisierung:
→ 1) Kurz-wirksame Benzodiazepine: Werden durch Hydroxylierung zum inaktiven Metaboliten abgebaut.
→ 2) Mittellang-wirksame Benzodiazepine: Werden durch Glucuronidierung inaktiviert.
→ 3) Lang-wirksame Benzodiazepine: z.B. Diazepam: Initial wird Diazepam zu N-Desmethydiazepam deakyliert; hierbei entsteht ein Metabolit (= Nordiazepam), der mit einer HZW von 70 Stunden deutlich länger wirksam ist als die Muttersubstanz (Cave: Kumulationsgefahr). Im nächsten Schritt wird Nordiazepam am C3 hydroxyliert (es entsteht Oxazepam), um schließlich über die Glucuronidierung der OH-Gruppe des C3 renal eliminiert zu werden.
→ III: Dosisreduktion:
→ 1) Die Halbwertszeit der Benzodiazepine nimmt mit dem Alter zu, sodass bei älteren Patienten mit einer relativ niedrigen Dosierung begonnen werden sollte.
→ 2) Auch bei Leber- und Niereninsuffizienz ist eine Dosishalbierung insbesondere der mittel- bis langwirksamen Benzodiazepine indiziert.
→ Klinisch-relevant:
→ A) Benzodiazepine besitzen eine große therapeutische Breite bei geringer Toxizität.
→ B) Innerhalb weniger Wochen entwickelt sich bei Dauertherapie eine Toleranzentwicklung mit Wirkungsabnahme und hohem Abhängigkeitspotenzial (= Benzodiazepinabhängigkeit), insbesondere bei Präparaten mit kurzer Halbwertszeit, sodass sie nicht länger als 4-6 Wochen appliziert werden sollten.
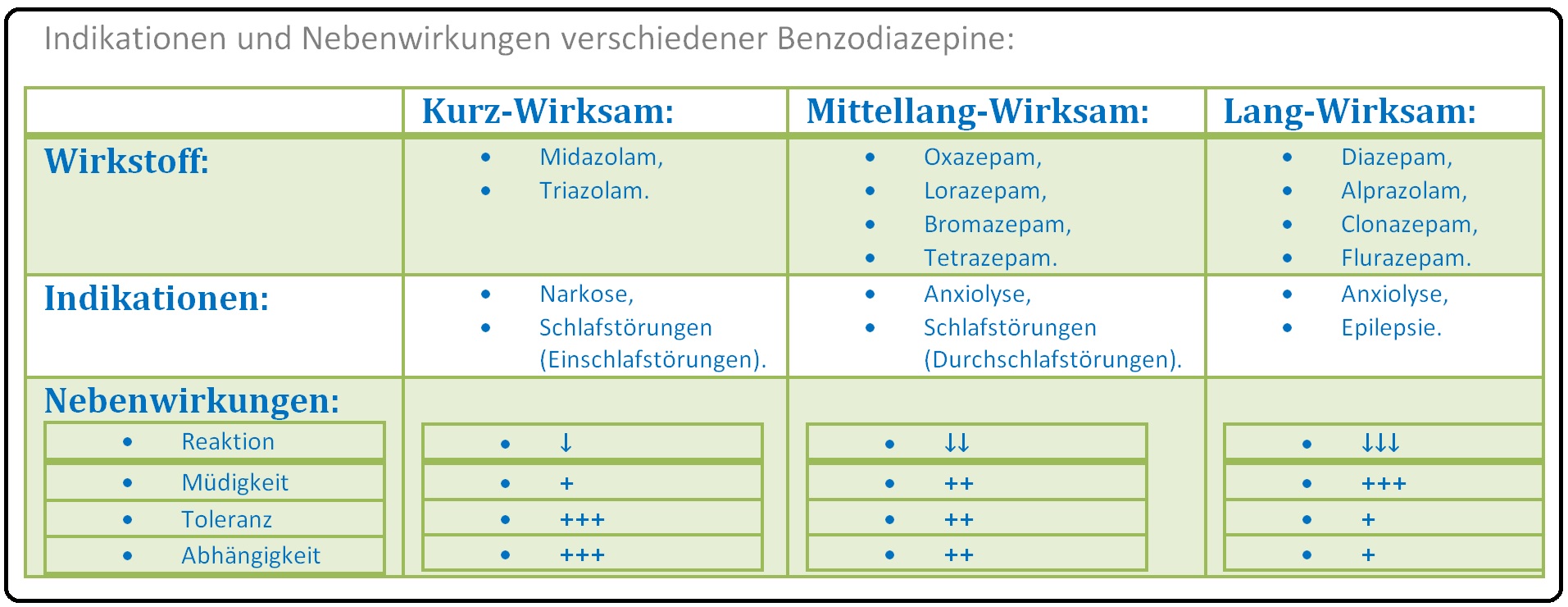
→ Nebenwirkungen:
→ I: Toleranzentwicklung: Ist v.a. abhängig von der Höhe der Dosis und der Dauer der Behandlung und umfasst die verschiedenen Benzodiazepin-Wirkungen unterschiedlich. Bei der antiepileptischen Wirkung ist sie sehr ausgeprägt während sie beim anxiolytischen Effekt gering ist.
→ II: Abhängigkeit: (Benzodiazepinabhängigkeit)
→ 1) Bei einer Langzeittherapie kann sich gerade bei den kurz-wirksamen Benzodiazepinen frühzeitig Missbrauch und Abhängigkeit (psychisch > physisch) entwickeln.
→ 2) Bei der Abhängigkeit unterscheidet man zwischen:
→ A) Low-Dose-Dependence: (= Niedrig-Dosis-Abhängigkeit; stellt die häufigere Dependence-Form dar) Hier besteht eine Abhängigkeit bei Dosierungen im therapeutischen Bereich (= 20mg Diazepam-Äquivalenz), infolge einer Langzeit-Substitution. Es entwickeln sich Entzugserscheinungen wie Angst, Rebound-Insomnie (Schlaflosigkeit), Albträume, myoklonische Zuckungen. Sie zeigt sich insbesondere bei Frauen und ist vermehrt mit einem Alkoholabusus bzw. -abhängigkeit assoziiert.
→ B) High-Dose-Dependence: (= Hoch-Dosis-Abhängigkeit) Manifestiert sich sehr selten und geht mit einer Toleranzentwicklung, Dosissteigerung und schweren Entzugserscheinungen einher.
→ III: Paradoxe-Reaktion: Gerade bei älteren Patienten und Kindern treten im Rahmen einer Benzodiazepin-Therapie gehäuft Symptome wie Unruhe, Angst, Schlaflosigkeit, Erregungszustände, Halluzinationen bis hin zur Aggressivität auf.
→ IV: Atemdepression: Benzodiazepine vermindern die Stimulation des Atemzentrums durch Hypoxie. Dies ist insbesondere bei Patienten mit chronisch-obstruktiven Lungenerkrankungen und gleichzeitiger Einnahme von Opiaten von Bedeutung.
→ V) Rebound-Insomnie: Tritt bei dauerhafter Einnahme und/oder plötzlichem Absetzen auf.
→ VI: Floppy-infant-Syndrom: Infolge der Plazentagängigkeit der Benzodiazepine während der Schwangerschaft bzw. hoher Benzodiazepin-Dosen unter der Geburt. Charakteristische Symptome sind Muskelschwäche, Atemdepression, Trinkschwäche, Hypotonie, Tachykardie und Hypothermie.
→ VII: Weitere Symptome: Sind Sedierung, Müdigkeit, Konzentrationsstörungen, Benommenheit, Schwindel, Koordinationsstörungen, Ataxie, Zyklusstörungen, Libidoverlust, Potenzstörungen etc.
→ Kontraindikationen: Wichtige Kontraindikation für die Benzodiazepine sind u.a.:
→ I: Myasthenia gravis,
→ II: Akute Intoxikationen mit zentral dämpfenden Pharmaka und Alkohol.
→ III: Suchterkrankungen (z.B. Alkoholabhängigkeit, etc.) in der Anamnese.
→ IV: Weitere Erkrankungen: Wie z.B.:
→ 1) Schwere Leber- und Nierenfunktionsstörungen.
→ 2) Akute respiratorische Insuffizienz.
→ 3) Akutes Engwinkelglaukom.
→ 4) Schwangerschaft (vor allem im 1. Trimenon infolge gehäuften Auftretens von Lippen-Kiefer-Gaumenspalten).
→ Wechselwirkungen:
→ I: Alkohol: Und Benzodiazepine verstärken ihre Wirkung wechselseitig und können hierüber lebensgefährliche Intoxikationen hervorrufen (= Benzodiazepinintoxikation).
→ II: Zentral-dämpfende Pharmaka: Wie Antihistaminika, Barbiturate, Narkotika, Opiate aber auch Antidepressiva und Neuroleptika steigern die Wirkung der Benzodiazepine. Auch in Kombination mit MAO-Hemmern zeigt sich eine deutliche Wirkungsverstärkung.
→ III: Die gleichzeitige Einnahme von Antihypertensiva oder Clozapin steigern die Blutdruck-Senkung.
→ IV: In Kombination mit Digitalis (insbesondere Digoxin) manifestiert ein deutlicher Anstieg des Digoxinspiegels mit Gefahr der Digitalisintoxikation.
→ V: CYP-3A4-Inhibitoren: Wie Cimetidin, Diltiazem, Erythromycin, Clarithromycin hemmen den Abbau der Benzodiazepine und verstärken somit die Wirkung.
→ Anwendung:
→ I: Benzodiazepine haben ein breites Wirkungsspektrum und werden u.a. zur Behandlung von pathologischen Angststörungen (z.B. generalisierte Angststörung, Panikattacken, phobische Störungen wie soziale Phobien, etc.), Erregungszuständen und abnormes Konfliktverhalten, aber auch beim Alkoholentzugssyndrom, Schlafstörungen, Epilesie, etc. eingesetzt.
→ II: Zudem können sie den Weg zur Psychotherapie (z.B. Verhaltenstherapie, Gesprächstherapie, Expositionstherapie, etc.) ebnen, indem sie psycho-vegetative Störkreise wie Angst und Panik durchbrechen.
→ III: Weitere Indikationen stellen Neurosen unterschiedlicher Genese sowie psychosomatische Störungen dar.
→ IV: Jedoch bergen Benzodiazepine auch Gefahren, da sie den Patienten durch ihren abschirmenden Effekt daran hindern, sich mit den individuellen Problemen auseinanderzusetzen. Sie fungieren als "Lebenserleichterer" und entwickeln hierüber ein hohes Gewöhnungs- und Abhängigkeitspotenzial (= Benzodiazepinabhängigkeit).
→ V: Alternativen insbesondere bei bestehender Suchtanamnese stellen niedrig dosierte Neuroleptika wie Buspiron dar.
→ VI: In seltenen Fällen schlagen psychotherapeutische Interventionen fehl, sodass eine medikamentöse Langzeittherapie indiziert sein kann. Bei diesen Patienten führt ein abruptes Absetzten der Medikation zu einer psychischen Dekompensation.
→ VII: Therapieablauf: Die Behandlung mit Benzodiazepinen erfolgt je nach Halbwertszeit 1-3x pro Tag in einer niedrigen Dosierung. Bei fehlender Symptomreduktion kann innerhalb der ersten Woche das Präparat aufdosiert werden, bis eine klinische Besserung erreicht wird. Anschließend wird eine schleichende Dosisreduktion versucht. Die Therapiedauer sollte kurzfristig sein und einen Zeitraum von 2-3 Monaten nicht überschreiten.
→ Klinisch-relevant: Benzodiazepine sollten immer ausgeschlichen werden, um ein Rebound-Phänomen mit konsekutivem Wiederauftreten bzw. Verstärken der ursprünglichen Symptomatik zu vermeiden.