→ Definition:
→ I: Nicht-alkoholische Fettleberkrankheit: (= NAFLD) Beinhaltet ein Spektrum von Fettlebererkrankungen, bei denen Alkohol (< 20g/d bei Männern und <10g/d bei Frauen) als Ursache ausgeschlossen ist. Hierzu zählen insbesondere:
→ 1) Nicht-alkoholische Fettleber: (= NAFL) Diffuse Verfettung der Leber (mindestens 50% der Hepatozyten weisen einen erhöhten Lipidgehalt auf) bzw. der Lipidgehalt übersteigt > 5% des Lebergewichtes.
→ 2) Nicht-alkoholische Steatohepatitis: (= NASH) Sie stellt eine nicht-alkoholische Fettleber dar, die die histologischen Charakteristika der Inflammation und Hepatozytendestruktion aufweisen.
→ 3) NASH-Zirrhose: Bei dieser Form besteht eine Leberzirrhose auf dem Boden einer nocht-alkoholischen-Steatohepatitis.
→ II: Sekundäre Steatosis: Hierbei handelt es sich um eine Fettleber, deren Ursprung weder Alkohol noch das metabolische Syndrom sind. Ursachen sind u.a.:
→ 1) Hepatitis C,
→ 2) Morbus Wilson, Zöliakie sowie die chronisch-entzündlichen Darmerkrankungen (Morbus Crohn, Colitis ulcerosa,).
→ 3) Totale parenterale Ernährung, Mangelernährung, langes Fasten und das Kurzdarmsyndrom.
→ 4) Fettstoffwechselstörungen: (metabolisch, genetisch wie z.B. Dysbetalipoproteinämie, familiäre Hyperlipidämie, Morbus Weber-Christian, akute Schwangerschaftsfettleber, Glykogenosen, etc.
→ 5) Medikamenteninduziert: Amiodaron, Nifedipin, Diltiazem, Valproat, Kortikosteroide, Methotrexat, hochdosiert Östrogene, Amphetamine, etc.
→ Epidemiologie:
→ I: Die nicht-alkoholische Fettleberkrankheit stellt mit einer Prävalenz von 14-24% die häufigste Lebererkrankung in den westlichen Industrienationen dar. Somit ist zukünftig mit einem Anstieg der Leberzirrhose- und hepatozellulären Karzinom-Rate zu rechnen.
→ II: Eine gesicherte nicht-alkoholische Steatohepatitis (= NASH) findet man in 2-15% der Leberlebendspender.
→ Pathophysiologie:
→ I: Der wichtigste Risikofaktor für die Entwicklung einer nicht-alkoholischen Fettleberkrankheit ist das metabolische Syndrom, wobei hier die Insulinresistenz und deren Folgen, insbesondere die Hyperinsulinämie und Lipolyse, zu einer Verfettung der Hepatozyten führen. Die vermehrte Aufnahme von Fettsäuren in die Hepatozyten verursacht eine Erschöpfung der mitochondrialen ß-Oxidation mit konsekutiver Fettsäurenakkumulation.
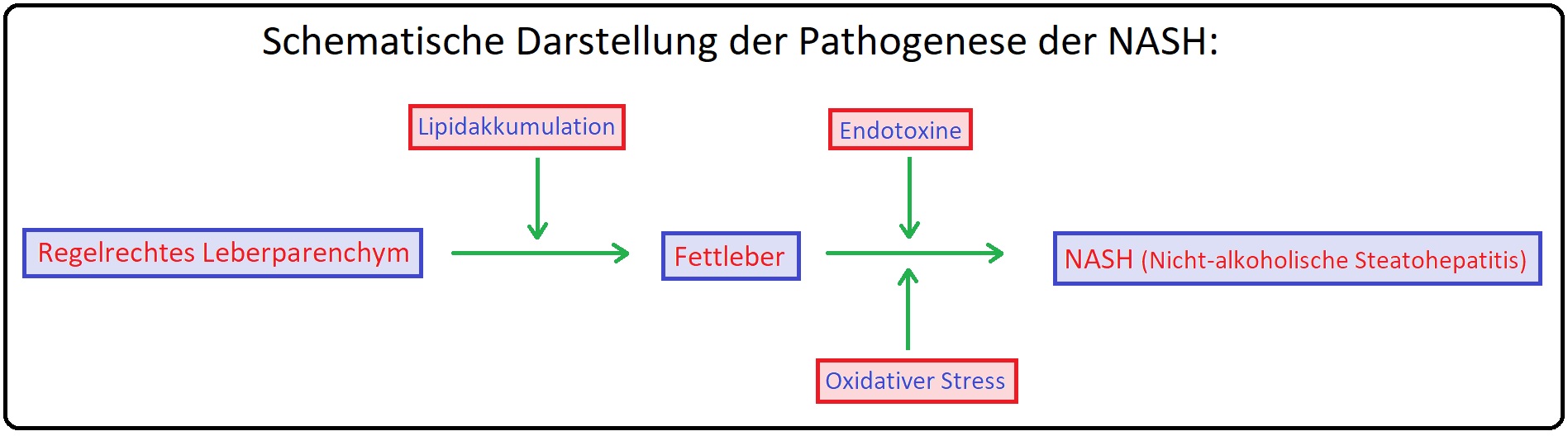
→ II: NASH-Entwicklung: Die intrazelluläre Lipidakkumulation erhöht die Sensitivität der Hepatozyten gegenüber schädlichen Faktoren. Der nächste Schritt ist multifaktoriell und führt zu einem inflammatorischen Infiltration mit Leberzellschädigung. Hierbei spielen insbesondere:
→ 1) Oxidativer Stress und Lipidperoxidation sowie die
→ 2) Endotoxämie mit vermehrter Zytokinproduktion von TNF-Alpha und apoptotischer Zelltod eine zentrale Rolle.
→ III: Weitere Risikofaktoren: Und mit der NASH assoziierte Erkrankungen sind u.a.:
→ IV: Apoptotische Mechanismen:
→ 1) Die Anhäufung von freien Fettsäuren in den Hepatozyten führt reaktiv über die Generierung oxidativer Spezies in den Mitochondrien zur Lipidperoxidation der Hepatozytenmembran und schließlich zum Zelltod.
→ 2) Weitere Apoptose-induzierende Prozesse sind die endotoxinvermittelte Expression von TNF-Alpha sowie die durch den oxidativen Stress verstärkte Expression von CD95-Ligand.
→ Klinik: Häufig existieren lange Zeit keine klinischen Symptome (sind sind insbesondere vom Ausmaß und Zeitraum der Entwicklung der Verfettung abhängig):
→ I: Allgemeinsymptome: Wie Müdigkeit, Abgeschlagenheit sowie uncharakteristische Oberbauchbeschwerden.
→ II: Evtl. Schmerzen bei Leberkapseldehnung bei rascher Fetteinlagerung.
→ III: Vor allem bei der NASH-Zirrhose manifestieren sich Zeichen einer portalen Hypertension.
→ Komplikationen: Wichtige und z.T. schwerwiegende Komplikationen insbesondere der NASH (= nicht-alkoholische Steatohepatitis) sind:
→ I: Portale Hypertension,
→ II: Ösophagusvarizen mit der Gefahr der akuten Ösophagusvarizenblutung.
→ III: Entwicklung einer Leberzirrhose bis hin zum
→ IV: Hepatozellulären Karzinom.
→ Diagnose:
→ I: Anamnese/klinische Untersuchung: Eruierung von Vorerkrankungen wie Adipositas, Diabetes mellitus Typ 2, gestörte Glukosetoleranz, Hyperlipoproteinämie, etc. (ein regelmäßiger Alkoholgenuss muss ausgeschlossen werden) sowie die Erfassung von BMI, Bauchumfang und Blutdruck.
→ II: Labor:
→ 1) Erhöhung der Transaminasen insbesondere GPT (GPT > GOT auf das 1,5-3-fache), aber auch yGT, Cholinesterase, evtl. auch der alkalischen Phosphatase (10-30%). Der GOT/GPT-Quotient liegt unter 1.
→ 2) Erhöhung des Serumferritinwertes (Transferrinsättigung) als Folge eines entzündlichen Prozesses.
→ 3) Des Weiteren Kontrolle der Lipide, Nüchternglukose, HbA1c, Immunparameter (wie ANA, SMA, SLA, LKM, etc.) und nicht zuletzt der Hepatitis B und C-Serologie.
→ 4) Einschätzung: Des Fibrosegrades wird mittels NAFLD-Fibrosis-Score gestellt. Sie beinhaltet Parameter wie Alter, BMI, Blutzucker, Thrombozyten, Albumin, GOT/GPT-Quotient, aber auch die Elastographie. Die Beuteilung erfolgt dann in eine Klassifikation, nämlich geringe, intermediäre und hohe Wahrscheinlichkeit einer fortgeschrittenen Fibrose.
→ III: Bildgebung:
→ 1) Sonographie: Die Sonographie weist bei der Diagnosestellung der Fettleber eine hohe Sensitivität auf. Sonographische Charakteristika einer Fettleber sind Hepatomegalie, diffus vermehrte Echogenität (die Leber ist heller als der Nierenparenchymmantel) und die Abrundung der Leberränder, ggf. mit beginnenden Zirrhosezeichen.
→ 2) Auch mittels CT und MRT ist der Nachweis einer Fettleber möglich.
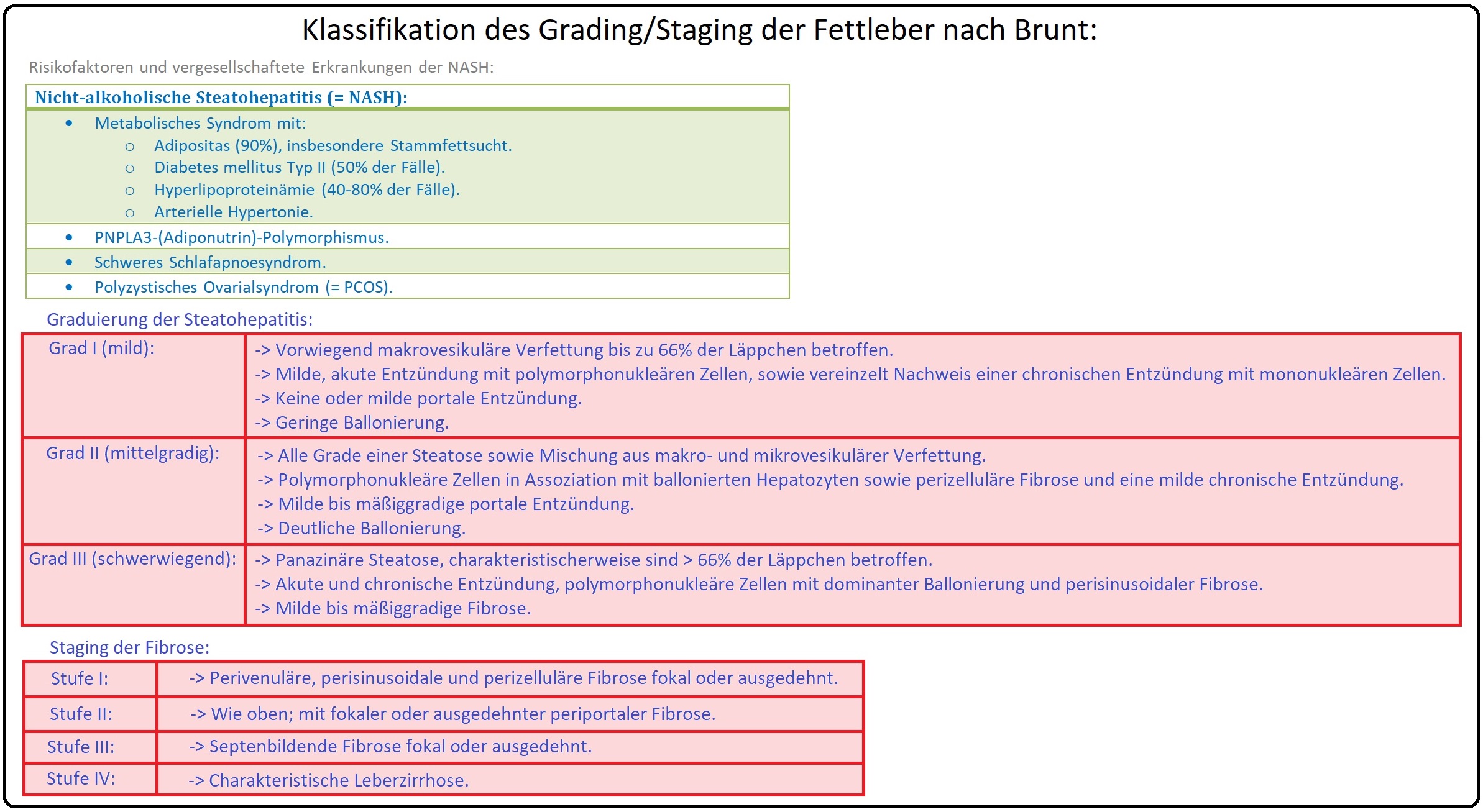
→ 3) Leberbiopsie: Dient der genauen Bestimmung des Ausmaßes der Leberschädigung und wird v.a. bei Verdacht auf Leberzirrhose eingesetzt. Die NASH zeigt histologisch eine makrovesikuläre Verfettung mit Infiltration von mononukleären und neutrophilen Entzündungszellen (läppchenzentrale, portale und periportale Entzündungsprozesse). Die Hepatozyten sind teilweise balloniert und nekrotisch. Zudem findet man häufig Mallory-Körperchen sowie eine perivenöse, perisinusoidale oder periportale Fibrose. Es existiert eine Klassifikation der histopathologischen Veränderung nach Brunt:
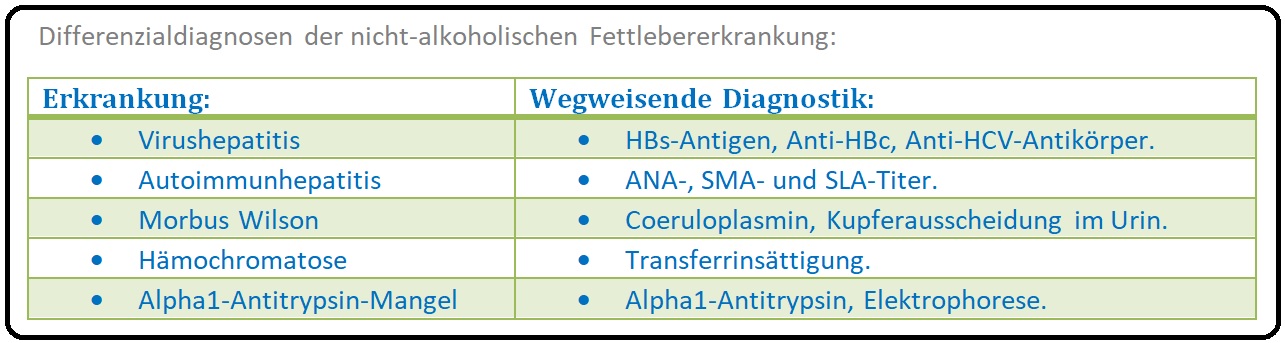
→ Differenzialdiagnose: Von der alkoholischen Fettleberkrankheit müssen insbesondere nachfolgende Erkrankungen abgegrenzt werden:
→ I: Hepatitis B und Hepatitis C mit Bestimmung von Hbs-Antigen, Anti-HBc und Anti-HCV-Antikörpern.
→ II: Autoimmunhepatitis mit möglichem Nachweis von Autoantikörpern wie ANA, SMA und SLA.
→ III: Weitere Differenzialdiagnosen: Sind u.a.:
→ 1) Morbus Wilson,
→ 2) Hämochromatose,
→ 3) Alpha1-Antitrypsin-Mangel,
→ 4) Differenzialdiagnostisch schwierig ist die Abgrenzung zur alkoholinduzierten Fettleberhepatitis, da bis heute keine sicheren histologischen Kriterien zur Unterscheidung existieren.
→ Therapie: Im Vordergrund der Behandlung der nicht-alkoholischen Fettleberkrankheit steht die Bekämpfung der krankheitsauslösenden Faktoren, um eine hepatische Progression zu vermeiden.
→ I: Allgemeinmaßnahmen: Hier spielt die Lebensstilmodifikation eine wichtige Rolle:
→ 1) Schonende Gewichtsreduktion (0,5-1,0kg/Woche) mit Kalorienrestriktion und körperliche Aktivität. Diese führt zumeist zu einer Normalisierung der Hyperlipidämie und gestörten Glukosetoleranz sowie zu einer Verbesserung der Leberwerte und Histologie (60% der Fälle).
→ 2) Alkoholkarenz, Nikotin-, Reduktion des Kaffeekonsums haben einen positiven Effekt.
→ 3) Auch wird das Vermeiden von fruktosereichen Nahrungsmitteln empfohlen (bei Fruktose gibt es Hinweise für ein erhöhtes Progressionrisiko).
→ 4) Impfung insbesondere Hepatitis A und B nach STIKO.
→ Klinisch-relevant: Radikale Fastenkuren können die hepatischen Entzündungsprozesse verstärken und sind kontraindiziert (es sind schon Todesfälle beschrieben).
→ II: Medikamentöse Therapie:
→ 1) Bei der nicht-alkoholischen Fettlebererkrankung kann zur Gewichtsreduktion eine medikamentöse Unterstützung mit Orlistat oder Liraglutid erfolgen.
→ 2) NASH: Aktuell existiert keine zugelassene Medikation. Man weiß jedoch, dass Pioglitazon auf die Insulinresistenz, Leberwerte und -histologie einen positiven Einfluss haben kann. Auch den Antioxidanzien Vitamin C und E wird einen positiven Effekt auf Leberwerte und -histologie zugesprochen.
→ 3) Die Applikation von Statinen zur Senkung der Hyperlipidämie sollte erwogen werden.
→ III: Bei Entwicklung einer NASH-Zirrose sind halbjährige Screening-Untersuchungen (Ösophagusvarizen, HCC mit Sonographie und AFP-Bestimmung).
→ IV: Ultima ratio ist die Lebertransplantation.
→ V: Prävention: Die Primärprävention der nicht-alkoholischen Fettleberkrankheit ist die Vermeidung von Übergewicht, Hyperlipidämie und der daraus resultierenden Insulinresistenz durch eine ausgewogene Ernährung und körperliche Aktivität.
→ Prognose: Der Krankheitsverlauf und die Prognose sind insbesondere vom Stadium der Erkrankung abhängig:
→ I: Die Fettleber hat eine gute Langzeitprognose, jedoch ist ein Übergang in eine NASH möglich (in 10% der Fälle).
→ II: In 10-30% entwickeln Patienten mit einer nicht-alkoholischen Steatohepatitis eine Fibrose oder Leberzirrhose. Folglich stellt die NASH die häufigste Ursache einer „kryptogenen“ Leberzirrhose dar.
→ III: Das Risiko für die Entstehung eines hepatozellulären Karzinoms ist mit dem einer Hepatitis-C-assoziierten Leberzirrhose vergleichbar, sodass engmaschige Kontrollscreening-Untersuchungen obligat sind.