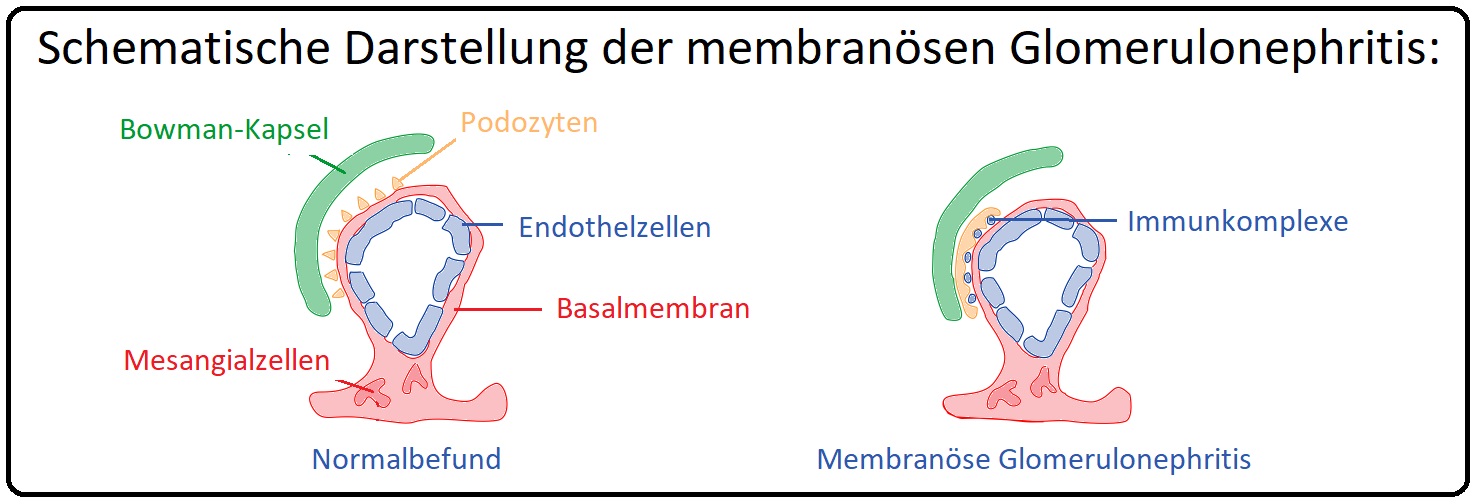
→ Definition: Bei der membranösen GN handelt es sich um eine Störung der podozytären Schrankenfunktion durch eine subepitheliale Ablagerung von Immunkomplexen und Komplement an der Außenseite der glomerulären Basalmembran. Histologische Kennzeichnung sind kleine spikeartige Ausziehungen der Basalmembran, die im weiteren Krankheitsverlauf zu Verdickung der Basalmembran führen.
→ Epidemiologie: Die membranöse Glomerulonephritis stellt mit einer Prävalenz von 1-2/100000 pro Jahr eine seltene Erkrankung dar und ist mit 30-50% der Fälle die häufigste Ursache für die Entwicklung eines nephrotischen Syndroms im Erwachsenenalter (Manifestationsgipfel zwischen dem 50.-55. Lebensjahr, wobei Männer häufiger als Frauen betroffen sind).
→ Ätiologie: Die genaue Enstehung der membranöse GN ist bis heute noch nicht genau geklärt. Aufgrund der Ablagerung von IgG und Komplement C3 wird von einem Immunologischen Pathomechanismus ausgegangen.
→ I: Primäre membranöse GN: Ist mit 80% der Fälle die häufigere Form und es handelt sich um eine idiopathische membranöse Glomerulonephritis.
→ II: Sekundäre membranöse GN: Ist in 20% der Fälle nachweisbar.
→ 1) Infektionen:
→ A) Hepatitis B/Hepatitis C,
→ B) HIV,
→ C) Lues und Echinokokkose.
→ 2) Medikamente: ACE-Hemmer insbesondere Captopril, Gold, Penicillamin.
→ 3) Andere Erkrankungen:
→ A) Lupus erythematodes, rheumatoider Arthritis, Sarkoidose, Sögren-Syndrom, etc.
→ B) Morbus Basedow, Hashimoto-Thyreoditis,
→ C) Tumor-assoziierte Antigene infolge von malignen Neoplasien wie beim Bronchial- oder kolonrektales Karzinom.
→ Pathogenese: Bei der membranösen GN kommt es im Zuge einer Immunkomplexbildung (durch Bildung von Ak gegen Podozytenantigene; als Zielantigen ist der Phospholipase A2-Rezeptor in der Podozytenmembran identifiziert worden) an den Podozyten über die Komplementaktivierung (Komplementfaktoren C5b-C9) zu einer entzündlichen Reaktion. Diese führt zu einer Dysregulation in den Podozyten, wodurch Sauerstoffradikale und Zytokine freigesetzt werden, die die Podozyten sowie weitere Proteine (z.B. Kollagen IV) in der Basalmenbran schädigen.
→ Klinik: Charakteristische Symptome der membranösen GN sind:
→ I: Die Ödembildung ist Leitsymptom der membranösesn Glomerulonephritis und entwickelt sich zumeist langsam, im Bereich der Knöchel und Unterschenkel. Steigt die Proteinurie > 3g/24h manifestiert sich ein nephrotisches Syndrom mit stark ausgeprägten Ödemen am ganzen Körper (Abb.: Differenzialdiagnose nephrotische - und nephritisches Syndrom).
→ II: Mikrohämaturie (50%) und
→ III: Arterielle Hypertonie in 25% der Fälle, wobei der Grad der Hypertonie mit Progression der Erkrankung zunimmt.
→ IV: Bei der sekundären Form stehen Symptome der zugrundeliegenden Erkrankung im Vordergrund.
→ VI: Komplikationen: Wichtige und z.T schwerwiegende Komplikationen der membranösen Glomerulonephritis sind u.a.:
→ 1) Erhöhtes Risiko für die Entwicklung von tiefen Venenthrombosen, insbesondere der Nierenvenen; so kann eine membranöse GN durch eine Lungenembolie klinisch sichtbar werden.
→ 2) In 5% der Fälle entwickelt sich eine rapid progressive Glomerulonephritis.
→ 3) Vermehrte Assoziation mit der diabetischen Nephropathie, dem Goodpasture-Syndrom oder der Wegener-Granulomatose, etc.
→ Diagnose:
→ I: Labor:
→ 1) Bei der idiopathischen Form serologischer Nachweis von Anti-PLA2-R1-Antikörper und THSD7A-Antikörper.
→ 2) Des Weiteren Bestimmung von ANA (ein hoher Titer weist auf einen Lupus erythematodes hin), möglicher Nachweis von p- und cANCA und von glomerulären Anti-Basalmembran-Antikörpern.
→ 3) Bestimmung des Komplementfaktors C3; dieser ist regelrecht bei idiopathischer membranöser Glomerulonephritis und erniedrigt bei systemischen Lupus erythematodes und Hepatitis-B-Infektion.
→ 4) Zeichen eines nephrotischen Syndroms mit Proteinurie (> 3.5g/d), Hypoproteinämie und Hypalbuminämie mit Ödembildung sowie Hypercholesterinämie.
→ Klinisch-relevant: Bei Nachweis einer THSD7A-Antikörper-positiven membranösen Glomerulonephritis liegt die Prävalenz für ein Malignom bei 25% der Fälle, sodass bei dieser Form der mambranösen Gloermulonephritis immer eine Tumorsuche empfohlen wird (bzw. obligat ist).
→ II: Nierenbiopsie:
→ 1) Verdickung der Basalmembran
→ 2) Nachweis von Basalmembranspikes und Fusion der Podozytenfortsätze.
→ III: Risikoklassifizierung: Zur Beurteilung der Prognose:
→ Therapie:
→ I: Kausal: Bei den sekundären Formen Behandlung der Grunderkrankung.
→ II: Symptomatisch:
→ 1) Therapie des nephrotischen Syndroms mit körperlicher Schonung, EW-Restriktion < 0,8g/kgKG/d, diuretische Kombinationstherapie mit Spironolacton und einem Thiazid.
→ 2) Therapie der arteriellen Hypertonie (Zielwert <125/80) mit einem ACE-Hemmer oder AT-1-Hemmer.
→ 3) Therapie der Hypercholesterinämie (Statine).
→ 4) Bei Serumalbuminwerte < 25g/l ist wegen der erhöhten Thromboemboliegefahr eine Antikoagulation (z.B. Heparine) indiziert.
→ 5) Immunsuppressive Therapie: Diese ist bei Patienten mit intermediärem Risiko und einem Serumkreatinin > 1,5mg/dl und bei allen Patienten mit hohem Risiko indiziert.
→ A) Prednisolon + Cyclophosphamid über 6 Monate.
→ B) Alternativ Pednisolon + Cyclosporin (kontraindiziert bei deutlich eingeschränkter GFR).
→ Klinisch-relevant:
→ A) Die Behandlung des therapierefraktären nephrotischen Syndroms erfolgt mittels Rifuximab.
→ B) Häufig zeigt sich trotz adäquater Therapie eine z.T. hohe Rezidivrate.
→ C) Nach einer möglichen Nierentransplantation kann sich die membranöse Glomerulonephritis erneut im Transplantat manifestieren.
→ Prognose:
→ I: Der Spontanverlauf der membranösen GN folgt der 1/3-Regel. Ein Drittel der Patienten entwickeln innerhalb der nächsten 10 Jahre ein Nierenversagen mit anschließender Nierenersatztherapie. 1/3 weist ein chronisches Stadium mit dauerhafter Proteinurie (Nierenfunktion stabil) auf und das letzte Drittel erfährt eine Spontanremission.
→ II: Prognostisch ungünstige Faktoren hierbei sind v.a.:
→ 1) Proteinurie > 10g/d sowie ein erhöhter Kreatininwert.
→ 2) Schwere arterielle Hypertonie.
→ 3) Interstitielle Fibrose bei der Biopsie und
→ 4) Männliches Geschlecht.