- Details
- Kategorie: Orale Antidiabetika
- Zugriffe: 10709
→ Definition:
→ I: Die Glitazone gehören zu der Substanzgruppe der Thiazolidinedione und werden zur medikamentösen Therapie des Diabetes Typ 2 eingesetzt. Es handelt sich hierbei um ein Insulinsensitizer mit Verbesserung der Insulinwirkung an Leber-, Muskel- und Fettzellen durch Regulation der Genexpression. So kommt es bei Patienten, bei denen eine Insulinresistenz im Mittelpunkt des pathophysiologischen Geschehen steht, zur Verbesserung der Insulinwirkung mit konsekutiver Normalisierung der Glukosekonzentration im Blut.
→ II: Die wichtigste und einzig zugelassene Substanz stellt das Pioglitazon (Rosiglitazon) dar.
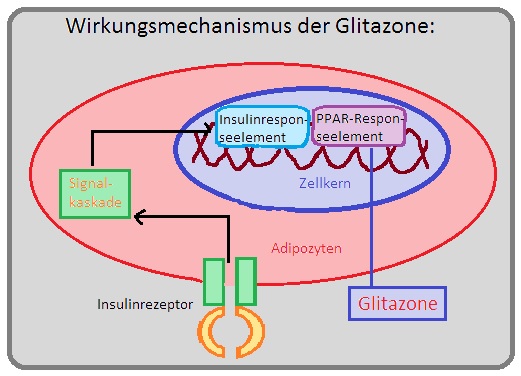
→ Wirkungsmechanismus:
→ I: Sie binden agonistisch an den PPAR-y (= Peroxisomal-Proliferative-Activated-Rezeptor-y) und steigern als Transkriptionsfaktor im Zellkern der Fett-, Muskel- und Leberzellen die Expression des insulinabhängigen Glukosetransporters-4 (GLUT-4). Ihre Wirkung erlangt Pioglitazon nur in Gegenwart von Insulin.
→ II: Sie steigern die Insulinwirkung auf Leber (durch Hemmung der hepatischen Glukoseproduktion) und Muskulatur; Folge ist eine verbesserte und vermehrte Glukoseaufnahme in die Zielgewebe.
→ III: Zudem fördern die Thazoliddindione die Fettdifferenzierung und das Fettgewebe-Wachstum (Lipogenese).
→ Wirkung:
→ I: Verbesserte Insulinwirkung an den Zielgeweben (Fett-, Muskel- und Leberzellen) durch agonistischen Effekt am PPAR-y mit konsekutiver Verminderung der Glukoseresistenz (und des Blutzuckerspiegels).
→ II: Senkung der Lipoproteinämie mit Zunahme von HDL und Senkung von LDL und der Triglyzeride.
→ III: Verbesserung des Blutdrucks, jedoch
→ IV: Gewichtszunahme mit Umverteilung des Fettgewebes (Zunahme des subkutanen – und Abnahme des viszeralen Fetts).
→ Pharmakokinetik:
→ I: Nach orale Einnahme wird Pioglitazon gut resorbiert und nahezu vollständig an Plasmaproteine gebunden.
→ II: Die Metabolisierung erfolgt in der Leber über das Cytochrom-P450-System (CYP2C8; CYP3A4). Die Plasma-Eliminationshalbwertszeit liegt zwischen 3-6 Stunden.
→ III: Der maximale Wirkungseintritt wird erst nach 4-8 Wochen erreicht.
→ Indikation:
→ I: Monotherapie des Diabetes mellitus Typ II,
→ II: Kombinationstherapie mit Metformin, Sulfonylharnstoffe oder Glindine.
→ Klinisch-relevant:
→ A) In der Kombination mit den Sulfonylharnstoffen tritt gehäuft eine Gewichtszunahme und periphere Ödeme auf.
→ B) In Kombination mit Insulin entwickelt sich häufiger eine Herzinsuffizienz.
→ Dosierung: Pioglitazon wird Mahlzeiten-unabhängig appliziert mit einer Dosis von 1x15-30mg/d bis zu einer Maximaldosis von 1x45mg/d.
→ Nebenwirkungen: Pioglitazol weist eine gute Leberverträglichkeit auf; jedoch sollten regelmäßige Kontrollen der hepatischen Funktion erfolgen. Charakteristische unerwünschte Wirkungen der Glitazone sind u.a.:
→ I: Starker Gewichtszunahme, Wasserretention mit Ausbildung peripherer Ödeme,
→ II: Anämie, Herzinsuffizienz und evtl. Infektionen der oberen Atemwege.
→ III: Diarrhoe und Flatulenz und nicht selten auch
→ IV: Kopfschmerzen.
→ V: Bei Frauen wurde eine erhöhte Frakturrate festgestellt.
→ Kontraindikationen: Sind insbesondere;
→ I: Herzinsuffizienz unabhängig vom Schweregrad (NYHA I-IV; insofern ist der Ausschluss einer Herzinsuffizienz vor Therapiebeginn obligat),
→ II: Schwere Leber- und Niereninsuffizienz,
→ III: Schwangerschaft und Stillzeit.
- Details
- Kategorie: Orale Antidiabetika
- Zugriffe: 10508
→ Definition: Bei den Alpha-Glukosidasehemmern handelt es sich um orale Antidiabetika zur Behandlung des Diabetes mellitus Typ II Hierzu zählen insbesondere die Acarbose und Miglitol.
→ Wirkungsmechanismus:
→ I: Hauptwirkung ist die verzögerte intestinale Glukoseresorption (die Glukoseidase-Hemmer senken das HBA1c um 0,5-0,8%) durch verlangsamten Abbau der kompelxen Kohlenhydrate sowie Poly- und Disaccharide in Monosaccharide.
→ II: Da Acarbose und Miglitol, als Pseudotetrasaccharide, den Oligosacchariden ähneln, hemmen sie kompetitiv (reversibel) die intestinalen Alpha-Glukosidasen (Glukoamylase, Maltase, Saccharase), die ihrerseits die Disaccharide (Saccharose, Maltose und Laktose) spalten.
→ III: Folge ist die Verringerung des postprandialen Blutzuckeranstiegs durch Verzögerung der intestinalen Glukoseresorption und langfristige die Senkung des HbA1c-Wertes. Zudem weisen die Gukosidase-Hemmer eine günstige Wirkung auf die Triglyzeride auf.
→ IV: Zusätzlich aktivieren die ungespaltenen Kohlenhydrate im distalen Dünndarm das Enterohormon Glukagon-like-peptid, welches wiederum die Sensibilität der Beta-Zellen des Pankreas steigert.
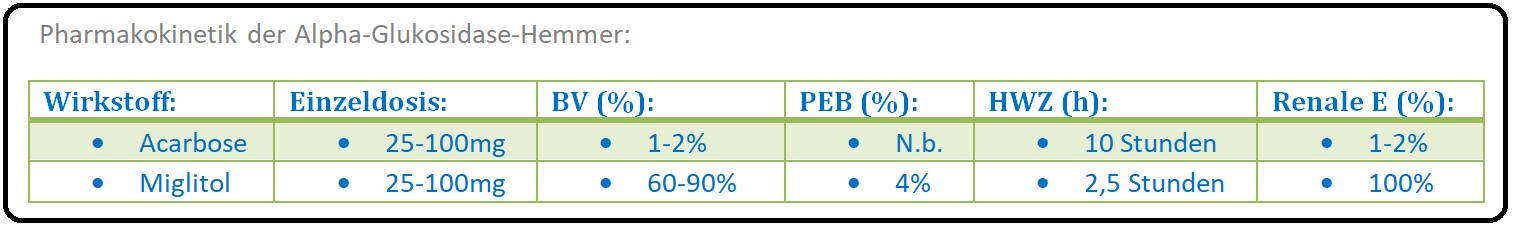
→ Pharmakokinetik: Die Alpha-Glukosidasehemmer werden nach oraler Aufnahme nur in geringem Maße (1-2%) resorbiert. Der Großteil wird in Form seiner Stoffwechsel-Produkte bzw. unverändert über den Darm ausgeschieden; nur ein geringer Teil wird renal eliminiert.
→ Dosierung: Initial einschleichend Dosierung mit 3x 50mg vor den Mahlzeiten, um mögliche Nebenwirkungen zu vermeiden; langsame Steigerung auf 3x 150-300mg/d bis zu einer Maximaldosis von 600mg/d.
→ Nebenwirkungen: Sie rufen insbesondere gastrointestinale Beschwerden mit Abdominalschmerzen und -krämpfen, Meteorismus, Flatulenz und Diarrhoe durch die Vergärung utilisierender Kohlenhydrate hervor. Vor allem die Acarbose kann ein Malassimilationssyndrom induzieren.
→ Klinisch-relevant:
→ A) Die Nebenwirkungen entstehen aufgrund eines Gärungsprozesses nicht gespaltener Kohlenhydrate. Hohe Dosen sollten aufgrund dessen vermieden werden.
→ B) Bei den Glukosidase-Hemmern besteht insbesondere bei der Monotherapie keine Gefahr der Hypoglykämie und Gewichtszunahme.
→ Kontraindikationen: Sind insbesondere:
→ I: Chronisch-entzündliche Darmerkrankungen (Morbus Crohn, Colitis ulcerosa) und das Malassimilationssyndrom.
→ II: Schwere Niereninsuffizienz und
→ III: Schwangerschaft und Stillzeit.
- Details
- Kategorie: Orale Antidiabetika
- Zugriffe: 16151
→ Definition: Metformin, aus der Gruppe der Biguanide, stellt das Mittel der 1. Wahl bei der oralen Behandlung des Diabetes mellitus Typ II dar und wirkt nur in Gegenwart von Insulin ohne den Plasmaspiegel zu erhöhen. Es wird insbesondere bei übergewichtigen Patienten eingesetzt (gewichtsneutrale bis leicht gewichtsreduzierende Wirkung) und hat einen eindeutigen blutzuckersenkenden Effekt mit nur sehr geringem Hypoglykämierisiko.
→ Wirkungsmechanismus: Der genaue Wirkmechanismus der Biguanide ist bis heute noch nicht abschließend geklärt, jedoch wird die Glukoseaufnahme sowie die Insulinwirkung (ohne Erhöhung des Insulinspiegels) in den peripheren Geweben erhöht. Metformin verursacht im Organismus insbesondere:
→ I: Verbesserung des Glukoseumsatzes: Durch
→ 1) Hemmung der intestinalen Glucoseaufnahme,
→ 2) Hemmung der hepatischen Gluconeogenese und
→ 3) Förderung des Glukosetransportes in die Muskelzellen (dieser Effekt reduziert den Insulinbedarf und verlangsamt die Progression der Insulinresistenz).
→ II: Senkung:
→ 1) Senkung des Nüchtern- und postprandialen Blutzuckers.
→ 2) Lipidsenkung, insbesondere von VLDL und der Triglyceride sowie ein Anstieg des HDL-Cholesterins.
→ 3) Gewichtsreduktion durch Steigerung der Lipolyse und Verminderung des Hungergefühls.
→ III: Kohlenhydratstoffwechsel: Metformin wird von den Hepatozyten aufgenommen und lagert sich an die Mitochondrienmembran an, wo es die Atmungskette hemmt (es findet ein Übergang von der aeroben zur anaeroben Energiegewinnung statt). In der Folge kommt es über den Anstieg der AMP-Konzentration zur Aktivierung der AMP-Kinase, die wiederum die Glukoneogenese, aber auch die Synthese von Lipiden und Triglyceriden hemmt.
→ IV: Fettstoffwechsel: Die Aktivierung der AMP-Kinase greift zusätzlich in den Fettstoffwechsel ein, indem sie das Schlüsselenzym, die Acetyl-CoA-Carboxylase, hemmt. Folgen sind:
→ 1) Hemmung der hepatischen Lipidsynthese und
→ 2) Steigerung der Fettsäureoxidation mit konsekutiver Senkung der Triglycerid- und VLDL-Konzentration.
→ Pharmakokinetik: Nach oraler Gabe wird Metformin gut resorbiert und unverändert über die Niere ausgeschieden. Metformin sollte einschleichend dosiert werden, um gastrointestinale Nebenwirkungen zu reduzieren. Die Halbwertszeit liegt bei 2-5 Stunden.
→ Indikation:
→ I: Metformin ist Mittel der 1. Wahl bei der Behandlung des Diabetes mellitus Typ II (insbesondere auch bei übergewichtigen Patienten). Die Kombination mit anderen Antidiabetika wie Sulfonylharnstoffe, Glinide, Glitazone, GLP-1-Agonisten oder Insulin ist möglich.
→ II: Metformin weist bei Patientinnen mit polyzystischem Ovarialsyndrom eine ovulationsfördernde Wirkung auf; bei diesem Syndrom sind typische klinische Zeichen Übergewicht und Insulinresistenz. Zudem führt die Senkung des Nüchtern-Insulinspiegels (durch Metformin) zu einer Verbesserung der Insulinresistenz.
→ Dosierung: Einschleichend mit einer Initialdosis von 1-2x 500mg während oder nach den Mahlzeiten; nach 2-3 Tagen langsame Dosissteigerung bis zu einer Maximaldosis von 3000mg/d bei Erwachsenen.
→ Nebenwirkungen:
→ I: Gastrointestinale Beschwerden mit Bauchschmerzen, Übelkeit, Erbrechen und Diarrhoe sowie die mögliche Ausbildung eines Malassimilationssyndroms.
→ II: Laktatazidose: Metabolische Azidose mit Hyperventilation und konsekutiven BGA-Veränderungen wie pH ↓, paO2 ↑, paCO2 ↓ und Bikarbonat ↓ sowie Laktat ↑ (Abb.: Normwerte der BGA). Selten, jedoch mit hoher Letalität, verursacht durch die Hemmung der hepatischen Gluconeogenese; sie entwickelt sich meist bei Nicht-Einhalten der Kontraindikationen bzw. bei Überdosierung der Substanz. Weitere Risikofaktoren sind gerade:
→ 1) Hohes Alter,
→ 2) Hypoxämie und
→ 3) Myokardinfarkt.
→ III: Weitere Symptome: Sind metallischer Geschmack und Ausbildung einer perniziösen Anämie aufgrund einer verminderten Resorption von Vitamin-B-12 und Folsäure.
→ Kontraindikationen:
→ I: Niereninsuffizienz mit einem Kreatinin im Serum von 1,2mg/dl bzw. Creatinin-Clearance von < 60ml/min.
→ II: Diabetische Ketoazidose, hyperosmolares Koma,
→ III: Stoffwechselstörungen, die mit einem erhöhten Risiko für die Ausbildung einer Laktatazidose. einhergehen. Hierzu gehören u.a. schwere Infektionen, Neoplasien, Herzinsuffizienz NYHA III-IV, respiratorische Insuffizienz.
→ IV: Schwere Lebererkrankungen (da eine Leberinsuffizienz die hepatische Verwertung von Laktat reduziert), Alkoholabhängigkeit und akute Pankreatitis.
→ V: Prä- und Postoperativ sowie vor und nach Kontrastmittelgabe (intravenös): Metformin muss 2 Tage vor bis 2 Tage nach der Kontrastmittelgabe bzw. Operation abgesetzt werden, da ansonsten die Gefahr der Entwicklung einer Niereninsuffizienz besteht.
→ VI: Schwangerschaft und Stillzeit.
→ Wechselwirkungen:
→ I: Cimetidin und Triamteren hemmen die renale Auscheidung von Metformin.
→ II: Steigerung der Metforminwirkung: (= BZ-senkend) durch Alkohol, Beta-Blocker, ACE-Hemmer.
→ III: Verminderung der Metfominwirkung: Durch Glukokortikoide, Beta-2-Sympathomimetika, Thiazide, Schleifendiuretika und L-Thyroxin.
→ Klinisch-relevant:
→ A) Metformin steigert die Insulinwirkung (= vermindert Insulinresistenz) ohne den Insulinspiegel anzuheben.
→ B) Es verringert die Entwicklung von mikro- und makrovaskulären Komplikationen.
→ C) Eine Hypoglykämie bildet sich unter der Therapie mit Metformin nicht aus.
→ D) Es hat keinen Einfluss auf den Stoffwechsel des Gesunden.
- Details
- Kategorie: Orale Antidiabetika
- Zugriffe: 13102
→ Definition:
→ I: Bei den Gliniden (= Insulinsekretagoga) handelt es sich um orale Antidiabetika zur medikamentösen Behandlung des Diabetes mellitus Typ II.
→ II: Die Substanzen dieser Gruppe unterscheiden sich strukturell deutlich von den Sulfonylharnstoffen, haben jedoch den gleichen Wirkungsmechanismus; Hauptvertreter dieser Substanzgruppe sind:
→ 1) Repaglinid und
→ 2) Nateglinid: Ist nur für eine Kombinationstherapie mit Metformin zugelassen.
→ Wirkungsmechanismus: Entspricht dem der Sulfonylharnstoffe.
→ I: Sie steigern die Insulinausschüttung aus den Beta-Zellen der Langerhans-Inseln des Pankreas, indem sie durch Bindung an den Sulfonylharnstoff SHR1 die ATP-abhängigen Kaliumkanäle schließen. In der Folge kommt es aufgrund einer Depolarisierung der Zelle zur Öffnung der Ca2+-Kanäle mit konsekutiver Induktion der Insulin-Inkretion.
→ II: Sie haben jedoch eine andere Bindungsstelle am Kalium-Kanal als die Sulfonylharnstoffe.
→ Pharmakokinetik: Besonderes Merkmal ist ihr schnelles An- und Abfluten nach oraler Zufuhr.
→ I: Ginide haben einen raschen Wirkungseintritt und eine kurze -dauer von ca 3 Stunden. Somit beeinflussen die Glinide nur den postprandialen Blutzuckeranstieg, jedoch nicht (kaum) den Nüchternglukosespiegel.
→ II: Sie werden über das Cytochrom-P-450-System (CYP3A4/CYP2C8/CYP2C9) in der Leber metabolisiert.
→ Klinisch-relevant: Da ihr Wirkungseintritt sehr rasch ist, dürfen sie nur unmittelbar vor den Mahlzeiten substituiert werden, um den postprandialen Glukoseanstieg zu vermeiden. Bei Ausbleiben der Nahrungszufuhr dürfen sie aufgrund der Gefahr einer Hypoglykämie nicht appliziert werden. Bei der Therapie mit Gliniden wird eine hohe Compliance-Anforderung (4-malige Zufuhr/d) an den Patienten gestellt.
→ Indikation:
→ I: Zur medikamentösen Behandlung des Diabetes Typ II.
→ II: Während Repaglinid als Monotherapeutikum verabreicht werden kann, ist Nateglinid nur in Kombination mit Metformin zugelassen.
→ Dosierung:
→ I: Repaglinid: Einschleichender Beginn mit einer Initialdosis von 0,5mg vor den Mahlzeiten. Anschließend schrittweise Dosissteigerung alle 1-2 Wochen bis zu einer maximalen Einzeldosis von 4mg/Mahlzeit (max. Tagesdosis 16mg/d).
→ II: Nateglinid: Initialdosis beginnend mit 3x 60mg/d vor den Mahlzeiten, langsame Steigerung auf 3x 120mg/d bis zu einer Maximaldosis von 540mg/d.
→ Nebenwirkungen: Sind u.a.:
→ I: Hypoglykämie, aber auch deutliche Gewichtszunahme,
→ II: Gastrointestinale Beschwerden mit Übelkeit, Erbrechen, Diarrhoe, evtl. Anstieg der Transaminasen und nicht zuletzt
→ III: Die kardiovaskulären Risiken, die bis heute noch nicht genau geklärt sind.
→ Kontraindikationen: Sind bei den Gliniden insbesondere:
→ I: Diabetes mellitus Typ I,
→ II: Schwere Leberinsuffizienz,
→ II: Ketoazidose und hyperosmolares Koma.
→ III: Schwangerschaft und Stillzeit.
→ Wechselwirkungen:
→ I: Steigerung der Glinid-Wirkung: (= BZ-senkend) U.a. durch Alkohol, Beta-Blocker, ACE-Hemmer, ASS, MAO-Hemmer.
→ II: Senkung der Glinid-Wirkung: (BZ-steigernd) Diazoxid, Thiazide, Kalziumblocker, ß-2-Sympathomimetika, Glukokortikoide, L-Thyroxin, etc.
- Details
- Kategorie: Orale Antidiabetika
- Zugriffe: 18735
→ Definition:
→ I: Bei den Sulfonylharnstoffen handelt es sich um eine Substanzgruppe von oralen Antidiabetika, die insbesondere zur Behandlung des Diabetes mellitus Typ II eingesetzt wird.Hierzu gehören insbesondere:
→ 1) Glibenclamid,
→ 2) Glimepirid und
→ 3) Gliclazid.
→ II: Sulfonylharnstoffe werden auch als Insulinsekretagoga (= Arzneimittel, die die Insulinsekretion fördern) bezeichnet. Hierzu gehören auch die Glinide.
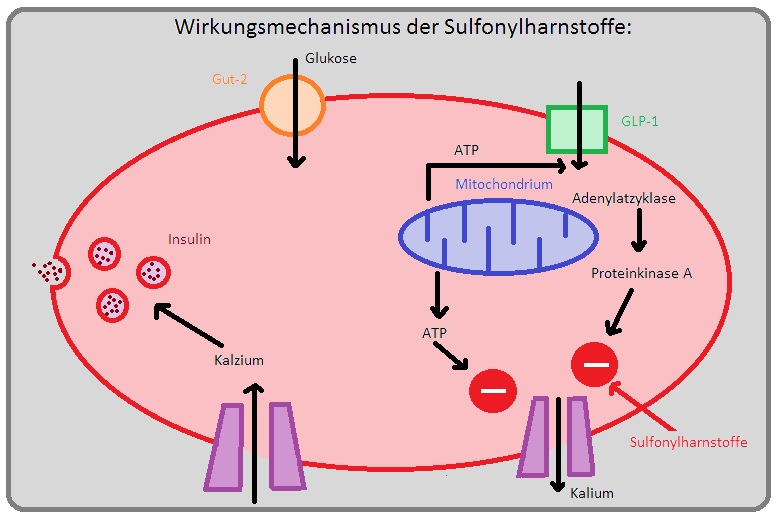
→ Wirkungsmechanismus: Die Wirkung der Sulfonylharnstoffe besteht im Wesentlichen in der Sensibilisierung der B-Zellen gegenüber physiologischen Inkretionsreizen.
→ I: Wichtige Voraussetzung für die blutzuckersenkende Wirkung ist das Vorhandensein von insulinproduzierenden B-Zellen. Sulfonylharnstoffe binden an die regulatorische Sulfonylharnstoff-Rezeptor-Untereinheit (SHR-1) der ATP-abhängigen K+-Kanäle der B-Zellen und verschließen diese. In der Folge werden spannungsabhängige Ca2+-Kanäle geöffnet und induzieren die Insulinausschüttung = Inkretion (siehe auch Glinide). Sie haben somit keinen Einfluss auf die Produktion von Insulin, sondern nur auf deren Freisetzung, sodass für die Therapie mit Sulfonylharnstoffen nachfolgende Vorrausetzungen gegeben sein müssen:
→ 1) Die Insulinproduktion besteht und
→ 2) Glukose und somit ATP ist als physiologischer Stimulus vorhanden.
→ II: Senkung des HbA1c um ca. 1%.
→ III: Sulfonylharnstoffe haben zusätzlich eine stimulierende Wirkung auf Somatostatin und eine hemmende auf Glukagon.
→ IV: Extrapankreatisch:
→ 1) Steigerung der Sensibilität der Insulinrezeptoren für Insulin,
→ 2) Verminderung der Down-Regulation der Insulin-Rezeptoren.
→ 3) Hemmung der hepatischen Glukoseproduktion.
→ Dosierung:
→ I: Glibenclamid:
→ 1) Beginnend mit einer Initialdosis von 1,75-3,5mg/d und schrittweise Steigerung über Tage bis Wochen bis zu einer mittleren Tagesdosis von 3,5-7,5mg/d (Maximaldosis 10,5mg/d), wobei morgens 2/3 und abends 1/3 der Gesamtdosis substituiert wird.
→ 2) Glibenclamid hat zusätzlich noch eine extrapankreatische Wirkung.
→ II: Glimepirid:
→ 1) Einschleichender Beginn mit einer Initialdosis von 1g/d, die mit einer Latenz von 1-2 Wochen gesteigert wird bis zu einer mittleren Tagesdosis von 1-4 mg/d (bis zu einer Maximaldosis von 6mg/d).
→ 2) Aufgrund seiner langen Wirkdauer wird es typischerweise nur 1x morgens verabreicht.
→ III: Gliclazid: Mittlere Tagesdosis 30-120mg/d.
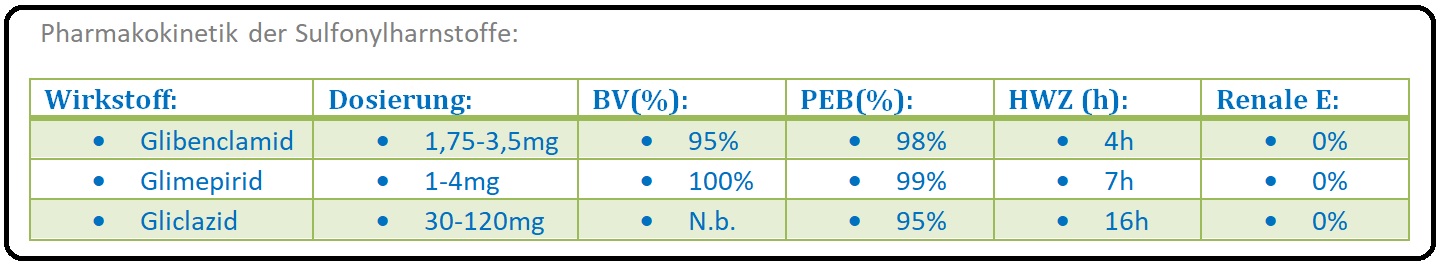
→ Pharmakokinetik:
→ I: Die Sulfonylharnstoffe werden nach orale Gabe gut resorbiert, im Plasma an Proteine gebunden, in der Leber über das Cytochrom-P-450-System (CYP2C9) metabolisiert und renal sowie biliär ausgeschieden.
→ II: Bei schwerer Leber- und Nierenschädigung besteht die Gefahr der Akkumulation mit konsekutiver Ausbildung schwerer Hypoglykämien.
→ III: Glibenclamid: Der optimale Wirkungseffekt wird bei Glibenclamid erst nach 5-7 Tagen erreicht; es hat eine Wirkungsdauer von 18-24 Stunden.
→ Indikation: Sie sind nur bei der Behandlung normalgewichtiger Patienten mit Diabetes mellitus Typ II (wenn eine unzureichende Blutzucker-Senkung trotz strikter Diät besteht) indiziert bzw. Kontraindikationen für Metformin existieren.
→ Nebenwirkungen:
→ I: Wichtige undhäufig auftretende Nebenwirkungen der Sulfonylharnstoffe sind insbesondere zum einen die Gewichtszunehme, zum anderen die Hypoglykämie.
→ II: Gastrointestinale Beschwerden mit Übelkeit, Erbrechen, Diarrhoe etc.
→ III: Allergische Hautreaktionen,
→ IV: Alkoholunverträglichkeit durch Hemmung der Aldehyddehydrogenase.
→ V: Sehr selten Blutbildveränderungen wie z.B. die hämolytische Anämie oder die lebensbedrohliche Agranulozytose.
→ Klinisch-relevant: Vor allem die Einnahme von Glibenclamid kann zu schweren Hypoglykämien führen, wenn u.a. ein erhöhter Glucoseverbrauch (schwere körperliche Arbeit) oder eine verminderte Glucoseaufnahme (Diät, Infekte) besteht.
→ Kontraindikationen: Wichtige Kontraindikationen sind u.a.:
→ I: Diabetes mellitus Typ I sowie diabetische Koma und Ketoazidose,
→ II: Schwere Leber- und Nierenerkrankungen,
→ III: Schwangerschaft und Stillzeit.
→ IV: Sulfonamid-Allergie.
→ V: Eine relative Kontraindikation stellt die Adipositas dar.
→ Wechselwirkungen: Wechselwirkungen werden durch Induktion bzw. Hemmung des Cytochrom-P-450-Systems (CYP2C9) erreicht:
→ I: Steigerung der Sulfonylharnstoff-Wirkung: Wird u.a. durch Alkohol, ASS, ß-Blocker, Cumarinderivate, MAO-Hemmer etc. hervorgerufen; Folge kann ein hypoglykämischer Schock mit tödlichem Ausgang sein.
→ II: Hemmung der Sulfonylharnstoff-Wirkung: ß-2-Sympathomimetika, Glukokortikoide, Thiazide, atypische Neuroleptika (Clozapin, Olanzapin) und nicht zuletzt durch L-Thyroxin.
→ Klinisch-relevant:
→ A) Kardiotoxische Wirkung der Sulfonylharnstoffe: Die Sulfonylharnstoffe agieren mit geringer Affinität auch an der SHR-2-Untereinheit der ATP-abhängigen K+-Kanäle der Kardiomyozyten. Durch Bindung an diese regulatorische Untereinheit wird der physiologische Zellschutz der Kardiomyozyten, nämlich die ischämisch bedingte Öffnung der ATP-abhängigen K+-Kanäle, die zu einer Hyperpolarisation und hierüber zu einem verminderten Ca2+-Einstrom bei hypoxischer Zellschädigung führt, unterbunden. Die genaue Bedeutung des Mechanismus ist jedoch noch nicht genau geklärt.
→ B) Sulfonylharnstoffversagen: Es entwickelt sich im Behandlungsverlauf eine Diabetes-Progression nach anfänglicher erfolgreicher Therapie aufgrund einer Erschöpfung der B-Zellen des Pankreas mit konsekutiver Verminderung der Insulinausschüttung.
→ C) Eine Kombinationstherapie mit Alpha-Glucosidase-Hemmern und Glitazonen ist möglich.