- Details
- Geschrieben von: CF
- Kategorie: Kolon und Rektum
- Zugriffe: 3247
→ Definition: Bei der (akuten) Appendizitis handelt es sich um eine (bakterielle) Entzündung der Appendix vermiformis am Zäkum.
→ Epidemiologie:
→ I: Die Appendizitis stellt die häufigste Ursache eines akuten Abdomens dar und etwa jeder 10. erkrankt in seinem Leben an dieser.
→ II: Der Manifestationsgipfel liegt zwischen dem 10.-30. Lebensjahr, wobei Männer 3mal häufiger als Frauen betroffen sind.
→ Ätiopathogenese: Nicht immer ist bei der Appendizitis die Ursache eruierbar.
→ I: In 60% der Fälle kommt es jedoch zu einer Obliteration des Appendixlumens durch z.B. eingedickten Stuhl (= Koprollithen), Fremdkörper, Parasiten (Askardien), Abknickungen, Adhäsionen, Narben, etc.
→ II: Die fortschreitende Sekretion der Mukosa und der fehlende Austausch mit dem Dickdarmlumen führt zu einem intraluminalen Druckanstieg, der den venösen Druck übersteigt und zur Hypoxie führt. Des Weiteren kommt es zur Überwucherung des Lumens mit Bakterien (z.B. Bacterioides fragilis, E. coli, etc.) und konsekutivem Eindringen in die Mukosawand. Durch die Infektion kommt es in der Regel innerhalb von 24-36 Stunden zur Ausbildung von einem Gangrän oder zu einer Perforation.
→ III: Der Zeitablauf ist aber auch sehr variabel und hängt insbesondere von der Lokalisation der Obstruktion ab; Verschlüsse im Bereich der Appendixspitze perforieren deutlich früher als an der Appendixbasis.
→ Klassifikation: Die Appendizitis kann nach dem histologischen Bild (abhängig vom Zeitraum) in verschiedene Stadien unterteilt werden:
→ Klinik:
→ I: Kurze Phase mit Inappetenz, Übelkeit und Erbrechen.
→ II: Das erste klinische Zeichen sind unklare kolikartige Schmerzen im Epigastrium, oder periumbilikal, die sich zumeist innerhalb einiger (4) Stunden in den rechten unteren Quadranten verlagern.
→ Klinisch-relevant: Charakteristisch ist der Symptomwechsel zwischen unbestimmten, schlecht lokalisierbaren viszeralen Oberbauchschmerzen und dem hellen scharf begrenzten somatischen Schmerz im rechten Unterbauch.
→ III: Weitere Symptome: Sind insbesondere:
→ 1) Abwehrspannung, Schmerzen beim Gehen und Schonhaltung durch Heben des rechten Beins bringt Entlastung.
→ 2) Fieber häufig nicht über 39°C.
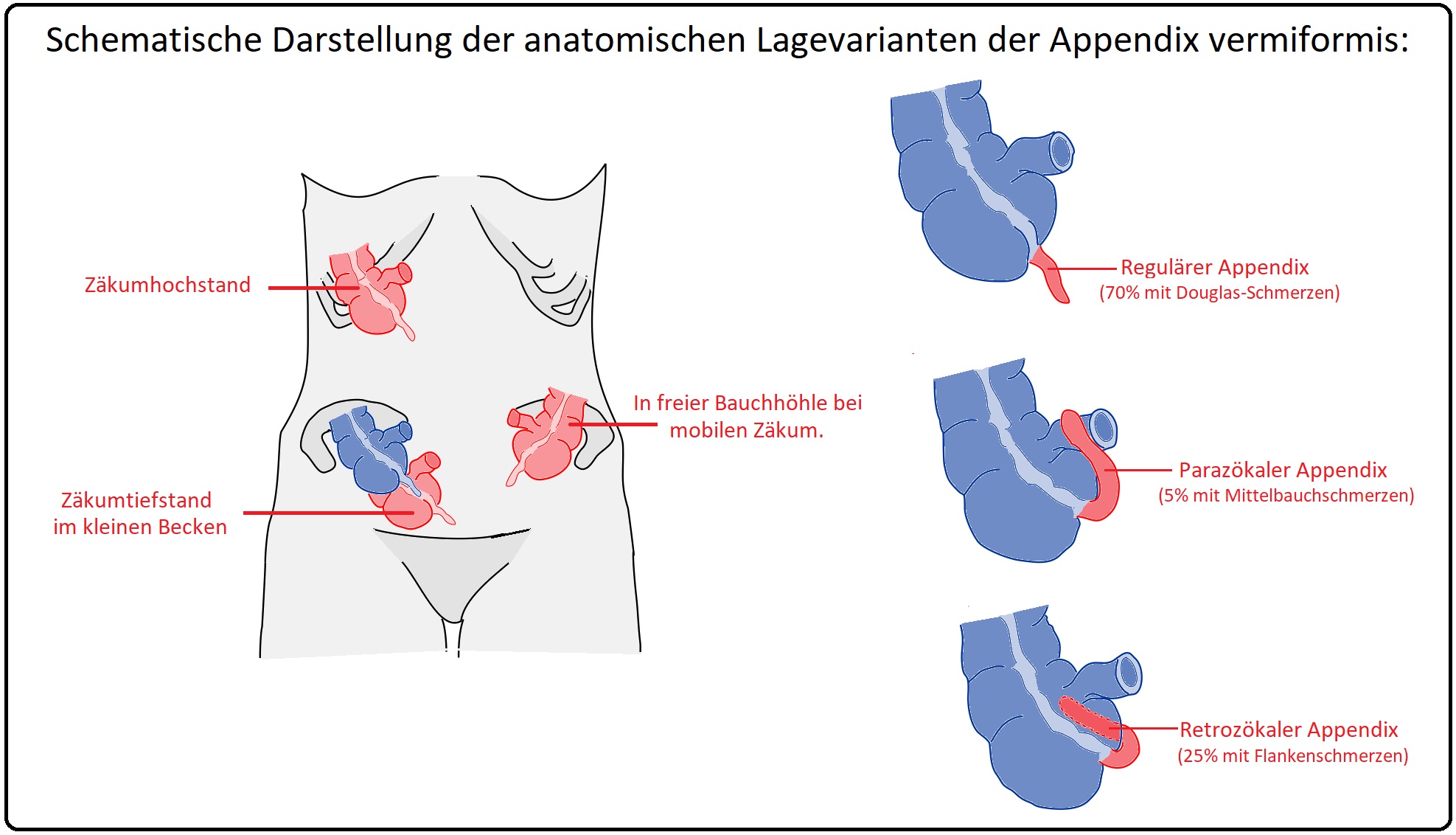
→ IV: Lagevarianten: Da das Mesoappendix den Wurmfortsatz nicht stark fixiert kann dieser in der Lage variieren.
→ 1) Die Appendix vermiformis kann sich in der Achse des Zäkums regulär oder ins kleine Becken fortsetzen, hinter das Zäkum (retrozäkal) ziehen oder nach medial zeigen (parazökal). Je nach Lage des Zäkums selbst (hoch, nach medial, tief) können sich weitere Varianten entwickeln.
→ 2) Klinisch Relevanz besteht dadurch, dass der Hauptschmerz in das jeweilige Dermatom projiziert wird, dessen parietales Peritoneum der Appendix am nächsten liegt.
→ 3) Beispiel: So verursacht ein retrozäkaler hochgeschlagener Appendix Rücken- bzw. Flankenschmerzen sowie eine Erythro- bzw. Leukozyturie (durch die Nähe zum rechten Ureter). Bei der Beckenappendizitis kommt es zumeist nach beginnenden Schmerzen im Epigastrium zu einer Verlagerung des Schmerzens linksseitig in das kleine Becken. Symptome sind hierbei u.a. Dysurie und Diarrhö.
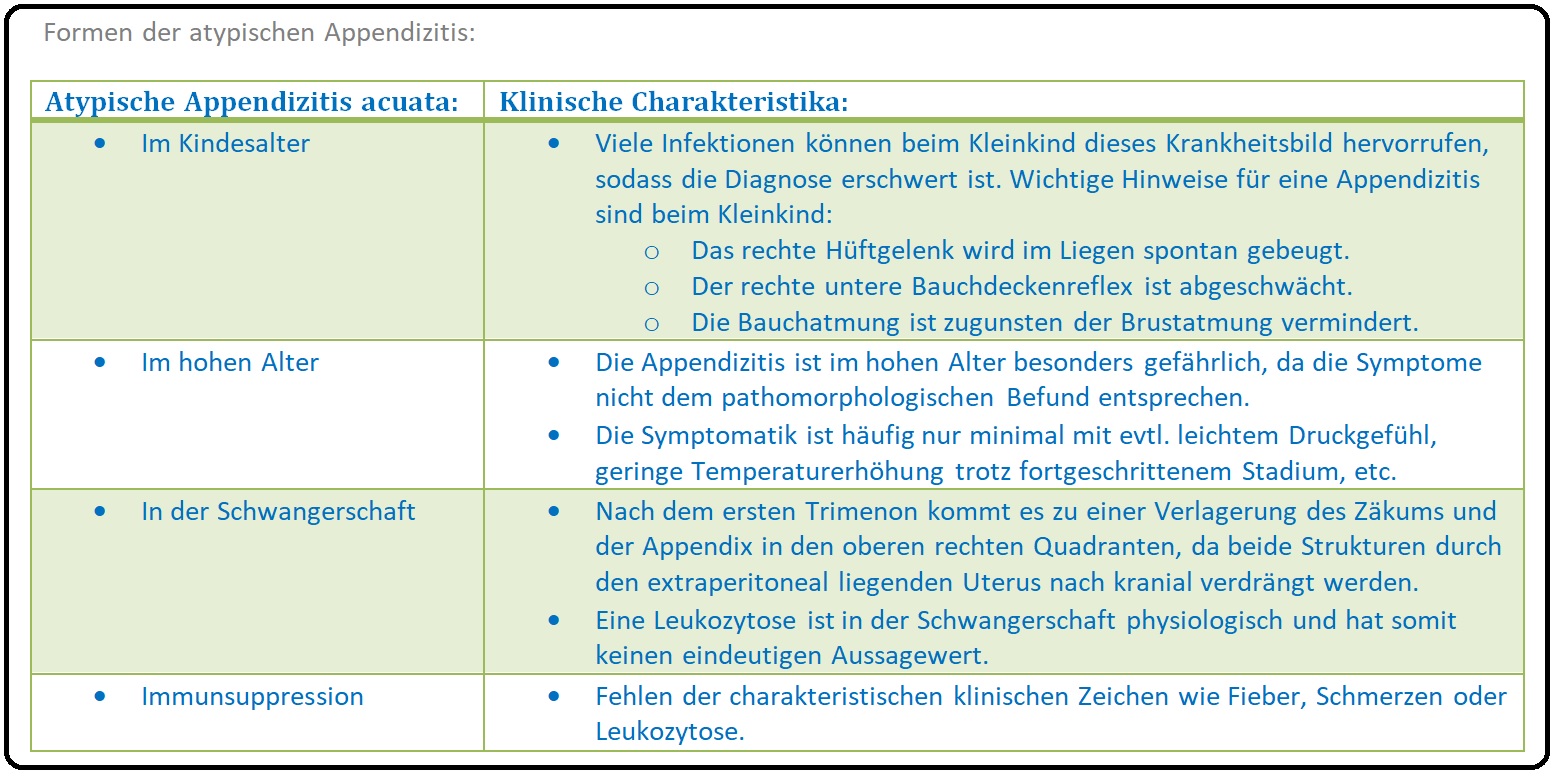
→ V: Atypische Appendizitis: Die akute Appendizitis kann aufgrund der Lage, des Patientenalters, bei bestehender Immunsuppression und während der Schwangerschaft einen atypischen Krankheitsverlauf aufweisen.
→ Komplikationen: Beinhalten zum eine die Hauptkomplikationen sowie das Übergreifen der entzündlichen Prozesse auf Nachbarorgane und -strukturen.
→ I: Hauptkomplikationen:
→ 1) Freie Perforation mit Entwicklung einer diffusen Peritonitis und
→ 2) Gedeckte Perforation mit möglicher Abkapselung.
→ II: Weitere Komplikationen: Sind u.a.:
→ 1) Perityphilitischer Abszess: Hierbei kommt es bei komplizierter Appendizitis zur einer örtlichen Abszedierung. Ursache ist überwiegend eine perforierte Appendizitis.
→ 2) Parakolische - und Douglas-Raum-, aber auch subphrenischer-, subhepatischer - und nicht zuletzt Psoasabszess, die nicht selten zu einer Sepsis führen können (intraabdominelle Abszesse).
→ 3) Pylephlebitis: Eine seltene fortgeschrittene Komplikation stellt die septische Phlebothrombose des Pfortadersystem (Pfortaderthrombose) mit hohem Fieber und Schüttelfrost dar.
→ Diagnose: Die Diagnose der akuten Appendizitis erfolgt fast ausschließlich anhand klinischer Gesichtspunkte (Anamnese, klinische Untersuchung, etc.)
→ I: Anamnese/klinische Untersuchung:
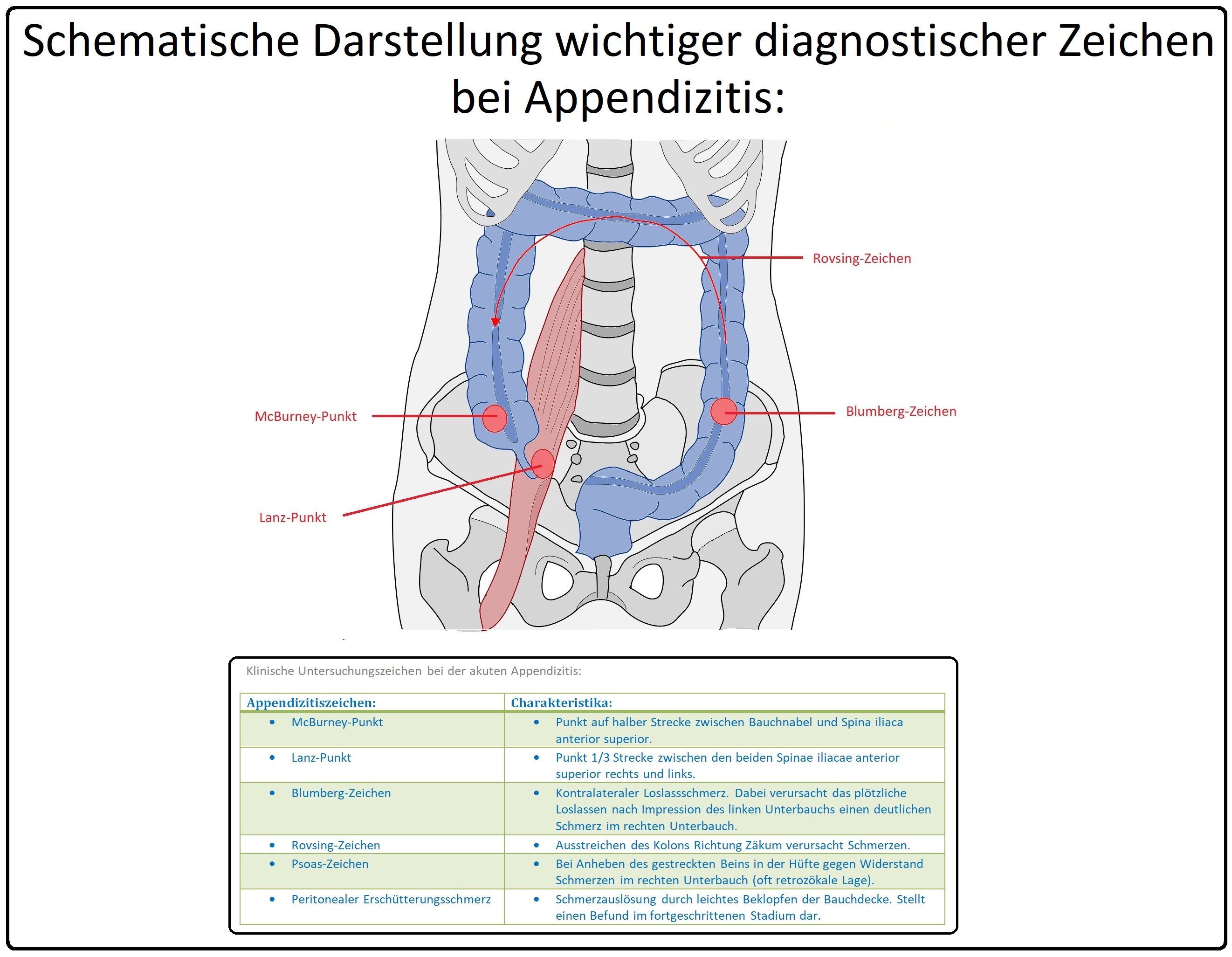
→ 1) Leitbefund ist der Druckschmerz im rechten Unterbauch mit punctum maximum im Bereich des McBurney oder Lanz Punkts. Typisch ist auch der Druckschmerz und die Abwehrspannung durch Reizung des parietalen Peritoneums. Des Weiteren gibt die Palpation Auskunft über mögliche Flüssigkeits- und Luftansammlungen.
→ 2) Die Aukultation dient insbesondere zum Ausschluss möglicher Differenzialdiagnosen wie Gastroenteritis (Infektion mit Viren, Bakterien z.B. Campylobacter jejuni, Yersinien, Listerien, etc.) mit Hyperperistaltik, mechanischer Ileus (klingelnde hoch gestellte Darmgeräusche), paralytischer Ileus oder Peritonitis mit Totenstille des Darms, etc.
→ 3) Bei Messung der Körpertemperatur leigt diese zumeist < 39°C (häufig besteht eine axillorektale Temperaturdifferenz von > 0,9°C).
→ II: Labor:
→ 1) Sehr Sensitiv ist die Erhöhung der Entzündungsparameter (BSG, CRP erhöht) insbesondere der Leukozytose, jedoch mit geringer Spezifität.
→ 2) In 25% der Fälle sind Erythrozyten und Leukozyten im Urin nachweisbar. Dies zeigt sich meist bei retrozökaler Lage unter entzündlicher Miteinbeziehung der Ureter und darf nicht von der Verdachtsdiagnose ablenken.
→ III: Sonographie: Charakteristische sonographische Zeichen einer Appendizitis sind insbesondere:
→ 1) Wandverdickung auf > 2mm.
→ 2) Evtl. sogenannte Target-Zeichen, auch Schießscheiben- oder Korkaden-Zeichen, die durch die ödematöse Schwellung der Wand entstehen.
→ 3) Vergrößerung des Gesamtdurchmessers auf > 6-7mm.
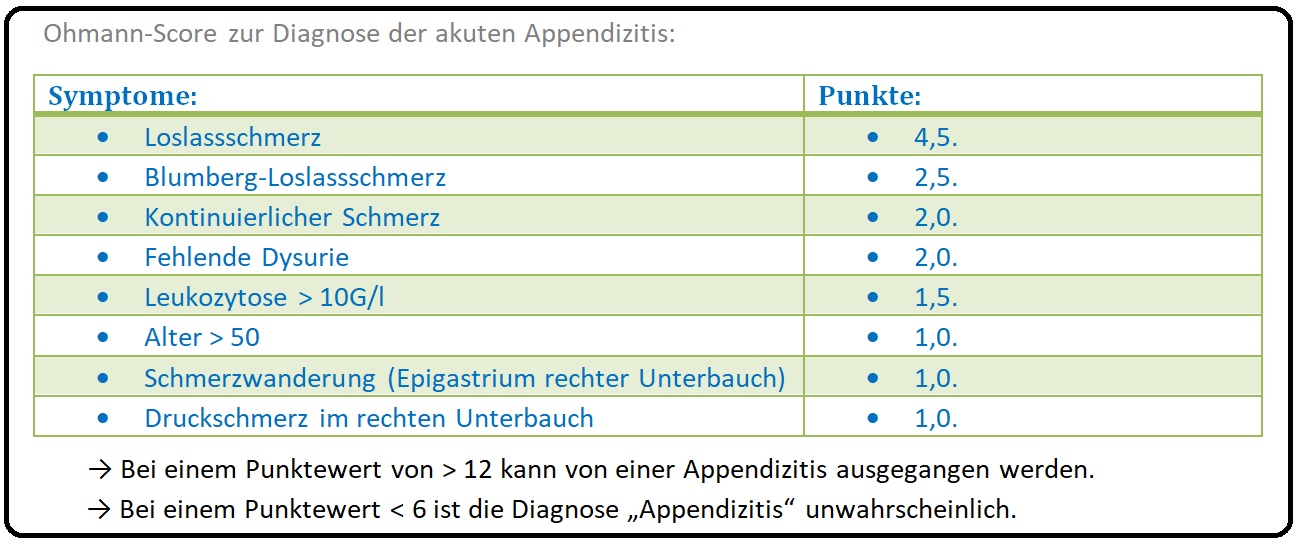
→ Klinisch-relevant: Für die akute Appendizitis hat sich der sogenannte Ohmann-Score als Diagnostikum etabliert und wird in einigen Zentren im Alltag als Routinegebrauch eingesetzt.
→ Differenzialdiagnose: Allgemein kann die akute Appendizitis jeden Zustand eines akuten Abdomens vortäuschen, sodass insbesondere nachfolgende Erkrankungen abgegrenzt werden müssen:
→ I: Gastrointestinal: Colon irrtabile, akute Gastroenteritis (z.B. Yersiniose, Infektion mit Campylobacter jejuni, Listeriose, etc.), Meckel-Divertikulitis, aber auch allgemein Divertikulitis, Morbus Crohn, Colitis ulcerosa, kolorektales Karzinom, perforierter Ulcus duodeni und - ventriculi, Pankreatitis, Cholezystitis, etc.
→ II: Urogenital: Wie Adnexitis, stielgedrehte Ovarialzysten, Corpusluteum (evtl. ruptiert), Extrauteringravidität, Uretersteine, Harnwegsinfekte (z.B. Zystitis, Pyelitis, Pyelonephritis, etc), etc.
→ III: Weitere Differenzialdiagnosen: Sind insbesondere ilioinguinales Syndrom, vertebragene Schmerzen, Lungenerkrankungen, Hinterwandinfarkt, Psoasabszess (intraabdominelle Abszesse), etc.
→ Therapie: Ziel der Behandlung ist die Behebung der Infektionsursachen und der damit verbundenen Komplikationen durch eine chirurgische Appendektomie, die laparoskopisch oder offen erfolgt.
→ I: Offene Appenektomie: (= Konventionelle Appendektomie):
→ 1) Die Laparotomie wird mittels Wechselschnitt (Eröffnung der Gewebeschichten entlang der Hautspalten und dem Faserverlauf) im rechten Unterbauch durchgeführt. Hierfür wird in der Regel die Aponeurose des M. obliquus externus abdominis in Faserrichtung gespalten und nach Eröffnung des Peritoneums die Appendix entlang der Tenia libera des Zäkums aufgesucht. Als nächstes werden die Gefäße (insbesondere die A. appendicularis aus der A. iliocolica) der Mesoappendix unterbunden und durchtrennt. Anschließend erfolgt die Ligatur der Appendixbasis und nach Abtragung des Wurmfortsatzes die Versenkung des Appendixstumpfes mit Hilfe einer Tabaksbeutel- oder Z-Naht. Letzter Schritt ist der schichtweise Verschluss der Bauchdecke.
→ 2) Eine erweiterte Operation ist erforderlich, wenn die Entzündung und Gewebedestruktion auf Nachbarstrukturen übergreift. Sie beinhaltet Abszesshöhlen zu drainieren und irreversibel geschädigte Gewebe zu entfernen, sodass z.B. eine Ileozäkalresektion mit anschließender Ileoaszendotomie indiziert sein kann.
→ 3) Ein weiterer wichtiger Schritt ist der intraoperative Ausschluss eines Meckel-Divertikels (Entzündung) im Bereich des Dünndarms. Exploriert wird dieser von der Bauhin´schen Klappe retrograd mit einem Abstand von 70-100cm.
→ II: Laparoskopische Appendektomie: Die Laparoskopie dient bei unklarem Abdomen sowohl der diagnostischen Abklärung als auch therapeutischen Intervention ohne große Traumatisierung. Nach Anlegen des Pneumoperitoneums wird umbilical sowie im rechten und linken Unterbauch ein Trokar eingebracht. Mesoappendix mit A. appendicularis werden mittels Elektrokoagulation oder Ligatur abgesetzt. Nach Erreichen der Appendixbasis erfolgt das Absetzten zwischen den Ligaturen oder nach Elektrokoagulation der Basis mittels Hochfrequenzstrom. Die Appendix wird anschließend mit dem Trokar im rechten Unterbauch geborgen.
→ Postoperative Komplikationen: Wichtige und zum Teil schwerwiegende Komplikationen nach Appendektomie sind u.a.:
→ I: Bauchdeckenabszess in 10-30% der Fälle.
→ II: Intraabdominelle Abszesse vor allem im Douglas-Raum und im kleinen Becken. In diesem Zusammenhang kann es durch Adhäsionsprozesse frühzeitig zu Darmpassagestörungen kommen.
→ III: Weitere Komplikationen: Sind insbesondere
→ 1) Protrahierte postoperative Darmparalyse vor allem bei eitriger Appendizitis und Peritonitis.
→ 2) Kotfistel gerade bei bestehender Stumpfinsuffizienz oder Morbus Crohn.
→ 3) Appendixstumpfinsuffizienz.
- Details
- Geschrieben von: CF
- Kategorie: Kolon und Rektum
- Zugriffe: 2338
→ Definition: Beim Peutz-Jeghers-Syndrom handelt es sich um eine autosomal-dominant vererbte heterogene Erkrankung, die durch das gleichzeitige Auftreten von multiplen Polypen im Gastrointestinatraktes (häufig auch Dünndarm) und mukokutanten durch Melanin induzierte Pigmentierungen auf Lippen, bukkal und perianal gekennzeichnet ist.
→ Epidemiologie:
→ I: Das Peutz-Jeghers-Syndrom stellt eine sehr seltene genetisch determinierte Erkrankung dar.
→ II: Sie weist in Deutschland ein eine Inzidenz von 1/100000 auf.
→ Ätiopathogenese:
→ I: Ursache ist eine Mutation des Landscaper-Gens STK-11(/LKB1) auf Chromosom 19p13.3. Dieses Gen kodiert die Serin-Threonin-Kinase, die insbesondere an der Regulation von Prozessen wie:
→ 1) Zellteilung,
→ 2) Zelldifferenzierung und
→ 3) Signaltransduktion beteiligt ist.
→ II: Neuere Studien zeigen, dass sich bei 20-40% der Fälle keine (positive) Familienanamnese erheben lässt, sodass man von Neumutationen ausgehen kann.
→ Klinik: Die Symptomatik des Peutz-Jeghers-Syndrom manifestiert sich zumeist schon in der ersten bis zweiten Lebensdekade mit:
→ I: Charakteristisch sind periorale, bukkale und gelegentlich perianale Pigmentierungen, die nicht selten im Kleinkindesalter auftreten und den intestinalen Phänomenen vorausgehen (sie verblassen häufig Erwachsenenalter).
→ II: Polypen: (= Polyposis generalisata)
→ 1) Die intestinalen Polypen können im gesamten Gastrointestinaltrakt auftreten, sind aber vornehmlich im Dünndarm (abnehmende Häufigkeit von Jejunum > Ileum > zu Duodenum), aber auch im Kolon (bzw. Rektum), seltener im Magen nachweisbar.
→ 2) Kleinere Polypen sind breitbasig, größere gestielt.
→ 3) Insbesondere die gestielten Polypen neigen zur Torsion und Invagination mit Blut im Stuhl, oberen und unteren gastrointestinalen Blutungen und Eisenmangelanämie,.
→ III: Weitere Symptome: Sind u.a. Diarrhö, aber auch kolikartige abdominelle Schmerzen, Ileus-Symptomatik (durch Obstruktion und Invagination) bis hin zum akuten Abdomen.
→ IV: Manifestation von Keimleistentumoren, die hormonell aktiv sein können:
→ 1) Bei jungen Mädchen können sie zu einer Pubertas praecox,
→ 2) Bei Jungen Pseudopubertas praecox und Gynäkomastie führen.
→ Klinisch-relevant: Etwa 30% der Betroffenen werden im ersten Lebensjahrzehnt symptomatisch, 60% in der zweiten Lebensdekade. Die simultane kutane und gastrointestinale Manifestation ist keinesfalls oblgat.
→ Komplikation: Eine wichtige und schwerwiegende Komplikation beim dieser Erkrankung ist das erhöhte Karzinomrisiko insbesondere für:
→ I: Kolorektales Karzinom, Magen-, Gallenblasen- und Pankreaskarzinom, aber auch Tumoren im Bereich der Papilla Vateri (Papillentumoren), etc.
→ II: Extraintestinale Tumoren von Ovar, Zervix, Mamma und Hoden.
→ Diagnose:
→ I: Anamnese/klinische Untersuchung: Mit Familienanamnese und Inspektion der Lippen und Wangenschleimhaut.
→ II: Endoskopische Untersuchungen mittels Ösophagogastroduodenoskopie, Koloskopie sowie Kapselendoskopie.
→ III: Histologie: Histologisch sind die harmatomatösen Peutz-Jeghers-Polypen durch eine ausgeprägte sich baumartig aufzweigende und fein verästelte Lamina muscularis mucosae gekennzeichnet und hierüber auch von weiteren polypösen Erkrankungen gut abgrenzbar.
→ Klinisch-relevant: Aufgrund des erhöhten Entartungsrisikos werden ab den 10. Lebensjahr endoskopische Kontrolluntersuchungen des oberen und
unteren Gastrointestinaltraktes mit konsekutiver Polypektomie in 2-jährigen Abständen empfohlen.
→ Differenzialdiagnose: Vom Peutz-Jeghers-Syndrom müssen insbesondere nachfolgende Erkrankungen abgegrenzt werden:
→ I: Akutes Abdomen anderer Genese (z.B. Divertikulitis, etc.).
→ II: Kolorektales Karzinom.
→ III: Polyposis anderer Genese wie z.B. die familiäre juvenile Polyposis, familiäre adenomatöse Polyposis, etc.
→ IV: Weitere Differenzialdiagnose: Sind u.a.:
→ 1) Gastrointestinale Blutungen (z.B. bei Ulcus ventriculi, Ulcus duodeni) Invaginationen, Infarzierungen anderer Genese.
→ 2) Hyperpigmentierung der Mundschleimhaut bei z.B. Morbus Addison, Hämochromatose, medikamenteninduziert (z.B. Retrovir), etc.
→ V: Tuberöse Sklerose: Hierbei handelt es sich um eine genetische Erkrankung, charakterisiert durch Adenoma sebaceum, geistiger Retardierung und Epilepsie. Zudem neigen die Patienten zu Harmatomen in den verschiedenen Organen. Dazu zählen intestinale Polypen vom Peutz-Jeghers-Typ, die sich im Schulalter entwickeln. Später im Erwachsenenalter auftretene Polypen sind vom adenomatösen Typ.
→ Therapie: Eine kausale Therapie beim Peutz-Jeghers-Syndrom existiert bis heute nicht, vielmehr erfolgt sie symptomatisch.
→ I: Regelmäßige Untersuchungen mit Polypektomie blutungsgefährdender oder malignomverdächtiger Polypen.
→ II: Zudem regelmäßige gynäkologische Kontrollen.
→ III: Im Rahmen eines akuten Abdomens muss die Laparatomie mit möglicher Teilresektion von infarzierten Darmabschnitten ins Auge gefasst werden.
- Details
- Geschrieben von: CF
- Kategorie: Kolon und Rektum
- Zugriffe: 3542
→ Definition: Beim kolorektalen Karzinom handelt es sich um eine sporadisch oder hereditär auftretende maligne Neoplasie, die zumeist von der Dickdarmschleimhaut ausgeht (Adenokarzinom). Nach der Lokalisation wird differenziert zwischen einem:
→ I: Rektum-Ca: Bei einer Distanz von 16cm abanal spricht man von einem Rektumkarzinom,
→ II: Kolon.Ca: Darüber hinaus von einem Kolonkarzinom.
→ Epidemiologie:
→ I: Das kolorektale Karzinom ist eines der häufigsten Karzinome in der westlichen Welt. Bei Frauen ist es nach dem Mamma-Karzinom das 2.- bei Männern nach dem Bronchial- und Prostatakarzinom das 3.-häufigste Malignom.
→ II: Männer sind etwas häufiger als Frauen betroffen, wobei der Manifestationsgipfel in der 6.-7- Lebensdekade liegt.
→ III: Ein früheres Auftreten des kolorektalen Karzinoms in der Adoleszenz (20. Lebensjahr) weist auf eine hereditäre Form z.B. familiäre Adenomatosen hin.
→ Ätiopathogenese:
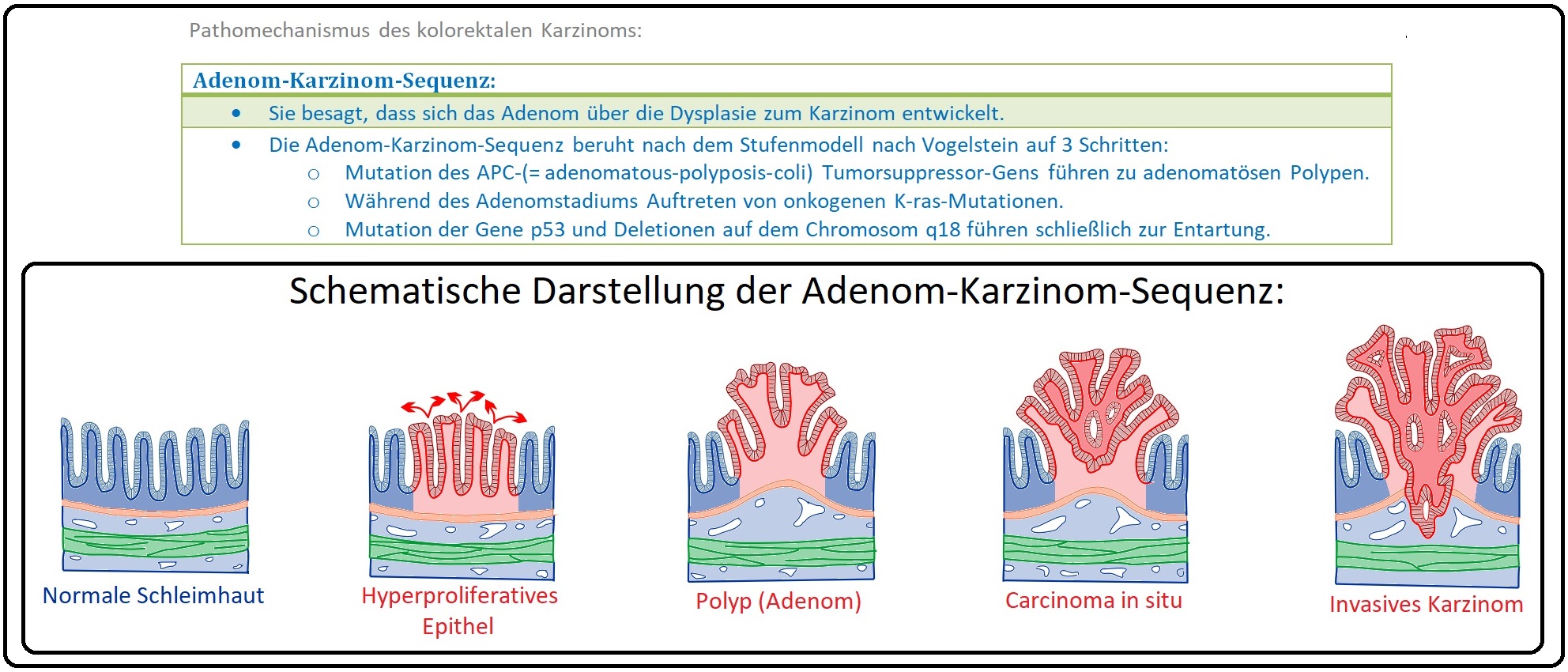
→ I: Fast alle kolorektale Karzinome (> 95% der Fälle) entwickeln auf dem Boden eines kolorektalen Adenoms im Sinne der Adenom-Dysplasie-Karzinom-Sequenz.
→ II: Die weiteren 5% sind überwiegend auf genetische Faktoren zurückzuführen (vor allem die familiären Formen werden autosomal-dominant vererbt). Hierzu zählen insbesondere:
→ 1) Dickdarmkarzinome in der Familienanamnese,
→ 2) Hereditäres kolorektales Karzinom ohne Polyposis (= HNPCC),
→ 3) Familiäre adenomatöse Polyposis (= FAP) sowie
→ 4) Intestinale Polyposis-Syndrome wie die familiäre juvenile Polyposis und das Peutz-Jeghers-Syndrom, etc.
→ III: Weitere Risikofaktoren: Für die Entwicklung eines kolorektalen Karzinoms sind u.a.:
→ 1) Chronisch-entzündliche Darmerkrankungen z.B. Morbus Crohn und v.a. Colitis ulcerosa,
→ 2) Höheres Lebensalter und tierische Nahrungsfette sowie zu wenig Ballaststoffe,
→ 3) BMI > 25 und mangelnde körperliche Bewegung, Rauchen, etc.
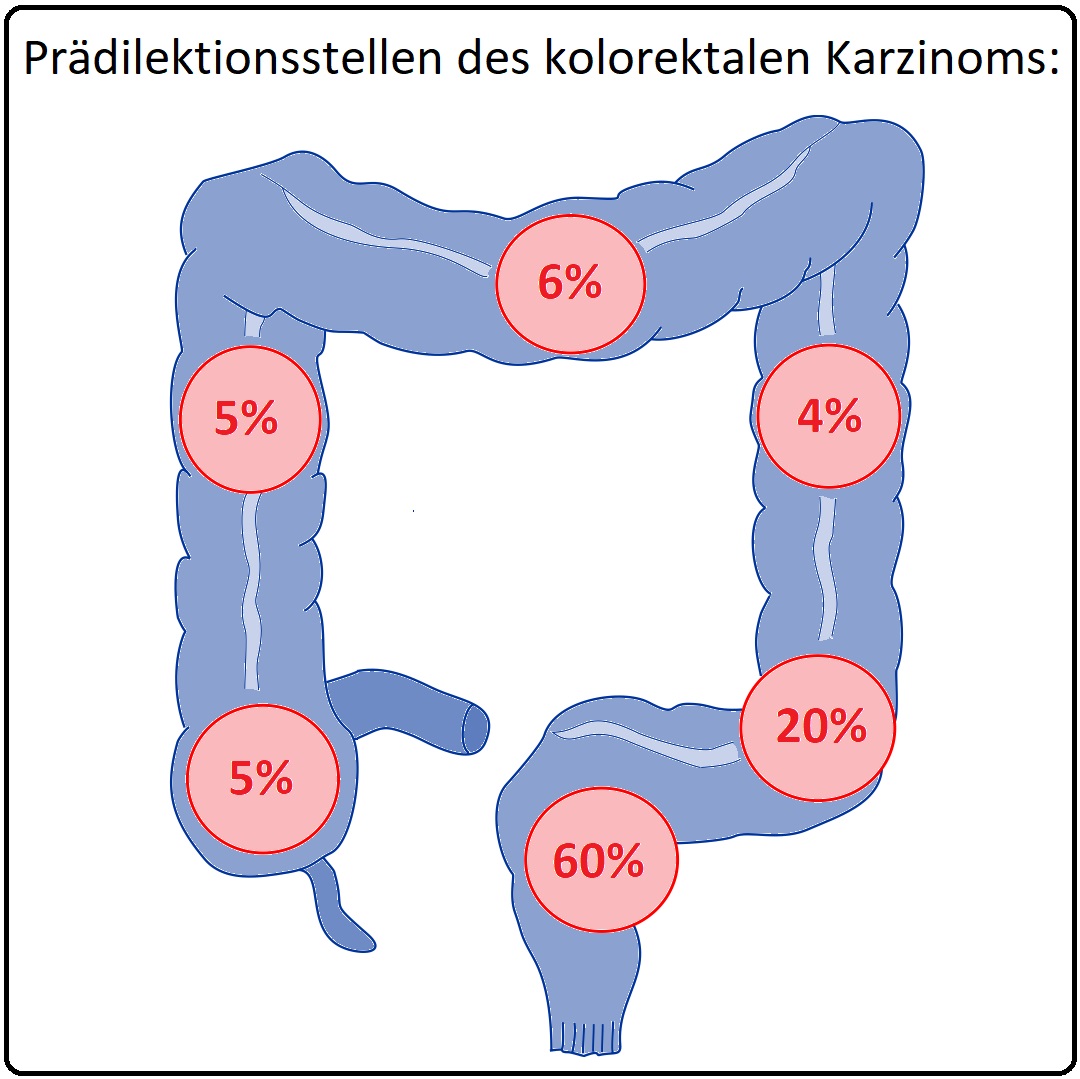
→ Lokalisation:
→ I: 60% der kolorektalen Karzinome sind im Rektum, 20% im Sigma, 10% im Zäkum bzw. Colon ascendens und weitere 10% im restlichen Kolon lokalisiert.
→ II: Es kann zudem nochmals unterschieden werden zwischen:
→ 1) Synchrones Vorkommen: Es besteht gleichzeitig ein Zweittumor; manifestiert sich in 3-5% der Fälle.
→ 2) Metachrones Vorkommen: Neues, nicht an der Anastomose auftretendes kolorektales Karzinom; frühsten 6 Monate nach Resektion des Primärtumor; manifestiert sich in 1-3% der sporadischen Form.
→ Pathologie:
→ I: Das Adenokarzinom stellt mit > 80% der Fälle die häufigste Form. Weitere seltene Typen sind u.a. muzinöses Adenokarzinom (10%), Plattenepithel-, Siegelringzell-, adenosquamöses -, kleinzelliges und undifferenziertes Karzinom (2%).
→ II: Makroskopisches Wachstum: Beim kolorektalen Karzinom werden nach der Wachstumsform verschiedene Typen differenziert:
→ 1) Ulzerierter Tumor exkaviert.
→ 2) Sessil polypoider Tumor, nodulär oder läppchenförmig.
→ 3) Anulärer, stenosierender Tumor und
→ 4) Flach-prominenter Tumor.
→ III: Malignitätsgrade: (= Grading) Hier unterscheidet man zwischen gut differenziert (G1), mäßiggradig differenziert (G2), schlecht differenziert (G3, Siegelringzell-Karzinom ist immer G3) und G4, die undifferenzierte bzw. kleinzellige Form. Nach WHO sind:
→ 1) G1 und G2 „low-grade“- sowie
→ 2) G3 und G4 „ high-grade“ -Karzinome.
→ Metastasierung: Initial erfolgt das Tumorwachstum zumeist polypoid in Richtung Darmlumen. Zusätzlich kann es gleichzeitig zum infiltrativen Wachstum
in die Muscularis propria und in die Serosa kommen. Im weiteren erfolgt die Ausbreitung:
→ I: Lymphogene Metastasierung: Das Kolonkarzinom metastasiert in die lokoregionären Lymphknoten (später auch in die mesenterialen Lymphknoten entlang derarteriellen Gefäße); die lymphogene Ausbreitung des Rektumkarzinoms erfolgt je nach Lokalisation über 3 Wege; die Prognose des Rektumkarzinoms ist umso ungünstiger je tiefer es (von der Anokutanlinie betrachtet) sitzt:
→ 1) Hoch-sitzend: (8-16cm) Metastasieren in die paraaortalen Lymphknoten (1. Metastasenstraße).
→ 2) Mittlere Etage: (4-8cm) Zusätzlich im Bereich der Beckenwand (2. Metastasenstraße).
→ 3) Tief-sitzend: (0-4cm) Zusätzlich noch die inguinalen Lymphknoten (3. Metastasenstraße).
→ II: Hämatogene Metastasierung: Erfolgt initial über die Vena portae in die Leber, anschließend in Lunge und Skelett.
→ III: Selten (per continuitatem) als z.B. lokale Fisteln in Nachbarorgane.
→ Klinik: Die klinischen Beschwerden treten überwiegend im fortgeschrittenen Stadium auf, da der Tumor nur sehr langsam wächst und für Jahre klinisch stumm bleibt. Die Symptomatik ist zumeist sehr uncharakteristisch und variiert abhängig von der Lokalisation des Tumors.
→ I: Allgemeinsymptome: Mit Gewichtsverlust, Müdigkeit, Abgeschlagenheit und Leistungsminderung sowie evtl. Fieber (aufgrund von Nekrosen und Lokalinfektionen).
→ II: Leibesschmerzen und wechselnde Stuhlgewohnheiten (Änderungen der Stuhlgewohnheiten mit einer Dauer von mehr als 3 Wochen).
→ III: Blutauflagerungen (= Hämatochezie) und Meläna (evtl. auch okkult).
→ IV: Entwicklung einer hypochromen mikrozytären Anämie (Eisenmangelanämie).
→ Komplikationen: Wichtige und z.T. schwerwiegende Komplikationen beim kolorektalen Karzinom sind insbesondere:
→ I: Lumenobstruktion mit der Ausbildung eines mechanischen (Sub-) Ileus.
→ II: Infektionen und mögliche Entwicklung einer Bakteriämie mit Streptococcus bovis oder einer Clostridium-septicum-Sepsis.
→ III: Darmperforation mit konsekutiver Peritonitis.
→ Diagnose:
→ I: Anamnese/Klinische Untersuchung:
→ 1) Umfangreiche Eigen- und Familienanamnese, einschließlich der Erfassung von Lebensstil und Vorerkrankungen, etc.
→ 2) Bei der körperlichen Untersuchung stehen die rektal-digitale Austastung (es lassen sich über diese Untersuchung bis zu 25% der Rektumkarzinome eruieren) sowie der Hämokulttest (ist durch das intermittierende Blutungsverhalten des Karzinoms in bis zu 50% falsch negativ) im Vordergrund.
→ II: Diagnostischer Goldstandard des kolorektalen Karzinoms stellt die komplette Koloskopie des Dickdarms mit Biopsie dar. Ist sie aufgrund z.B. möglicher Stenosen nicht möglich, kommen CT- und MR-Kolonographie (= virtuelle Endoskopie) zum Einsatz.
→ III: Staging: Beim Tumor-staging stehen die Erfassung von Lebermetastasen und Lungen- (v.a. Rektumkarzinom) mittels Sonographie, Röntgen-Thorax und CT im Vordergrund.
→ III: Labor: Die Tumormarker CEA und Ca19-9 sind zur Diagnosestellung weniger spezifisch, korrelieren aber mit der Tumormasse und dienen insbesondere der postoperativen Verlaufskontrolle (bei kompletter Tumorresektion R0 normalisieren sich die präoperativ erhöhten Werte und steigen bei Rezidiven erneut an).
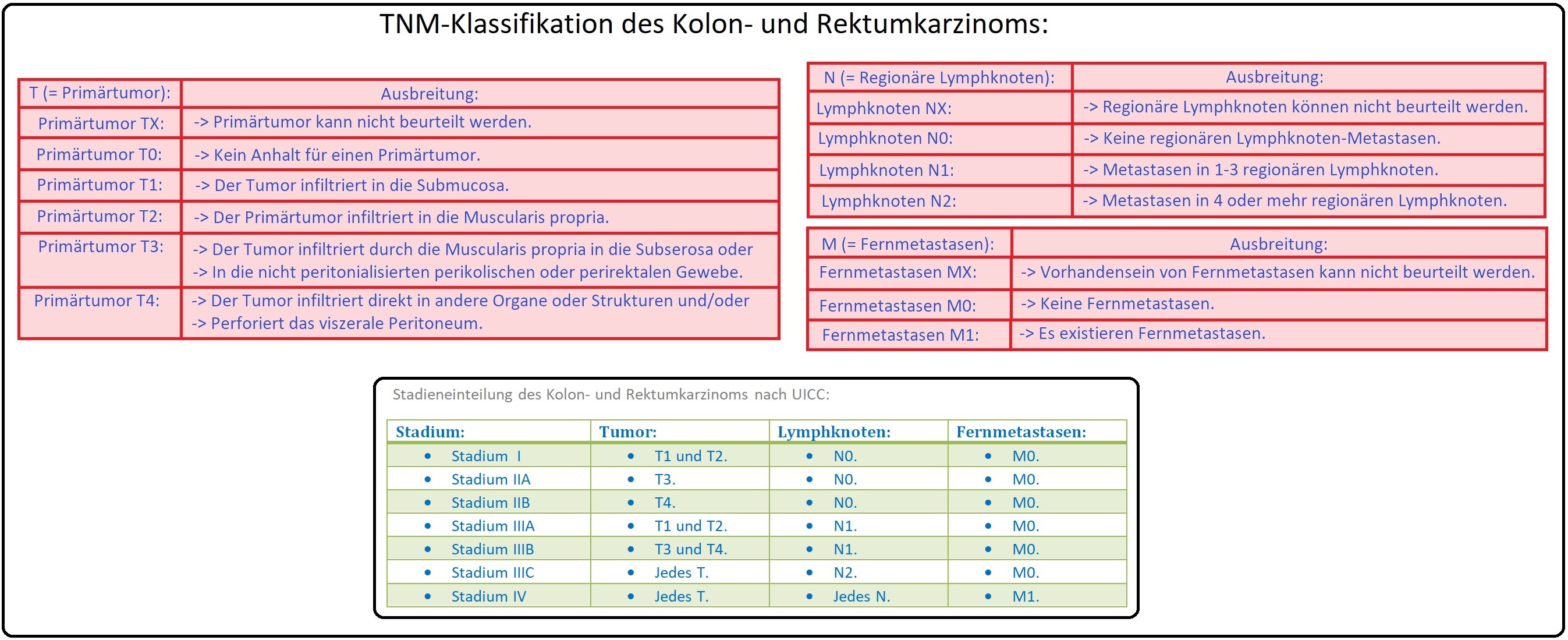
→ Klassifikation:
→ I: Die Einteilung des Kolon- und Rektumkarzinom erfolgt (UICC) mit Hilfe der TNM-Klassifikation:
→ II: Eine weitere Klassifikation erfolgt nach Dukes kommt aus dem angloamerikanischen Sprachraum und findet heutzutage kaum (keine) Anwendung mehr. Sie beinhaltet:
→ 1) Dukes A: Das Karzinom infiltriert in Mukosa (T1) und Submucosa (T2).
→ 2) Dukes B: Es kommt zum Befall des perikolischen bzw. perirektalen Fettgewebes (T3/T4).
→ 4) Dukes C: Es manifestieren sich Lymphknotenmetastasen (N1/N2) zum einen im Bereich der regionären Lymphknoten (C1) oder der paraaortalen Lymphknoten (C2).
→ 5) Dukes D: Es bestehen Fernmetastasen (z.B. Lebermetastasen).
→ Differenzialdiagnose: Vom kolorektalen Karzinom müssen insbesondere nachfolgende Erkrankungen abgegrenzt werden:
→ I: Hämorrhoiden (peranaler Blutabgang),
→ II: Divertikulose und Divertikulitis.
→ III: Chronisch entzündliche Darmerkrankungen insbesondere Morbus Crohn und Colitis ulcerosa, aber auch die ischämische Kolitis.
→ IV: Weitere maligne Neoplasien wie wie Lymphome, neuroendokrine Karzinome oder sehr selten GIST.
→ V: Weitere Differenzialdiagnosen: Sind insbesondere Colon irritabile, Angiektasien, Endometriose, benigne Strikturen, etc.
→ Therapie: Ziel der Behandlung ist die operative R0-Resektion (=kurativ) mit konsekutiver Entfernung des Primärtumors, einschließlich regionaler Lymphknoten und evtl. isolierter Metastasen (Leber, Lungen).
→ I: Operative Therapie: Die Resektion erfolgt in No-Touch-Technik mit Ligatur der zu- und abführenden Gefäße. Nach der Lokalisation des Primärtumors werden unterschiedliche Verfahren angewandt:
→ 1) Rektumkarzinom: Bei Malignomen im oberen und mittleren Drittel erfolgt eine En-Bloc-Entfernung als anteriore sphinktererhaltende Rektumresektion. Bei Tumoren im unteren Drittel (bei denen der Sicherheitsabstand < 3cm) ist eine abdominoperineale Rektumexirpation mit Anlage eines Kolostomas, als sogenannte Hartmann-Operation, indiziert.
→ 2) Kolonkarzinom: Auch hier wird eine En-bloc-Resektion je nach Lokalisation im Sinne einer rechten oder linken Hemikolektomie bzw. einer Transversumresektion durchgeführt (siehe auch chirurgische Therapie des kolorektalen Karzinoms).
→ II: Adjuvante Therapie: Die adjuvante Chemotherapie ist im Stadium II und III eindeutig indiziert. Sie wird auch als palliative Behandlung in R2-Situationen oder bei Metastasierung empfohlen. Die besten Ergebnisse weist das FOLFOX-Schema (Oxaliplatin + 5-Fluoruracil/Folinsäure) beim Kolonkarzinom. Beim Rektumkarzinom wird als Standard eine kombinierte Radiochemotherapie als adjuvante Behandlung (insbesondere wenn keine neoadjuvante Radiochemotherapie erfolgt ist) durchgeführt.
→ III: Palliativmaßnahmen: Sie umfassen u.a.:
→ 1) Unter Palliativ-Operation werden Eingriffe verstanden, bei denen durch das fortgeschrittene Tumorstadium Reste der Malignome belassen werden. Durch diese Resektion wird versucht zum einen Komplikationen zu beseitigen, zum anderen die Lebenserwartung des Patienten zu verlängern.
→ 2) Umgehungsanastomosen, endoskopische (Metall-) Stenteinlage und Anlage eines Anus praeter.
→ 3) Weitere palliative Interventionen sind insbesondere die Lasertherapie, Argon-Plasma-Koagulation oder die Elektrotherapie.
→ Nachsorge: Regelmäßige standardisierte Nachsorgeuntersuchungen zur Früherkennung von Rezidiven und Metastasen sind obligat und umfassen:
→ Prognose:
→ I: Die Prognose ist insbesondere von folgenden Faktoren abhängig:
→ 1) Stadium des kolorektalen Karzinoms, das vor allem durch die Infiltrationstiefe, Lymphknotenbefall, Organbefall nach der TNM-Klassifikation eingeteilt wird.
→ 2) Nach dem Differenzierungsgrad (G) und dem histologischen Typus, die das biologische Verhalten des Tumors bestimmt.
→ 3) Gerade beim Rektumkarzinom ist die Höhenlokalisation aufgrund verschiedener Metastasierungswege und der direkten Ausbreitung (= per continuitatem) von besonderer Bedeutung.
→ II: Die 5-Jahresüberlebensrate nach radikaler R0-Resektion konnte auf bis zu 70% gesteigert werden. Hierbei fallen auf das Tumorstadium T1 90-100%, Stadium T2 70-85% und das Stadium T3 50-70%.
→ III: Der große Anteil der Tumorrezidive wird innerhalb der ersten 18 Monate nach Ersteingriff diagnostiziert (nur selten treten sie in den ersten 3 Jahren auf).
→ Prophylaxe: Zur Früherkennung existiert für die Nichtrisiko-Patienten eine sogenannte Vorsorge-Untersuchung als fäkaler Okkult-Bluttest (bei Frauen ab dem 35. Lebensjahr, bei Männer ab dem 45. Lebensjahr) bzw. eine Früherkennungskoloskopie. Bei Risikopatienten (hereditäre Form) sind die Vorsorgeuntersuchungen deutlich früher angelegt.
- Details
- Kategorie: Kolon und Rektum
- Zugriffe: 11183
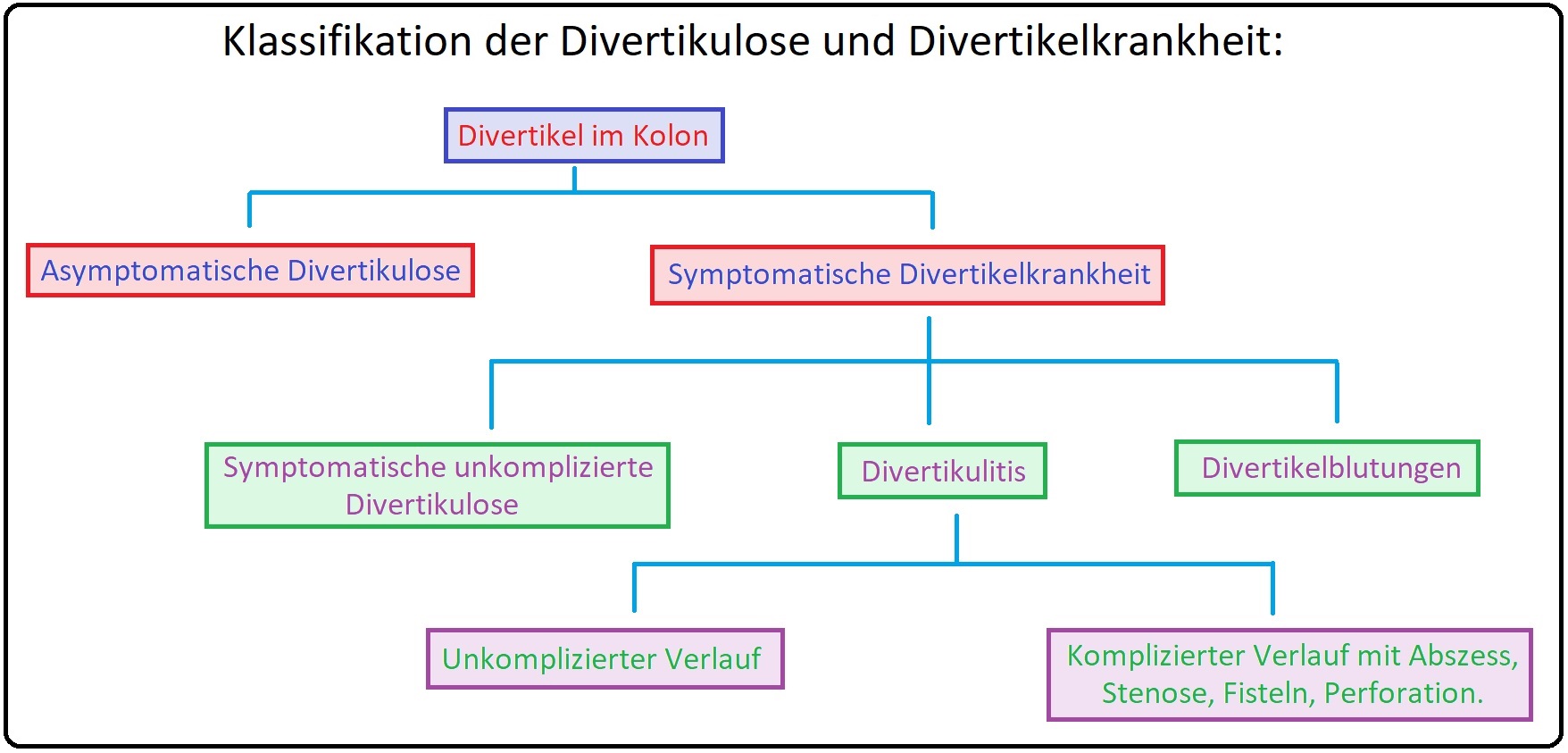
→ Definition: Die Divertikulitis ist definiert als eine Entzündung bzw. Infektion eines oder mehrer mit z.T. Darminhalt gefüllten Divertikel.
→ Epidemiologie: Die Divertikulitis stellt die häufigste Komplikation der Divertikulose dar. Etwa 15-25% aller Divertikelträger bilden im Krankheitsverlauf eine Divertikulitis aus; mit zunehmendem Alter steigt die Inzidenz; so weisen Patienten zwischen dem 65.-70. Lebensjahr eine Prävalenz von 238/100000, bei den über 85. Jährigen 631/100000 auf.
→ Ätiopathogenese:
→ I: Ursache ist ein Stuhlaufstau im Bereich des Divertikelhalses mit konsekutiver Bakterienvermehrung und anschließenden Entzündungsprozessen.
→ II: Je nach Ausmaß der Entzündung unterscheidet man zwischen:
→ III: Wichtige Risikofaktoren, die eine Divertikulitis triggern sind u.a.:
→ 1) Höheres Lebensalter,
→ 2) Obstipation,
→ 3) Bewegungsarmut,
→ 4) Fettreiche, ballaststoffarme Kost etc.
→ IV: Lokalisation: Divertikel können im gesamten Kolon vorkommen, jedoch sind sie in > 95% der Fälle im Colon sigmoideum, in 1% im Colon transversum und in je 2% im Zökum bzw. Colon ascendens lokalisiert.
→ Klinik:
→ I: Meist akut auftretende Schmerzen im linken Unterbauch (= Linksappendizitis), die z.T. in den Rücken ausstrahlen.
→ II: Tastbare druckschmerzhafte Walze des Sigmas, evtl. umschriebener Peritonismus.
→ III: Tenesmen und Flatulenz.
→ IV: Stuhlunregelmäßigkeiten von Diarrhoe bis Obstipation.
→ V: Weitere Symptome: Sind u.a. Übelkeit, Erbrechen, subfebrile Temperaturen bis hin zu hohem Fieber, Schleim- und Blutbeimengungen im Stuhl, aber auch Stuhlverhalten.
→ VI: Bei chronischem Krankheitsverlauf kann es zur narbigen Schrumpfung des Sigmas mit zunehmender Stenosesymptomatik kommen.
→ Komplikationen:
→ I: Gedeckte Perforation, die sich durch den Austritt von Kontrastmittel im CT bzw. den Erregernachweis im Abszesspunktat eruieren lässt.
→ II: Abszessbildung (intraabdominelle Abszesse) oftmals in den retroperitonealen Raum (Douglas-Raum) sowie Leberabszesse.
→ III: Fistelbildung in die Harnblase im Bereich der Blasenhinterwand mit rezidivierenden Harnwegsinfekten (z.B. Zystitis, Pyelonephritis, etc.), Pneumaturie und Fäkalurie sowie in die Scheide, Dünndarm und Haut.
→ IV: Frei Perforation mit konsekutiver kotiger Peritonitis (Nachweis von freier Luft).
→ V: Sekundäre Stenosen bei chronischer Divertikulitis infolge entzündlicher Prozesse der Darmwand und narbiger Strikturen (narbiger Schrumpfung) mit der Gefahr der mechanischen Ileus-Entwicklung. Retroperitoneale Entzündungen können die Harnleiter miteinbeziehen und zur Dysurie und Ureterstenosen führen.
→ VI: Divertikelblutungen: Bei bis zu 15% der Fälle können sich massive therapiebedürftige Blutungen ausbilden.
→ Diagnose:
→ I: Anamnese/Klinische Untersuchung: Lokalisierte Abwehrspannung, durchschmerzhafte Walze des Sigmas sowie eine ausgeprägte Druckschmerzhaftigkeit des Douglas-Raums bei der rektalen Palpation.
→ II: Labor:
→ 1) Leukozytose, BSG- und CRP-Erhöhung.
→ 2) Urin: Leukozyten- und Erythrozyten-Nachweis bei Blasenbeteiligung.
→ III: Bildgebende Verfahren:
→ 1) Sonographie: Nachweis der Divertikel, evtl. Targetzeichen (= schießscheibenähnlicher Kolonquerschnitt im Bereich der wandverdickten Segmente), evtl. Nachweis eines Douglasabszesses.
→ 2) Röntgen Abdomen:
→ A) Leeraufnahme (in Linksseitenlage oder im Stehen) mit Darstellung von freier Luft im Abdomen oder retroperitoneal bzw. von Spiegelbildungen bei bestehendem Ileus.
→ B) Kolonkontrastmittelaufnahme: Mit Barium zur Abschätzung der Ausdehnung der Entzündung. Des Weiteren können Stenosen, Fistelbildungen, intraabdominelle Abszesse nachgewiesen werden.
→ Klinisch-relevant: Bei Verdacht auf eine Perforation ist die Gabe von Barium kontraindiziert, da es eine schwer behandelbare Barium-Peritonitis auslösen kann. In diesem Fall erfolgt die Applikation eines wasserlöslichen Kontrastmittels (z.B. Gastrografin).
→ 3) CT/MRT: Stellt das sicherste Verfahren zur Diagnose der Divertikulitis (Stadieneinteilung) und ihrer Komplikationen dar.
→ IV: Koloskopie: Es sollte im akuten Stadium aufgrund der Perforationsgefahr darauf verzichtet werden; dient jedoch zusätzlich der Erkennung von pathologischen Veränderungen wie Polypen oder einem Kolonkarzinom.
→ Klassifikation: Man unterscheidet hinsichtlich der Klinik und Diagnose nach Hansen und Stock verschiedene Stadien der Divertikulitis:
→ Differenzialdiagnose: Von der Divertikulitis sind u.a. anchfolgende Erkrankungen abzugrenzen:
→ I: Chronisch entzündliche Darmerkrankungen wie die Colitis ulcerosa, aber vor allem auch der Morbus Crohn.
→ II: Reizdarm-Syndrom und Appendizitis sowie
→ III: Kolonkarzinom.
→ IV: Weitere Erkrankungen: Sind u.a.:
→ 1) Gynäkologische wie die extrauterine Schwangerschaft, Adnexitis, etc.
→ 2) Harnwegsinfektionen und Nierenerkrankungen wie die akute Pyelonephritis, Pyonephrose, etc.
→ Therapie:
→ I: Konservative Therapie: Gerade beim ersten Schub einer unkomplizierten Divertikulitis sollte eine konservative Behandlung erfolgen. Hierzu gehören:
→ 1) Nahrungskarenz,
→ 2) Parenterale Flüssigkeitszufuhr und Analgetika-Therapie,
→ 3) Gabe eines Breitband-Antibiotikums wie Metronidazol + Ciprofloxacin (alternativ Piperacillin + Tazobactam) mit Abdeckung der Anaerobia und gram-negativen Bakterien.
→ 4) Größere Abzesse können mittels CT oder sonographisch unter Anlage einer Drainage abgeleitet werden.
→ II: Operative Therapie: Eine operative Indikation besteht u.a. bei:
→ 1) Rezidivierender Divertikulitis (> 3-7 Schübe, elektiv OP),
→ 2) Freier Perforation mit/ohne begleitender Peritonitis (Notfall-OP),
→ 3) Massive Blutungen (Notfall-OP),
→ 4) Ileus (Notfall-OP),
→ 5) Intraabdominelle Abszess- und Stenosebildung (dringliche OP),
→ 6) Fistelbildung in Blase, Vagina und Bauchdecke (dringliche OP), sowie
→ 7) Gedeckte Perforation (dringliche OP).
→ III: Verfahren:
→ 1) Rektosigmoidresektion laparoskopisch oder offen mit End-zu-End-Anastomose.
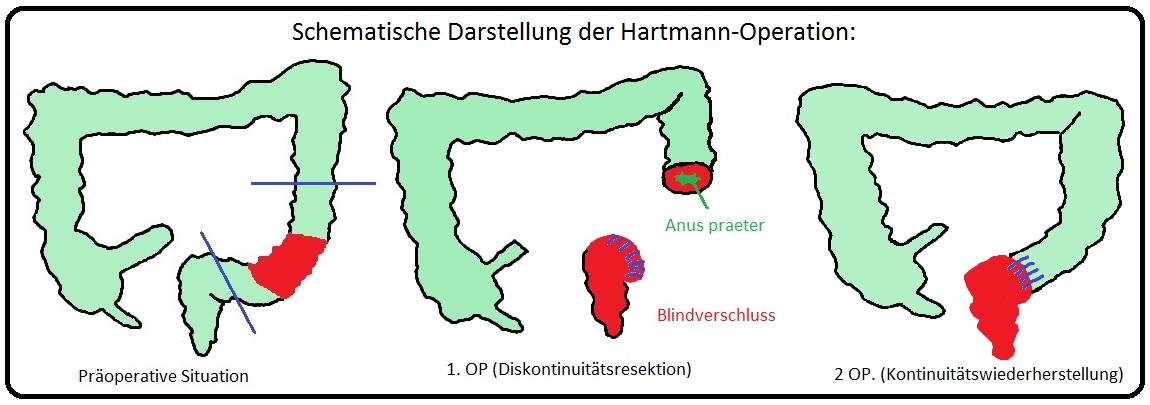
→ 2) Bei der freien Perforation mit kotiger Peritonitis erfolgt die OP nach Hartmann. Es handelt sich um eine zweizeitige Operation:
→ A) Erste Sitzung: Diskontinuitätsresektion (= Rektosigmoidresektion) mit Blindverschluss des Rektums und Anlage eines Anus praeter des Colon descendens. Zudem ist eine umfangreiche Lavage der Peritonealhöhle indiziert.
→ B) Zweite Sitzung: Rückverlagerung des Anus praeter und Reanastomosierung durch eine Deszendorektostomie. Diese erfolgt zumeist erst nach 12-16 Wochen.
→ Prognose: Bei der Elektiv-Operation liegt die Letalität < 1%; gerade bei einer freien Perforation mit kotiger Peritonitis ist die Sterblichkeit deutlich höher (> 50%).
- Details
- Kategorie: Kolon und Rektum
- Zugriffe: 7513
→ Definition: Bei der Divertikulose handelt es sich um multiple Ausstülpungen der Darmwand des Intestinaltraktes. Man unterscheidet hierbei zwischen:
→ I: Echten Divertikeln: Sie stellen Ausstülpungen aller Darmwandschichten (Mukosa, Muskularis, Serosa) dar, sind kongenital angelegt, treten zumeist solitär auf und sind deutlich seltener; echte Divertikel sind insbesondere im Zaekum und Colon ascendens lokalisiert.
→ II: Falschen Divertikeln: (= Pseudodivertikel) Es handelt sich um erworbene Ausstülpungen der Darmmukosa und Submucosa durch Lücken in der Tunica muscularis. Sie treten überwiegend multipel auf und sind bevorzugt im linken Hemikolon lokalisiert.
→ III: Meckel-Divertikel: Er repräsentiert einen echten Divertikel und ist ein Rudiment des Ductus omphaloentericus, ca. 90cm proximal der Ileozökalklappe.
→ Epidemiologie: Die Inzidenz für eine Divertikulose nimmt mit dem Alter zu. Während sie sich bei den > 50. Jährigen in 5% der Fälle manifestiert, liegt sie bei den > 80. Jährigen bei > 70% vor. Männer und Frauen sind gleich häufig betroffen (wobei in jüngeren Jahren die Männer im höheren Lebensalter die Frauen etwas dominieren).
→ Ätiopathognese: Bei der Divertikulose handelt es sich um eine Zivilisationskrankheit, die insbesondere durch die Ernährungsgewohnheiten (v.a. zu wenig Ballaststoffe) der westlichen Welt gefördert wird.
→ I: Ursache ist eine vermehrte Muskelkontraktur (Spasmus), gerade der intestinalen Längsmuskulatur (Tänien), bei ballaststoffarmer (faserarmer) Ernährung.
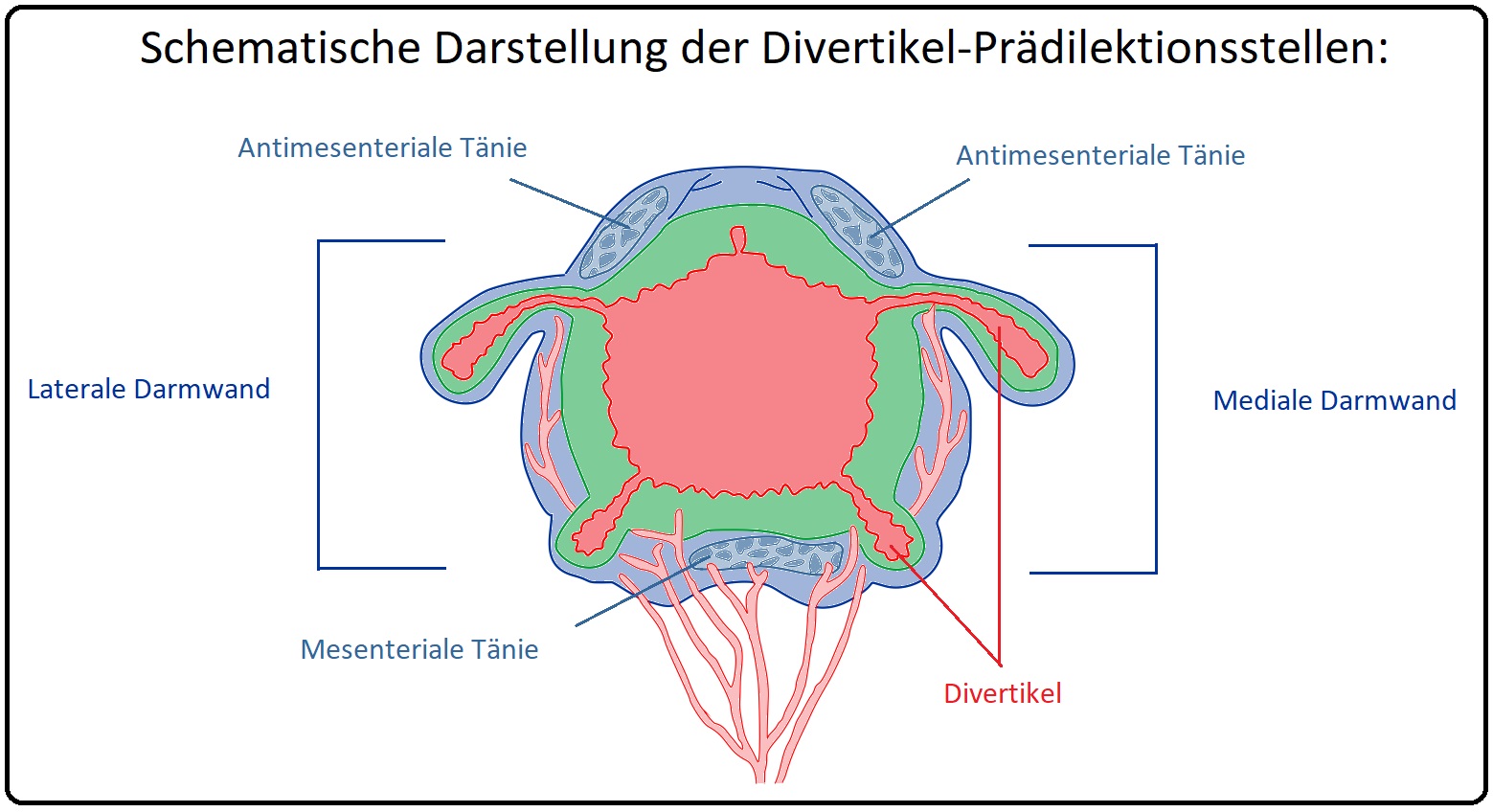
→ II: Durch den erhöhten intraluminalen (intrakolischen) Druck kommt es im höheren Lebensalter infolge eines Darmwandelastizitätsverlustes (generelle Bindegewebsschwäche) zum Schleimhautprolaps, insbesondere im Bereich muskulärer Schwachstellen, an den Durchtrittsstellen der mesenterialen Gefäße.
→ III: Risikofaktoren: Für die Entwicklung einer Divertikulose sind u.a.:
→ 1) Höheres Lebensalter infolge einer altersbedingten Abnahme des elastischen Bindegwebes.
→ 2) Adipositas mit Aufweitung der Gefäßkanäle durch Fetteinlagerung.
→ 3) Ausgeprägter transmuraler Druckgradient zwischen Darmlumen und Bauchhöhle.
→ 4) Ballaststoffarme Kost und chronische Obstipation verantworlich.
→ IV: Nach ihrer Morphologie unterscheidet man zwischen:
→ 1) Inkompletten Divertikeln: (= intramurale Divertikel) Hierbei liegen die Divertikel auf Darmwandniveau und sind von außen nicht erkennbar.
→ 2) Kompletten Divertikeln: (= transmurale Divertikel) Die Divertikel stülpen sich über die Darmwand hinaus, d.h. sie überschreiten die Ringmuskelschicht nach außen.
→ V: Lokalisation: Die Divertikulose kann in allen Darmabschnitten auftreten, ist jedoch in > 90% im Bereich des Colon sigmoideum lokalisiert.
→ Klinik: Nicht selten bleibt die Divertikulose ein lebenlang symptomlos (nur 20-30% zeigen klinisch-relevante Komplikationen wie Divertikulitis, Stenosen, Blutungen oder Perforation).
→ I: Die unkomplizierte Divertikulose verläuft in > 80% klinisch asymptomatisch.
→ II: Selten zeigen sich unspezifische Symptome wie intermittierende, krampfartige Schmerzen im linken Unterbauch nach Nahrungsaufnahme oder klinische Zeichen eines Reizdarm-Syndroms.
→ III: Weitere Symptome: Sind u.a. wechselnde Stuhlkonsistenz mit Phasen der Diarrhoe und Obstipation, Völlegefühl, Blähungsbeschwerden, etc.
→ IV: Die Saint-Trias ist charakterisiert durch das gleichzeitige Auftreten von:
→ 1) Divertikulose,
→ 2) Cholelithiasis und
→ 3) Axialer Hiatushernie.
→ Komplikationen: Charakteristische Komplikationen sind:
→ I: Blutungen (= untere gastrointestinale Blutung durch Ruptur eines arteriosklerotisch veränderten Gefäßes; bildet sich in 10-30% der Fälle aus; sind häufig selbstlimitierend),
→ II: Spontane Perforation insbesondere beim Zäkumdivertikel.
→ III: Divertikulitis,
→ IV: Malassimilationssyndrom bei Fehlbesiedlung bestehender Dünndarmdivertikel.
→ V: Papillenstenose und Pankreatitis bei peripapillären Duodenaldivertikeln.
→ Diagnose:
→ I: Meist handelt es sich um einen Zufallsbefund im Rahmen einer Koloskopie.
→ II: Guter endoskopischer Nachweis der Divertikelausführungsgänge; begleitender Ausschluss eines Kolonkarzinoms.
→ III: Röntgen-Kontrastmittel: Darstellung der mit Kontrastmittel-gefüllten Divertikel.
→ Therapie: Im Vordergrund der Divertikulose-Behandlung steht die Veränderung der Lebensgewohnheiten
→ I: Allgemeinmaßnahmen:
→ 1) Ernährungsumstellung auf ballaststoffreiche Kost mit z.B. Leinsamen, Weizenkleie etc.
→ 2) Ausreichende Flüssigkeitszufuhr,
→ 3) Stuhlregulation evtl. mit kolloidalen Laxanzien.
→ 4) Bei bakterieller Fehlbesiedlung antibiotische Therapie.
→ II: Operative Therapie: Bei Rezidivblutungen oder nicht-beherrschbaren Blutungen ist eine operative Behandlung durchzuführen:
→ 1) Ist die Blutung lokalisiert, erfolgt eine Segmentresektion mit anschließender End-zu-End-Anastomose.
→ 2) Bei massiven, nicht-lokalisierbaren (diffusen) Blutungen kann eine notfallmäßige, subtotale Kolektomie mit ileorektaler Anastomose indiziert sein. Selten muss ein endständiger Ileostoma mit Rektumblinverschluss durchgeführt werden.