- Details
- Geschrieben von: CF
- Kategorie: Antiarrhythmika
- Zugriffe: 13738
→ Definition:
→ I: Bei den Klasse-III-Antiarrhythmika handelt es sich um Kalium-Kanal-Blocker, deren Hauptvertreter Sotalol, Amiodaron und Dronedaron sind.
→ II: Sie blockieren die spannungsabhängigen Kalium-Kanäle des Arbeitsmyokards (= hERG-Kanal) und verhindern somit den Kalium-Ausstrom während der Repolarisationphase (= Phase 3 des AP im Myokard).
→ III: Folgen sind vor allem eine Verlängerung sowohl der Aktionspotenzialdauer als auch der Refraktärperiode.
→ Klinisch-relevant: Der hERG-Kanal stellt einen spannungsaktivierten, einwärtsgleich-richtenden Kalium-Kanal der Kardiomyozyten dar. Er induziert die Phase 3 (= Repolarisationsphase) des AP im Arbeitsmyokard und besteht aus 4 Untereinheiten, die jeweils über 6 Transmembranproteine verfügen. Die genetische Anlage für den hERG-Kanal liegt auf Chromosom 7. Strukturelle Anomalien in diesem speziellen Kanal können zu lebensbedrohlichen Herzrhythmusstörungen wie z.B. das Long-QT-Syndrom mit Verlängerung der QT-Dauer führen.
→ Wirkung: Antiarrhythmika der Klasse III verlängern die Dauer des Aktionspotenzials (Abb.: Wirkung der Antiarrhythmika auf das Aktionspotenzial) durch Hemmung des repolarisierenden Kalium-Auswärtsstroms in der Phase 2 und 3 des AK; dies geht einher mit der Zunahme der Refraktärzeit (Verlängerung der QT-Zeit im Oberflächen-EKG). Die Wirkung der Kaliumkanal-Blocker ist bei langsamer Herzfrequenz deutlich stärker als bei schneller und sie entwickeln sie in erster Linie auf atrialer Ebene.
→ Indikation: Wichtige Einsatzgebiete der Klasse-III-Antiarrhythmika sind insbesondere:
→ I: Schwere therapierefraktäre supraventrikuläre Tachykardien.
→ II: Medikamentöse Kardioversion bei bestehendem Vorhofflimmern.
→ III: Schwere ventrikuläre Tachykardien sowie
→ IV: Rhythmusstörungen mit linsventrikulärer systolischer Dysfunktion.
→ Klinisch-relevant:
→ A) Bei der Therapie des Vorhofflimmerns sind beide Substanzen zur Wiederherstellung des Sinusrhythmus gleichermaßen wirksam.
→ B) Zur Rezidivprophylaxe ist das Amiodaron jedoch dem Sotalol deutlich überlegen.
→ Nebenwirkungen:
→ I: Kardiale Nebenwirkungen: Sind insbesondere:
→ 1) Sinusbradykardie sowie sinusatriale und atrioventrikuläre Überleitungsstörungen.
→ 2) Im Vordergrund der kardialen unerwünschten Wirkungen steht die dosisabhängige Verlängerung des AP und QT-Intervalls. Hierdurch nimmt das Risiko für die Entwicklung ventrikulärer Extrasystolen und einer Torsades-de-pointes-Tachykardie (EKG-Befund: Torsades-de-pointes-Tachykardie) deutlich zu.
→ 3) Insbesondere die Hypokalämie stellt einen prädisponierenden Faktor für Herzrhythmusstörungen dar. Ursache ist u.a. die Einnahme von:
→ A) Laxanzien,
→ C) Schleifendiuretika und
→ D) Glukokortikoiden.
→ II: Extrakardiale NW: Sind u.a.:
→ 1) Gastrointestinale Beschwerden, Anstieg der Transaminasen, Arzneimittel-Hepatitis, hepatische Cholestase, selten Leberzirrhose.
→ 2) Neurologische Symptome: Mit Kopfschmerzen, Tremor, peripherer Neuropathie, Dyskinesien und Ataxie.
→ 3) Weitere Symptome: Sind Amiodaron-Keratopathie, Schilddrüsenfunktionsstörungen, Photosensibilität, Hautreaktionen etc.
→ Klinisch-relevant: Sotalol und Amiodaron:
→ A) Verstärken die negativ chronotrope und negativ bathmotrope Wirkung der Beta-Blocker, Herzglykosiden und des Verapamils und
→ B) Steigern die blutdrucksenkende Wirkung vieler Antihypertensiva.
→ Kontraindikationen: Die Behandlung mit Antiarrhythmika der Kasse III birgt einige wichtige Kontraindikationen. Hierzu zählen:
→ I: Sinusbradykardie,
→ II: Sick-Sinus-Syndrom,
→ III: Long-QT-Syndrom,
→ IV: Kombinationstherapie mit Digitalis oder Beta-Blockern,
→ V: Hypokaliämie und die
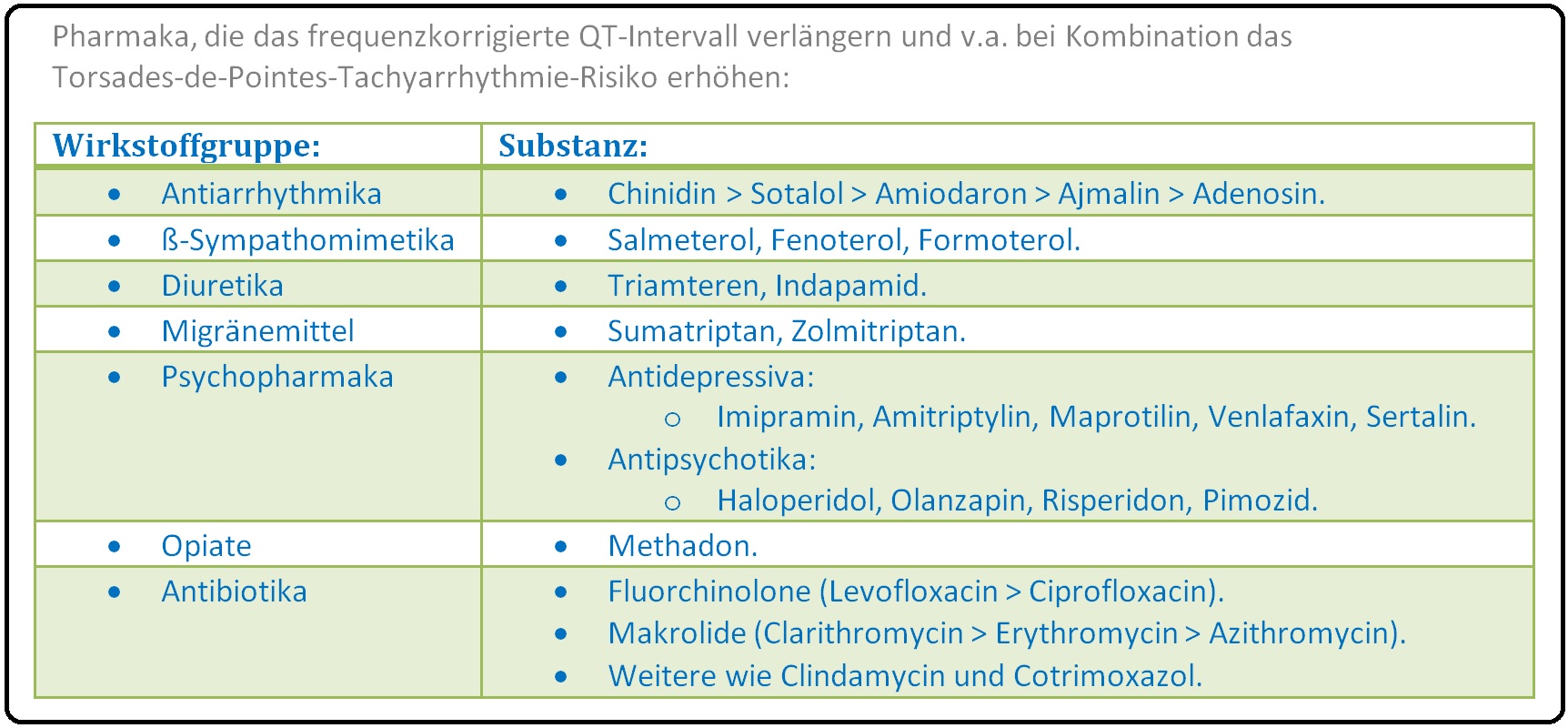
→ VI: Gleichzeitige Behandlung mit Pharmaka, die das QT-Intervall verlängern. Hierzu gehören:
- Details
- Geschrieben von: CF
- Kategorie: Antiarrhythmika
- Zugriffe: 8692
→ Definition: Bei Propafenon handelt es sich um ein Antiarrhythmika der Klasse I c, welches insbesondere in der Behandlung von supraventrikuären und ventrikuläre Tachykardie eingesetzt wird.
→ Wirkungsmechanismus:
→ I: Es hemmt die spannungsabhängigen Natrium+-Kanäle, vermindert hierüber die Leitungsgeschwindigkeit in allen Herzabschnitten (Vorhof, Ventrikel und Erregungsleitungssystem) gleichermaßen und verlängert hierüber die Depolarisationsphase. Die Repolarisationsphase wird kaum beeinflusst.
→ II: Propafenon weist auch geringe ß-blockierende (= negativ chronotrop) und Calzium-antagonisierende Eigenschaften auf.
→ III: Ein anticholinerger Effekt wie bei den Klasse-Ia Antirrhythmika (Chinidin, Ajmalin) besteht nicht.
→ IV: Es hat kaum Einfluss auf die QT-Zeit.
→ Indikation:
→ I: Supraventrikuläre Tachykardien, einschließlich der Präexzitationssyndrome (WPW-Syndrom).
→ II: (Paroxymales) Vorhofflimmern,
→ III: Ventrikuläre Tachykardien,
→ IV: Fokale atriale Tachykardie.
→ Pharmakokinetik:
→ I: Propafenon wird nach oraler Einnahme gut enteral resorbiert und zu 90% an Plasmaprotein gebunden. Die Bioverfügbarkeit liegt jedoch nur bei 50%, da es präsystemisch in der Leber über das Cytochrom P-450-System (CYP 2D6 Monooxygenase) metabolisiert wird.
→ II: Die HWZ beträgt 3-6 Stunden und es wird vorwiegend hepatisch ausgeschieden; Bei Leberinsuffizienz besteht immer Kumulationsgefahr.
→ Klinisch-relevant: Beim Metabolismus von Medikamenten besteht ein genetischer Polymorphismus mit unterschiedlichen Metabolisierer. Hierzu zählen u.a. der "extensive" Metabolizer und der "poor"-Metabolizer (5-10% in Europa). Bei den Langsammetablizer können sich sehr hohe Propafenon-Plasmaspiegel sowie eine komplette ß-Blockade manifestieren.
→ Dosierung: Es wird bei der Behandlung von supraventrikulären und ventrikulären Tachykardien mit einer Initialdosis von 3x 150mg/d begonnen. Eine Dosissteigerung sollte erst nach 3-4Tagen erfolgen bis zu einer Maximaldosis von 900mg/d.
→ Nebenwirkungen:
→ I: Allgemein: Propafenon weist bei normaler Dosierung selten Nebenwirkungen auf.
→ II: Kardial: Schwerwiegende unerwünschte Wirkungen sind insbesondere Herzarrhythmien (die arrhythmogene Potenz des Propafenon scheint bei linksventrikulären Funktionsstörungen und weiteren Vorerkrankungen des Herzens besonders hoch zu sein), bei Überdosierung Kammerflimmern und Asystolie. Bei Verbreiterungen des QRS-Komplexes ist ein sofortiger Therapieabbruch indizinert.
→ III: Extrakardial: Sind vor allem Tremor, Mundtrockenheit, Geschmacksstörungen, Übelkeit, Erbrechen hepatische Cholestase, Parästhesien, Kopfschmerzen, Sehstörungen, orthostatische Dysregulation, Schwindel, aber auch Potenzstörungen.
→ IV: Da Propafenon auch beta-blockierende Eigenschaften besitzt, kann sich bei disponierenden Patienten eine bronchiale Obstruktion verstärken.
→ Intoxikationszeichen:
→ I: Klinische Symptome einer Propafenonintoxikation sind Hypotonie, tonisch-klonische Krämpfe, Somnolenz bis hin zum Koma und Atemstillstand.
→ II: Echogardiographisch können sich höhergradige AV-Blockierungen (EKG-Befund: AV-Block), atriale und/oder ventrikuläre Störungen der Erregungsausbreitung, Sinusknotenautonomien, aber auch ventrikuläre Tachykardien und Kammerflimmern manifestieren.
→ Klinisch-relevant: In den CAST-Studien ist in der Behandlung von ventrikulären Heterotopien mit Propafenon/Flecainid bei Postinfarktpatienten eine höhere Letalität nachweisbar.
→ Kontraindikation: Sind insbesondere:
→ I: Zustand nach Myokardinfarkt und Herzinsuffizienz mit einer Ejektionsfraktion < 35%.
→ II: Schwere strukturelle Herzveränderungen wie die KHK.
→ III: Sinuskotensyndrom,
→ IV: AV-Block II/III Grades (EKG-Befund: AV-Block),
→ V: Bifaszikuärer Block,
→ VI: Obstruktive Lungenerkrankungen (z.B. COPD) und nicht zuletzt
→ VII: Die Schwangerschaft.
→ Wechselwirkungen:
→ I: Propafenon hemmt u.a. den Abbau von oralen Antikoagulantien, einigen Beta-Blockern wie Metoprolol oder Propranolol, Desipramin, Digoxin, Theophyllin etc.
→ II: Die Inhibition der CYP 2D6 durch Cimetidin, Chinidin hemmt den Abbau von Propafenon.
→ III: Rifampicin u.a. beschleunigt die Abbau von Propafenon.
→ IV: Lokalanästhetika verstärken die Wirkung von Propafenon.
- Details
- Geschrieben von: CF
- Kategorie: Antiarrhythmika
- Zugriffe: 14965
→ Definition: Bei Amiodaron handelt es sich um ein Klasse-III-Antiarrhythmikum und stellt biochemisch ein jodsubstituiertes Molekül dar, das insbesondere die spannungsabhängigen Kalium-Kanäle in der Repolarisationsphase blockiert und so zu einer selektiven Verlängerung des Aktionspotenzials führt.
→ Wirkung:
→ I: Amiodaron hemmt in der Repolarisationsphase die spannungsabhängigen Kalium-Kanäle.
→ II: Zudem blockiert es auch noch die Natrium- und Kalzium-Kanäle und verlangsamt hierdurch die Depolarisation der Schrittmacherzellen im Sinusknoten mit konsekutiver Abnahme der Herzfrequenz.
→ III: Agiert als nicht-kompetitiver Alpha- und Beta-Rezeptor-Antagonist, wodurch die Noradrenalin-Exozytose aus der peripheren sympathischen Nervenendigung unterbunden wird.
→ IV: Klinische Auswirkung ist eine elektrokardiograpisch nachweisbare Verlängerung des QRS-Komplexes und der PQ-Zeit.
→ Indikation:
→ I: Akuttherapie:
→ 1) Mittel der 1. Wahl bei hämodynamisch stabilen ventrikulären Tachykardie.
→ 2) Mittel der Wahl bei therapierefraktärem Kammerflimmern und pulsloser ventrikulärer Tachykardie.
→ 3) Schwere, z.T. therapieresistente supraventrikuläre - (z.B. Vorhofflimmern) und ventrikuläre Tachykardien bei bestehender linksventrikulärer Herzinsuffizienz. Beim Vorhofflimmern sollte es jedoch aufgrund der z.T. schweren Nebenwirkungen nur bei therapeutischen Versagen anderer Antiarrhythmika oder bei ventrikulärer Vorschädigung eingesetzt werden.
→ Pharmakokinetik:
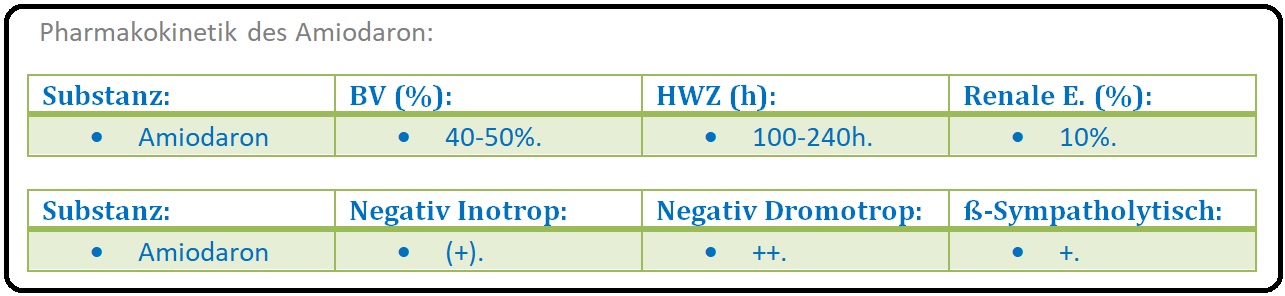
→ I: Nach oraler Applikation wird Amiodaron unvollständig resorbiert; die Bioverfügbarkeit ist sehr variabel und liegt (first-pass-Effekt) zwischen 25-80%.
→ II: Die Substanz wird in der Leber über die CYP 3A4 in den wirksamen Metaboliten Desethylamiodaron verstoffwechselt.
→ III: Die Elimination von Amiodaron und seines Hauptmetaboliten erfolgt sehr langsam, überwiegend biliär (Halbwertszeit liegt bei 52 Tagen).
→ IV: Die ausgeprägte Lipophilie der Substanz ruft eine große Affinität zu den verschiedenen Geweben (flaches Kompartiment Myokard, Muskeln), insbesondere zum tiefen Kompartiment (Fettgewebe, Kornea, Haut, Lunge, Leber, Nervengewebe) hervor.
→ V: Um eine schnelle therapeutische Wirkung zu erlangen, muss das Myokard mit Hilfe einer hohen Initialdosis aufgesättigt werden (Latenz von wenigen Tagen bis 2 Wochen). Anschließend wird eine geringere Erhaltungsdosis verabreicht.
→ VI: Dosierung:
→ 1) Die Aufsättigung wird durch die Gabe von 3x 200mg/d bis max. 3x 400mg/d oral über einen Zeitraum von 10-14 Tagen begonnen. Grund der hohen Aufsättigungsdosis ist die ausgeprägte Lipophilie von Amiodaron in den tiefen Kompartimenten der verschiedenen Gewebe.
→ 2) Erhaltungsdosis: Bei anhaltender Therapie sollte die Erhaltungsdosis maximal 200mg/d nicht überschreiten.
→ 3) Intravenöse Gabe: Initialdosis 5mg/kgKG über 5min, nach 15min ist eine Wiederholung möglich oder 300mg in einer 5%igen Glukoselösung über 20min. Bei intravenöser Applikation erfolgt der Wirkungseintritt nach wenigen Minuten, die maximale Wirkung wird nach 15min erreicht und eine Umverteilung in tiefere Kompartimente erfolgt nach 4 Stunden.
→ Klinisch-relevant: Bei vorzeitigem Übergang in die Erhaltungsdosis kann die Amiodaron-Dosis aufgrund einer Umverteilung in tiefere Kompartimente unter die therapeutisch wirksame Grenze fallen.
→ Nebenwirkungen: Die Nebenwirkungen entwickeln sich aufgrund der Ablagerung und Speicherung von Amiodaron in den verschiedenen Geweben. Hierzu zählen:
→ I: Extrakardiale Nebenwirkungen:
→ 1) Amiodaron-Keratopathie: Infolge von (gelbbraunen) Mikroablagerung in der Kornea und Entwicklung möglicher Sehstörungen. Ist zumeist innerhalb eines Zeitraumes von 6-12 Monaten nach Absetzten der Substanz reversibel.
→ 2) Haut: Durch Amiodaronablagerung kann sich eine Photosensibilität mit Ausbildung eines Erythems manifestieren; weitere dermatologische Veränderungen sind das Erythema nodosum und die Hyperpigmentierung.
→ 3) Leber: Isolierte Erhöhung der Transaminasen, evtl. Medikamentenhepatitis, cholestatischer Ikterus bis hin zur Leberzirrhose. Aber auch gastroenterologische Störungen mit Völlegefühl, Übelkeit, Erbrechen und Obstipation.
→ 5) Lunge: Eine sehr seltene, aber komplikationsreiche NW ist die alveoläre oder interstitielle Pneumonie mit der Gefahr der Ausbildung einer Lungenfibrose (insbesondere bei lang dauernder, hoch dosierter Anwendung).
→ 6) Nervensystem: Es können neurologische Symptome wie Kopfschmerzen, Schlafstörungen, Tremor, periphere Neuropathien wie Parästhesien und Ataxie hervorgerufen werden.
→ 7) Muskulatur: Vor allem die exogen-toxische Myopathie.
→ 8) Blutbildung: Bei Amiodaron besteht auch immer ein erhöhtes Risiko für die Entwicklung einer aplastischen Anämie.
→ Klinisch-relevant: Amiodaron hat zusätzlich Einfluss auf die Schilddrüsenfunktion.
→ A) Amiodaron blockiert die T4-Dejodase und verhindert somit die Umwandlung des weniger stoffwechselaktiven T4 in das aktive T3; Hierdurch entsteht das stoffwechselinaktive rT3 (reverse T3). Zudem antagonisiert die T3-Wirkung am Hormon-Rezeptor. Klinisches Korrelat ist die Hypothyreose.
→ B) Hyperthyreose: Der hohe Jodanteil im Amiodaronmolekül (37%) kann bei vorbestehender Schilddrüsenautonomie eine Hyperthyreose mit deutlich erhöhtem T3 bis hin zur thyreotoxischen Krisen auslösen.
→ II: Kardiale Nebenwirkungen:
→ 1) Bei zu schneller intravenöser Applikation kann es zum deutlichen Blutdruckabfall kommen.
→ 2) Proarrhythmische Wirkung mit Auslösung von Bradykardien, sinuatrialer oder atrioventrikuläre Überleitungsstörungen (EKG-Befund: AV-Block). Im Vordergrund der kardialen Nebenwirkungen steht jedoch die dosisabhängige Verlängerung des Aktionspotenziales und der QT-Zeit mit erhöhter Gefahr der Entwicklung von ventrikulären Extrasystolen bis hin zur Torsades-de-pointes-Tachykardie (EKG-Befund: Torsades-de-Pointes-Tachykardie).
→ 3) Prädisponierender Faktor für die Herzrhythmusstörungen durch Amiodaron ist die Hypokaliämie, die insbesondere durch Pharmaka wie Schleifendiuretika, Thiazide, Laxanzien etc. hervorgerufen werden kann.
→ Kontraindikationen: Bestehen für Amiodaron bei:
→ I: Kardiale Vorerkrankungen: Wie Bradykardie, Sick-Sinus-Syndrom, vorbestehende QT-Verlängerung, AV-Block II/III Grades (EKG-Befund: AV-Block), aber auch schwere arterielle Hypotonie und dekompensierte Herzinsuffizienz.
→ II: Jodallergie,
→ III: Schilddrüsenerkrankungen (insbesondere Hyperthyreose),
→ IV: Schwere (obstruktive) Lungenerkrankungen (z.B. COPD, Lungenemphysem),
→ V: In der Schwangerschaft und Stillzeit (= bei gebährfähigen Frauen sollte während der Amiodaron-Therapie eine ausreichende Kontrazeption erfolgen).
→ VI: Eine gleichzeitige Therapie mit MAO-Hemmern ist auch kontraindiziert.
→ Wechselwirkungen: Amiodaron ist nicht nur Substrat der CYP3A4, sondern stellt auch einen Inhibitor der CYP 1A2, CYP 2D6 und CYP 3A4 dar. Wichtige Wechselwirkungen bestehen bei der Kombination mit:
→ I: Phenprocoumon/Wafarin: Gefahr schwerer Blutungen.
→ II: Simvastatin: Erhöhtes Risiko für die Entwicklung einer Rhabdomyolyse.
→ III: Cyclosporin: Verstärkung der kardiotoxischen und zentralnervösen NW.
→ IV: Bei gleichzeitiger Therapie mit Betablockern und Ca2+-Antagonisten kommt es zu einem additiven Effekt am Sinus- und AV-Knoten.
→ V: Hemmung des Digoxinabbaus mit Gefahr der Digoxinintoxikation. Eine Umstellung auf Digitoxin ist möglich.
- Details
- Geschrieben von: CF
- Kategorie: Antiarrhythmika
- Zugriffe: 9317
→ Definition: Bei Ajmalin und Prajmalin handelt es sich neben dem Chinidin um Antiarrhythmika der Klasse Ia; sie werden insbesondere in der Behandlung der supraventikulären - und ventrikulären Tachykardien eingesetzt. Klasse-Ia-Antiarrhythmika binden nur an aktivierte Natrium-Kanäle und blockieren zusätzlich Kaliumkanäle, was wiederum zu einer Verlangsamung und einer verminderten Leitungsgeschwindigkeit führt.
→ Wirkungsmechanismus:
→ I: Ajmalin und Prajmalin blockieren die spannungsabhängigen Natrium+-Kanäle, insbesondere im His-Purkinje-System, Ventrikel und möglichen akzessorischen Leitungsbahnen. Charakteristikum ist die Verlängerung des Aktionspotenzials und der QT-Zeit (Abb.: Wirkung der Antiarrhythmika auf das Aktionspotenzial).
→ II: Im Vergleich zu Chinidin haben sie einen deutlich geringeren anticholinergen Effekt.
→ Indikation:
→ I: Mittel der Wahl in der Akuttherapie von supraventrikulären Tachykardien (= schmaler QRS-Komplex), auch infolge einer AV-Reentrytachykardie oder eines Präexzitationssyndroms (z.B. WPW-Syndrom).
→ II: Ventrikuläre Tachykardien (= breiter QRS-Komplex).
→ Klinisch-relevant: Gerade Ajmalin dient der nicht-invasiven Diagnostik von Rhythmusstörungen:
→ A) Nachweis akzessorischer Leitungsbahnen:
→ 1) Nach Gabe von 50mg Ajmalin i.v. erfolgt die elektrokardiographische Nachweis bzw. Verlustes der Delta-Wellen (= WPW-Syndrom).
→ 2) Sind die Delta-Wellen nicht mehr nachweisbar, spricht dies für eine lange Refraktärzeit der akzessorischen Leitungsbahnen. Hierbei besteht keine Gefahr für die Entwicklung eines plötzlichen Herztodes.
→ 3) Die Persistenz der Delta-Wellen steht elektrokardiographisch für eine kurze Refraktärzeit. Folglich ist eine Überleitung der Vorhoftachykardie auf die Kammer möglich.
→ B) Demaskierung eines Brugada-Syndroms: Nach Gabe von Ajmalin ist der Nachweis eines Rechtsschenkelblocks (EKG-Befund: Schenkelblock allgemein) kombiniert mit einer rechtspräkordialen ST-Elevation ein elektrokardiographisches Charakteristikum für das Vorhandensein eines Brugada-Syndroms.
→ Pharmakokinetik:
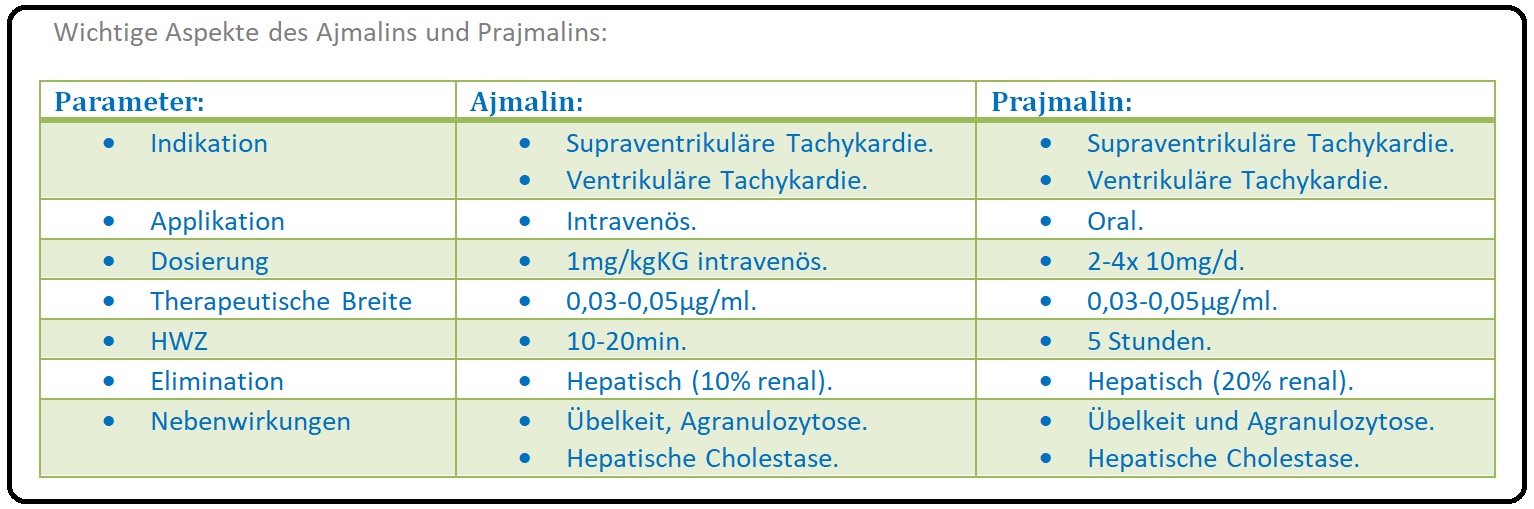
→ I: Ajmalin wird nur sehr schlecht enteral resorbiert, sodass es parenteral verabreicht wird. Nach i.v. Applikation hat es eine HWZ von unter einer Stunde (ca. 10-20min).
→ II: Prajmalin hat nach guter enteraler Resorption (80%) eine Bioverfügbarkeit von ca. 50% und eine mittlere HWZ von 5 Stunden.
→ III: Beide werden vorwiegend hepatisch ausgeschieden (= Prajmalin wir zu 20% unverändert renal eliminiert, Ajmalin zu 10%).
→ IV: Ajmalin weist im Vergleich zu Lidocain neben der besseren ventrikulären Tachykardieterminierung eine Steigerung des Herzzeitvolumens auf, sodass es sich in der Notfalltherapie der Ventrikeltachykardien etabliert hat.
→ Dosierung:
→ I: Ajmalin: Initial meist 10mg/min i.v. bis zu einer maximalen Einzeldosis von 50mg. Bei unzureichendem Erfolg kann eine Wiederholung nach 30min. erfolgen.
→ II: Prajmalin: Initialdosis von 60-80mg/d. Für die Dauertherapie reichen zumeist 2-4x10mg/d (40mg/d).
→ Nebenwirkungen:
→ I: Extrakardial:
→ 1) Appetitlosigkeit, Übelkeit, Erbrechen, evtl. intrahepatische Cholestase mit Fieber, Juckreiz, Ikterus und Transaminase-Anstieg sowie Leberschädigung.
→ 2) Kopfschmerzen, Lichtempfindlichkeit, Augenflimmern und Doppelbilder.
→ 3) Selten entwickeln sich eine Thrombozytopenie oder Agranulozytose.
→ II: Kardial:
→ 1) Höhergradige AV-Blockierung (EKG-Befund: AV-Block) bis hin zur Asystolie, aber auch
→ 2) Ventrikuläre Tachykardie bis hin zum Kammerflimmern.
→ Kontraindikationen: Sind u.a.:
→ I: Herzinsuffizienz und Myokardinfarkt.
→ II: Niereninsuffizienz (insbesondere bei Prajmalin).
→ III: Höhergradige atrioventrikuläre Erregungsleitungsstörungen.
→ IV: Auch ist eine Kombination mit weiteren Antiarrhythmika kontraindiziert.
- Details
- Geschrieben von: CF
- Kategorie: Antiarrhythmika
- Zugriffe: 9580
→ Definition: Bei Chinidin handelt es sich neben Ajmalin um ein Antiarrhythmika der Klasse I a und wird insbesondere zur Rezidivprophylaxe bei persistierendem Vorhofflimmern eingesetzt. Chinidin ist ein Alkaloid, das aus der Rinde des mittelamerikanischen Chinabaumes stammt.
→ Wirkung:
→ I: Die Substanz blockiert spannungsabhängige Na+-Kanäle, indem es an offene Natrium-Kanalprotein bindet; die Wirksamkeit ist am Na+-Kanal frequenzabhängig, da der Komplex so langsam dissoziiert, dass die Wirkung kumuliert. Zudem beeinflusst Chinidin auch die K+-Leitfähigkeit und führt hierüber zu einer verzögerten Repolarisation sowie zu einer Verlängerung des Aktionspotenzialdauer (und der Refraktärzeit). Beim K+-Kanal weist Chinidin eine umgekehrte Frequenzabhängigkeit auf; d.h. mit zunehmender Herzfrequenz nimmt die Blockade des Kalium-Stroms ab.
→ II: Vasodilatatorisch: Direkte Gefäßrelaxation mit Blutdruckabfall.
→ III: Parasympatolytisch:
→ 1) Die Hemmung der schnellen spannungsabhängigen Na+-Kanäle hat keinen Einfluss auf den Sinusknoten, da hier das Aktionspotenzial calciumabhängig ist, vielmehr bewirkt der anticholingere Effekt von Chinidin eine Frequenzsteigerung.
→ 2) Im AV-Knoten induziert Chinidin eine beschleunigte Überleitung.
→ Klinisch-relevant:
→ A)Aufgrund der verkürzten Überleitung im AV-Knoten, die durch eine Herabsetzung des zentralen Vagotonus und einen vermehrten Einfluss des Sympathotonus hervorgerufen wird, besteht die Gefahr, dass ein Vorhofflattern auf den Ventrikel übertragen werden kann. Folgen sind ventrikuläre Kammertachykardien, (= paradoxer Chinidineffekt) und Synkopen. Eine Kombination mit Verapamil ist obligat.
→ B) Chinidin hemmt neben den Na+- auch die Kaliumkanäle, die wiederum zu einer Verlängerung der Aktionspotenzialdauer im Vorhof und Ventrikel führt.
→ Indikation: Chinidin wird insbesondere zur medikamentösen Kardioversion eingesetzt:
→ I: Supraventrikuläre (und ventrikuläre Tachykardien) sowie SVES.
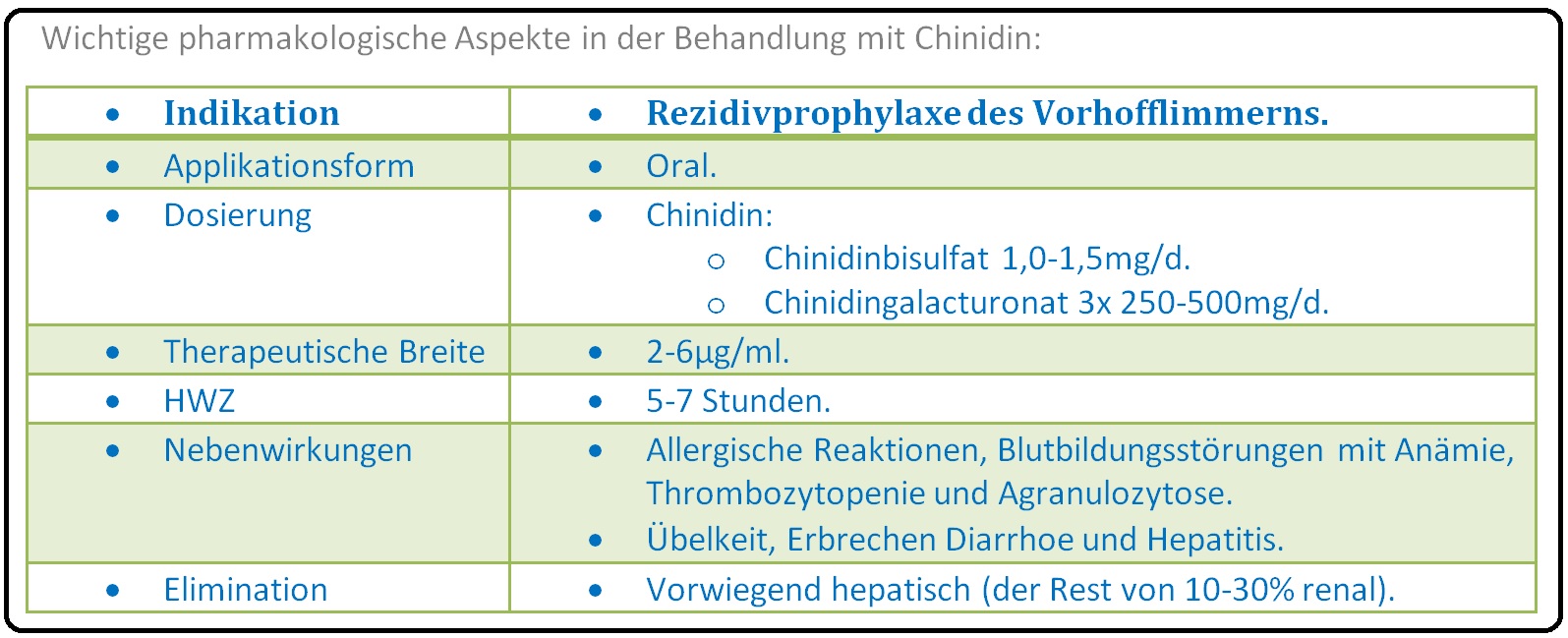
→ II: Rezidivprophylaxe bei persistierendem Vorhofflimmern nach erfolgreicher Kardioversion (ggf. in Kombination mit Verapamil).
→ III: Rezidivprophylaxe bei paroxysmalem, symptomatischem Vorhofflimmern.
→ Klinisch-relevant: Die Dauertherapie mit Chinidin vermindert zwar die Inzidenz des Vorhofflimmerns, steigert jedoch die Letalität, sodass es im Einsatz der Rezidivprophylaxe obsolet ist.
→ Pharmakokinetik: Nach enteraler Resorption (80%) tritt die Chinidinwirkung nach ca. 15min ein und erreicht ihr Maximum nach 1-3 Stunden. Die HWZ beträgt 5-7 Stunden, anschießend wird der Großteil des Chinidins (75%) durch Hydroxylierung hepatisch metabolisiert und der Rest (10-30%) unverändert renal eliminiert. Der therapeutische Plasmaspiegel liegt bei 3-6µg/ml. Die Substitution erfolgt ausschließlich oral, da die intravenöse Applikation erhebliche Nebenwirkungen (u.a. massiver Blutdruckabfall) aufweist.
→ Nebenwirkungen: Sie entwickeln sich aufgrund der antimuskarinischen Eigenschaften des Chinidin und sind u.a.:
→ I: Kardial:
→ 1) Erregungsleitungsstörungen wie Schenkelblock (u.a. Links- und Rechtsschenkelblock) und AV-Block (EKG-Befund: AV-Block) aber auch Gefahr der Entwicklung einer Herzinsuffizienz (aufgrund des negativ-inotropen Effektes).
→ 2) Blutdruckabfall.
→ 3) Chinidin kann eine Kammertachykardie bis hin zu einer Torsades-de-pointes-Tachykardie (EKG-Befund: Torsades-de-Pointes-Tachykardie) hervorrufen; dies wird als "paradoxer Chinidin-Effekt" bezeichnet.
→ 4) Zudem wirkt es proarrhythmisch.
→ Klinisch-relevant: Chinidin weist einen ausgeprägten anticholinergen Effekt auf, der wiederum der antiarrhythmischen Komponente entgegenwirkt und zu einer Steigerung der Herzfrequenz mit konsekutiver Beschleunigung der AV-Überleitung führt. Dies wird als paradoxe Chinidinwirkung bezeichnet.
→ II: Extrakardial:
→ 1) Anticholinerg: Mit Mundtrockenheit, verminderter Schweißbildung, Akkommodationsstörungen, Miktionsstörungen und gastrointestinalen Beschwerden (insbesondere Obstipation), etc.
→ 2) Neurotoxisch: Mit Lichtscheue, Farbsehstörungen, evtl. Nystagmus und Tinnitus.
→ 3) Gastrointestinal: Übelkeit, Erbrechen und Diarrhoe.
→ 4) Allergisch: Allergische Hautreaktionen (z.B. allergisches Erythem), selten entwickelt sich eine Knochenmarksdepression mit Thrombozytopenie (z.B. idiopathische thrombozytopenische Purpura, etc.), Agranulozytose und hämolytische Anämie. Eine initiale Testdosis dient der Vermeidung einer anaphylaktischen Reaktion.
→ 5) Cinchonismus: Hierbei handelt es sich um eine dosisabhängige Symptomatik mit Sehstörungen, Tinnitus bis hin zum Hörverlust, Erregung und Delir, aber auch Atem- und Kreislaufdepression können sich manifestieren.
→ Kontraindikationen: Hierzu zählen u.a.:
→ I: Herzinsuffizienz und Myokardinfarkt.
→ II: Herzrhythmusstörungen wie das Sick-Sinus-Syndrom, AV-Block Grad II/III und eine QT-Verlängerung (um mehr als 30% des Ausgangswertes).
→ III: Digitoxinintoxikation.
→ IV: Chinidin darf nicht mit anderen kardiodepressiven Medikamenten (z.B. Beta-Blockern, Parasympathomimetika, etc.) kombiniert werden.
→ Wechselwirkungen:
→ I: Chinidin hemmt den Abbau von oralen Antikoagulanzien (z.B. Macumar), tri- und tetrazyklischen Antidepressiva sowie Neuroleptika.
→ II: Zusätzlich verringert es die renale Clearance von Digoxin. Eine Dosisreduktion und Bestimmung des Plasmaspiegels ist diesbezüglich obligat.
→ III: Die Kalziumantagonisten, Verapamil, Diltiazem und Nifedipin sowie die Makrolide, etc. hemmen den Chinidinabbau.
→ IV: Barbiturate, Carbamazepin, Phenytoin, etc. beschleunigen durch Enzyminduktion den Abbau von Chinidin.